Научно-практический рецензируемый сетевой журнал «Вестник урологии» («Vestnik Urologii / Urology Herald») издаётся Ростовским государственным медицинским университетом. Первый выпуск опубликован 31 мая 2013 года.
Решением Высшей аттестационной комиссии при Министерстве науки и высшего образования Российской Федерации от 17.12.2019 года журнал включён в ПЕРЕЧЕНЬ рецензируемых научных изданий, в которых должны быть опубликованы основные научные результаты диссертаций на соискание учёной степени кандидата наук, на соискание учёной степени доктора наук. Научная специальность и соответствующая ей отрасль науки, по которой присуждаются ученые степени: 3.1.13 — Урология и андрология (медицинские науки)
22 ноября 2022 года журнал одобрен Консультативным советом по отбору контента Scopus (CSAB) для включения в международную базу данных SCOPUS.
Главный редактор: д-р. мед. наук, проф. Глухов Владимир Павлович (Ростов-на-Дону, Россия)
Первый заместитель главного редактора: д-р мед. наук, проф. Коган Михаил Иосифович (Ростов-на-Дону, Россия)
Заместитель главного редактора: канд. мед. наук Ильяш Анна Владимировна (Ростов-на-Дону, Россия)
Ответственный редактор: канд. мед. наук Исмаилов Руслан Самедович (Ростов-на-Дону, Россия)
Редакционная коллегия / редакционный совет: ведущие специалисты России, Европы, Азии и США
Тип рецензирования: двустороннее слепое (анонимное)
Научная тематика: общая урология, андрология, онкоурология, уроинфекциология, нейроурология, детская урология, женская урология, визуализация в урологии, эндоскопическая и лапароскопическая урология, реконструктивно-пластическая урология, трансплантология, анестезиология в урологии, урологическое образование, история урологии
Контент: оригинальные статьи, дискуссионные статьи, обзоры литературы, клинические наблюдения, лекции, история урологии, клинические рекомендации, новые медицинские технологии в урологии, отчёты о научно-образовательных мероприятиях
Читательская аудитория: урологи, андрологи, онкоурологи, детские урологи-андрологи, нефрологи, гинекологи, хирурги, трансплантологи, анестезиологи, врачи общей практики, научные сотрудники, специалисты фармакологических компаний
В своей работе редакция журнала «Вестник урологии» руководствуется правилами и рекомендациями:
- Комитета по этике научных публикаций (COPE)
- Всемирной ассоциации медицинских редакторов (WAME)
- Международного комитета редакторов медицинских журналов (ICMJE)
- Едиными стандартами представления результатов испытаний (CONSORT)
- Рекомендациями в отношении принципов, которые должны лежать в основе заявлений об издательской этике и недобросовестной издательской практике (PEMS)
Форма периодического распространения: сетевая
Тип доступа: открытый
Частота публикаций: ежеквартальная (4 выпуска в год); с 2024 года - 6 выпусков в год
Первый номер: 31 мая 2013
Языки: русский, английский
Территория распространения: Российская Федерация, зарубежные страны
Учредитель: федеральное государственное бюджетное образовательное учреждение высшего образования «Ростовский государственный медицинский университет» Министерства здравоохранения Российской Федерации
Поддержка: выпуск журнала осуществляется при поддержке профессиональной некоммерческой организации "Ассоциация Урологов Дона"
Адрес редакции: 344022, Россия, г. Ростов-на-Дону, пер. Нахичеванский, 29
E-mail редакции: urovest@mail.ru
Телефон редакции: +7 (863) 201-44-48
Свидетельство о регистрации средства массовой информации: Эл № ФС77-53256 от 22 марта 2013 года выдано Федеральной службой по надзору в сфере связи, информационных технологий и массовых коммуникаций (Роскомнадзор)
ISSN: 2308-6424
Текущий выпуск
ОРИГИНАЛЬНЫЕ СТАТЬИ
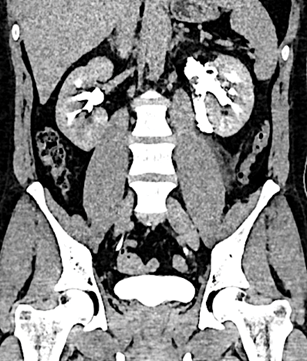
Введение. Мочекаменная болезнь (МКБ) является одним из наиболее распространённых и социально значимых урологических заболеваний. Доказанными факторами риска МКБ являются мужской пол и возраст пациентов. В общей популяции пациентов вероятность развития МКБ увеличивается с возрастом, однако факторы риска, связанные с полом, изучены недостаточно.
Цель исследования. Оценить возрастно-половые особенности пациентов с МКБ.
Материалы и методы. В настоящее исследование включены 23 464 пациента госпитализированных в урологическое отделение ГБУЗ «ГКБ №31 им. академика Г.М. Савельевой ДЗМ» в период с 2019 по 2024 год включительно. Исследуемую группу составили пациенты с установленным диагнозом «МКБ», в то время как все остальные пациенты с отсутствием МКБ составили контрольную группу.
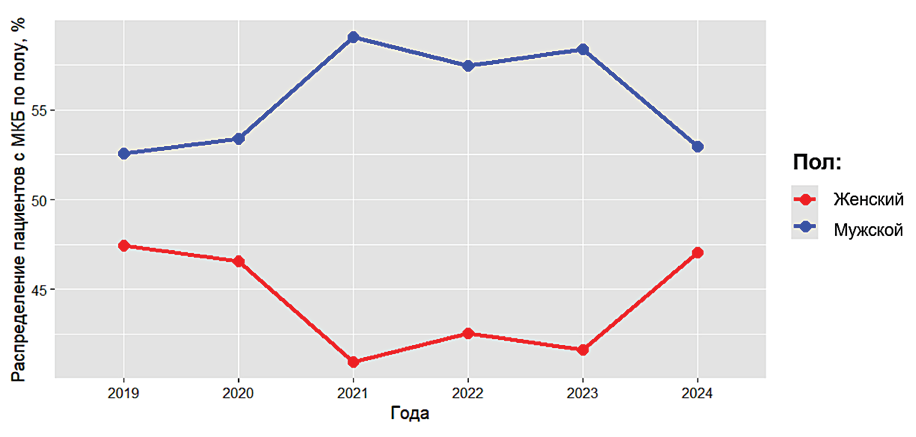
Результаты. Из 23 464 пациентов МКБ установлена у 38,2% (8972 человека). Среди пациентов с МКБ 55,9% случаев приходилось на мужчин (средний возраст мужчин с МКБ – 50,1 лет), в то время как 44,1% случаев – на женщин (средний возраст женщин с МКБ – 54,5 лет). Распространённость МКБ среди мужчин с возрастом постепенно растёт, выходя на плато в период с 30–34 лет до 45–49 лет. Максимальный шанс наличия МКБ характерен для возрастной группы 35–39 лет: для данной группы пациентов шанс наличия МКБ в 4,3 раза выше, чем для мужчин 18–24 лет (ОШ 4,326; 95% ДИ 3,433 – 5,449; p < 0,001, что соответствует вероятности наличия МКБ 68,8%). В дальнейшем отмечается постепенное снижение шанса наличия МКБ. Распространённость МКБ среди женщин с возрастом тоже увеличивается, достигая пика в возрастной категории 60–64 лет. Так, шанс наличия уролитиаза у женщин 60–64 лет в 3,4 раз выше, чем у женщин 18–24 лет (ОШ 1,553; 95% ДИ 1,242 – 1,943; p < 0,001, что соответствует 53,7% вероятности наличия МКБ). Для пациенток в возрасте 65 лет и старше шанс наличия МКБ остаётся стабильно высоким.
Заключение. Средний и пожилой возраст мужчин ассоциирован со снижением вероятности уролитиаза, в то время как этот же возраст у женщин с повышением вероятности уролитиаза. Такие особенности могут быть связаны с физиологическим изменением уровня половых гормонов, среди которых андрогены рассматриваются в качестве стимуляторов камнеобразования, а эстрогены – в качестве ингибиторов камнеобразования.
Введение. Хроническая болезнь почек (ХБП) представляет собой актуальную медико-социальную проблему, сопровождающуюся широким спектром осложнений, включая эректильную дисфункцию (ЭД) и нарушения репродуктивного здоровья. Эти состояния значительно снижают качество жизни мужчин с ХБП и усугубляются на фоне заместительной почечной терапии (ЗПТ).
Цель исследования. Изучить влияние ЗПТ в виде гемодиализа на эректильную функцию и репродуктивное здоровье пациентов с ХБП.
Материалы и методы. Проспективное наблюдение у 201 пациента мужского пола (средний возраст – 35,2 ± 1,9 года) с ХБП, получавших программный гемодиализ. Эректильную функцию оценивали по международному индексу эректильной функции (МИЭФ-5). Для диагностики гемодинамики в сосудах полового члена использовали ультразвуковое исследование с допплерографией артерий полового члена. Гормональный профиль пациентов изучали по уровням тестостерона, лютеинизирующего гормона, фолликулостимулирующего гормона, репродуктивную функцию – по спермограмме и объёму яичек. Все исследования выполняли на трёх этапах: исходно, при высокой азотемии, 12 месяцев после начала ЗПТ.
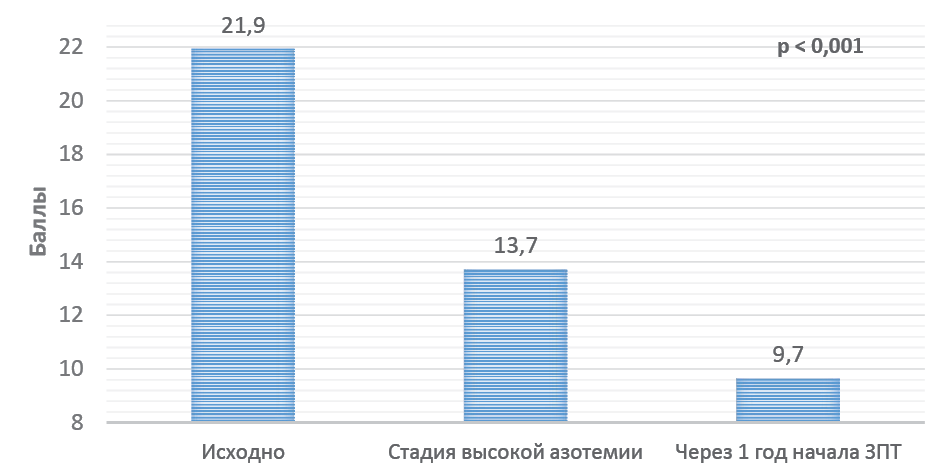
Результаты. Отмечено прогрессирование ЭД со снижением средних показателей по данным анкеты МИЭФ-5 с 21,9 до 9,7 балла (p < 0,001), причём доля умеренно-лёгкой ЭД увеличилась до 20,4%, умеренной – до 65,7%, тяжёлой – до 13,9%. Средний показатель пиковой систолической скорости в кавернозных артериях справа снизился с 6,5 ± 0,1 до 4,8 ± 0,1 см/с (p < 0,001), уровень тестостерона – с 5,1 ± 0,2 до 4,0 ± 0,2 нг/мл (p < 0,001), лютеинизирующего гормона – с 8,9 ± 0,1 до 6,9 ± 0,1 (p < 0,001), фолликулостимулирующего гормона – с 6,3 ± 0,1 до 5,0 ± 0,1 (p < 0,001), частота нормоспермии – с 59,2% до 50,7% (p < 0,001), с увеличением случаев патологического нарушения сперматогенеза (астенозооспермия, олигозооспермия, олигоастенотератозооспермия) в совокупности до 14,0% (p < 0,001).
Заключение. ХБП и гемодиализ вызывают многофакторные нарушения эректильной и репродуктивной функций, обусловленные сосудистыми, гормональными и структурными изменениями.
Введение. Интерстициальный цистит (ИЦ), являясь хроническим неинфекционным заболеванием, до сих пор имеет неясную этиологию и многочисленные патофизиологические теории развития. Это определяет необходимость проведения доклинических экспериментальных исследований на животных. Наиболее тождественной моделью ИЦ человека является циклофосфамид-индуцированный цистит у грызунов.
Цель исследования. Изучение эффектов фармакологической активности препарата Неоваскулген® в сравнении с препаратом Ботокс® на модели ИЦ у крыс, вызванного циклофосфамидом.
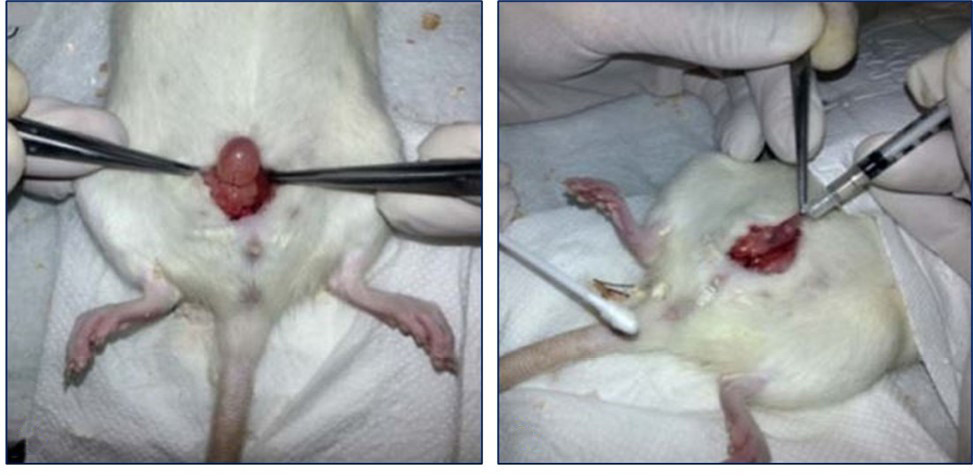
Материалы и методы. Исследование выполнено на 90 самках крыс линии Wistar. Индукция ИЦ проведена препаратом Эндоксан®. В качестве терапевтических средств применяли препараты Неоваскулген® и Ботокс®. Эффективность оценивали сравнительным анализом уродинамических паттернов и морфологически. Полученные данные обрабатывали параметрическими и непараметрическими методами статистического анализа.
Результаты. Индуцированный ИЦ развился у всех животных. Оба препарата статистически значимо улучшили изучаемые уродинамические показатели, клиническая эффективность Неоваскулген® была сравнима с Ботоксом®. Морфологическая оценка показала, что введение исследуемых препаратов сопровождалось снижением отёка тканей, меньшей выраженностью кровоизлияний и очаговой лимфогистиоцитарной инфильтрации, а также деструктивных изменений слизистой мочевого пузыря. При этом интенсивность патологических тканевых процессов на фоне введения Неоваскулгена® была наименьшей.
Заключение. Модель циклофосфамидного ИЦ считается наиболее адекватной ИЦ человека. Проведённый эксперимент крайне важен для изучения эффективности нового лекарственного препарата, которым является Неоваскулген®. Препарат показал свою эффективность в снижении частоты мочеиспусканий и внутрипузырного давления. Внутридетрузорное введение уменьшает остроту воспалительной реакции тканей мочевого пузыря.
Введение. Глубокий эндометриоз (ГЭ) – это наиболее тяжёлая форма заболевания, при которой поражается не только репродуктивная система, но и соседние органы с развитием серьёзных последствий. По частоте вовлечения в ГЭ мочевыделительная система занимает второе место.
Цель исследования. Изучить клинико-анамнестические особенности течения глубокого инфильтративного эндометриоза с вовлечением мочевого пузыря.
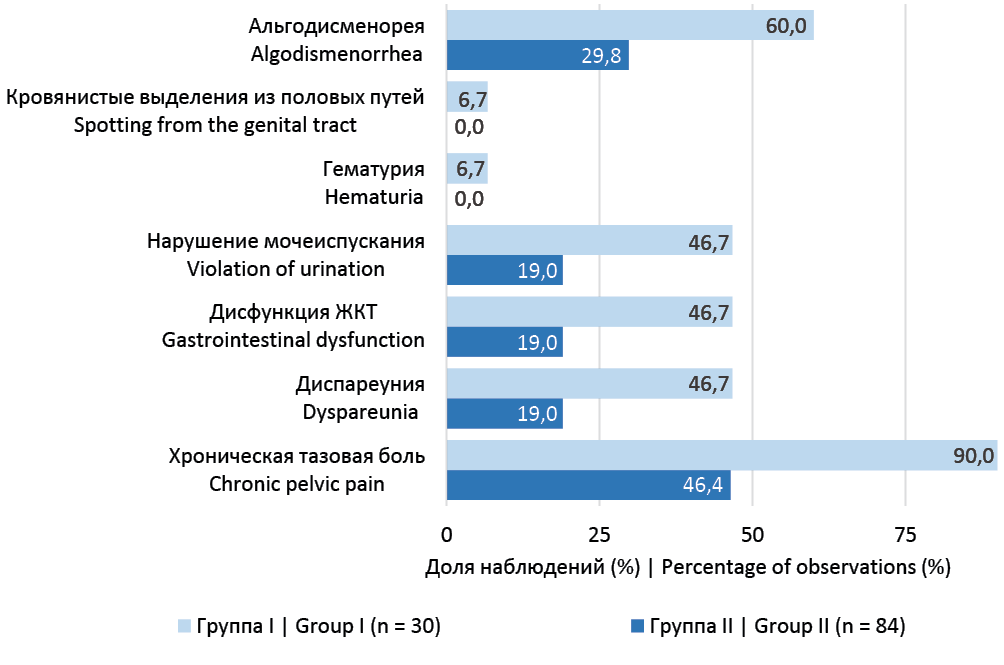
Материалы и методы. Проведён ретроспективный анализ данных 114 женщин, проходивших хирургическое лечение глубокого инфильтративного эндометриоза. Пациентки были разделены на две группы в зависимости от наличия (группа 1, n = 30) или отсутствия (группа 2, n = 84) поражения мочевого пузыря или пузырно-маточного углубления.
Результаты. Интенсивность симптомов, которые вынуждают пациенток обратиться за медицинской помощью, проявляется начиная с 30 лет. Промежуток между первым посещением врача в связи с эндометриозом и датой операции составляет 11,6 [7,0; 37,1] месяцев в группе 1 и 13,1 [4,7; 31,5] месяцев – группе 2 (p = 0,450). Самым частым симптомом была хроническая тазовая боль 66/114 (60,0%): группа 1 – 27/30 (90,0%); группа 2 – 39/84 (46,4%) (p = 0,000). Симптомы нижних мочевых путей встречались достоверно чаще в группе женщин с вовлечением детрузора в эндометриоидный инфильтрат: группа 1 – 14/30 (46,7%), группа 2 – 16/84 (19%) (p = 0,000). Симптомы нарушения мочеиспускания манифестировали за 1 – 2 суток до начала или в первый день менструаций. Эндометриоидный инфильтрат во всех случаях поражал заднюю стенку тела мочевого пузыря. Лапароскопическая резекция мочевого пузыря была выполнена в 17/30 (50,0%) случаях.
Заключение. Женщины, страдающие ГЭ с вовлечением мочевого пузыря, имеют более тяжёлое течение заболевания. Вовлечение мочевого пузыря в ГЭ наблюдается, как правило, при рецидиве эндометриоидной болезни. При подозрении на эндометриоидное вовлечение мочевого пузыря стоит прицельно исследовать заднюю стенку тела мочевого пузыря.
Введение. Пункционная биопсия почки является распространённой манипуляцией среди пациентов нефрологического и онкоурологического профилей. Морфологическое прижизненное исследование ткани почки проводят с целью уточнения диагноза, стадии патологического процесса, определения дальнейшей тактики лечения и оценки прогноза. В данном исследовании рассматривается текущая практика биопсии почек при различных патологических состояниях.
Цель исследования. Оценить эффективность и безопасность выполнения биопсии почки при различных патологических состояниях, а также анализ структуры осложнений, частоты и факторов риска их развития.
Материалы и методы. Проведён ретроспективный анализ пациентов, которым в период с января 2018 года по сентябрь 2023 года была выполнена чрескожная пункционная биопсия почки в ПСПБГМУ им. акад. И.П. Павлова. В данное исследование был включён 1 201 пациент в возрасте от 18 до 84 лет. Биопсия по поводу новообразований почки была выполнена 24 пациентам, для уточнения нефрологического диагноза – 1177 больным. Изучали диагностическую ценность биопсии в зависимости от количества взятых биоптатов. Регистрируемые осложнения после биопсии распределяли по тяжести в соответствии с классификацией Clavien-Dindo. Осложнение классифицировали как серьёзное, если оно требовало таких вмешательств, как переливание крови, радиологическое или хирургическое вмешательство.
Результаты. В исследовании приняли участие 625 мужчин (52%), средний возраст которых составил 57 ± 15 лет, и 576 женщин (48%), средний возраст которых – 55 ± 17 лет. Информативность материала не различалась у пациентов, которым был выполнен забор двух и более биоптатов: диагностическая ценность у них составила от 83% до 91% и превысила случаи с забором одного столбика ткани (46,4%, p = 0,002). Осложнения после нефробиопсии возникли у 122 пациентов (10,2%). Серьёзные осложнения наблюдались у 15 (1,2%) пациентов, одному из которых (0,08%) потребовалось срочное оперативное вмешательство в объёме нефрэктомии, а 9 (0,7%) пациентам была выполнена ангиография с эмболизацией почечных артерий. Летальных исходов зарегистрировано не было. В большинстве случаев развитие осложнений было диагностировано в первые 6 часов после биопсии (n = 112, 91,8% от общего числа осложнений). Больший процент осложнений наблюдался у лиц женского пола, пациентов более молодого возраста, пациентов, имеющих более высокий уровень азотемии и повышенные показатели МНО и ПТИ. Также большее число осложнений наблюдалось у пациентов с артериальной гипертензией. В отношении количества выполненных вколов частота развития кровотечения в послеоперационном периоде оказалась выше у пациентов, которым было выполнено 4 вкола (p = 0,044).
Заключение. Биопсия почки является малоинвазивной, относительно безопасной процедурой. Для информативности и минимизации риска развития осложнений достаточно взятия двух столбиков ткани. Предварительная оценка факторов риска развития осложнений, коррекция модифицируемых факторов риска (артериальная гипертензия, коагулопатия), наблюдение в послеоперационном периоде (не менее шести часов) позволяют свести к минимуму риск развития осложнений после биопсии.
Введение. Современные подходы к диагностике рака предстательной железы (РПЖ) включают использование мультипараметрической магнитно-резонансной томографии (мпМРТ) и биопсии простаты. Fusion-биопсия, объединяющая данные мпМРТ и ультразвукового исследования (УЗИ), позволяет повысить точность диагностики. Тем не менее остаются вопросы о целесообразности использования таргетных и стандартных биопсий, а также об их диагностической ценности в зависимости от доступа.
Цель исследования. Сравнить эффективность трансректальной и трансперинеальной fusion-биопсии предстательной железы, проанализировать вклад таргетных и стандартных биоптатов в диагностическую точность каждой методики, оценить возможность сокращения количества биоптатов для снижения осложнений, уменьшения длительности процедуры и экономической оптимизации диагностики.
Материалы и методы. Это сравнительное исследование, проведённое в период с октября 2024 по январь 2025 года в СПб ГБУЗ «Клиническая больница Святителя Луки». В исследование были включены 162 пациента с подозрением на РПЖ. В первой группе пациентов (n = 115) была выполнена трансректальная fusion-биопсия предстательной железы под ТРУЗИ-контролем. Второй группе пациентов (n = 47) была выполнена трансперинеальная fusion-биопсия предстательной железы стабилизированным методом при помощи степпера и стабилизатора.
Результаты. При трансректальной fusion-биопсии РПЖ был выявлен в 54 случаях (46,95%) при анализе таргетных биоптатов и в 81 (70,4%) случае при анализе стандартных биоптатов. Стандартные биоптаты самостоятельно выявили рак в 44 (38,26%) случаях, тогда как таргетные биоптаты в 5 (4,34%) случаях. При этом в 6 (5,22%) случаях таргетные биоптаты обеспечили повышение балла по шкале Gleason. Отказ от стандартных биоптатов при трансректальной методике привел бы к снижению выявляемости рака на 38,26%, включая агрессивные формы в 9,57% случаев. В группе трансперинеальной fusion-биопсии РПЖ был выявлен в 31 (65,96%) случае по результатам таргетных биоптатов и в 25 (53,19%) случаях – по результатам стандартных биоптатов. Только таргетные биоптаты выявили рак в 9 (19,15%) случаях, тогда как стандартные биоптаты добавили лишь 3 (6,38%) случая, все из которых соответствовали ISUP 1. Повышение балла Gleason на основании таргетных биоптатов наблюдалось в 4 случаях (8,51%).
Заключение. При трансперинеальной методике отказ от стандартных биоптатов может позволить сократить количество забираемых образцов без значительного ухудшения диагностической точности. В то же время для трансректальной fusion-биопсии стандартные биоптаты остаются важным компонентом, особенно для выявления агрессивных форм рака и повышения точности диагностики.
Введение. В структуре общего травматизма повреждения почек составляют от 2 до 10% случаев. Вопрос лечения разрыва почки, проникающего в чашечно-лоханочную систему (ЧЛС), является дискутабельным. В последнее десятилетие появляются данные, подтверждающие высокую эффективность консервативного метода лечения в соответствии с протоколами non-operative management (NOM).
Цель исследования. Определение оптимальной тактики лечения закрытой травмы почки, проникающей в чашечно-лоханочную систему.
Материалы и методы. В исследование включены 43 пациента, находившихся на стационарном лечении в Научно-исследовательском институте скорой помощи им. И.И. Джанелидзе с 1998 года по 2023 год, с закрытой травмой почки, проникающей в ЧЛС. Пациенты были разделены на две группы – проспективную и ретроспективную. Тяжесть повреждений почки оценивали по шкале Американской ассоциации хирургической травмы (AAST). В соответствии с балльной оценкой Ю.Н. Цибина проводили оценку тяжести травматического шока. Лечение травм почек, проникающих в ЧЛС, проводили консервативным и хирургическим способами.
Результаты. Медиана возраста у пациентов составила 43 [35 – 55] года. Соотношение мужчин и женщин составило 32:11. Лечение большинства пациентов из проспективной группы проводили консервативным (n = 12) и малоинвазивным (n = 9) способами. В ретроспективной группе всем пострадавшим (n = 21) выполняли открытые хирургические вмешательства. В ретроспективной группе отмечалась более высокая частота выполнения нефрэктомий. Частота развития осложнений и летальность у пациентов разных групп статистически достоверно не различались.
Заключение. Консервативный способ является оптимальным при лечении закрытой травмы почки, проникающей в ЧЛС. В случаях развития мочевых затёков следует выполнять стентирование мочеточника или пункционную нефростомию.
Введение. Стрессовое недержание мочи (СНМ) – распространённое заболевание, которое может существенно нарушать качество жизни женщин. Несмотря на эффективность слинговых операций, предоперационные страхи у пациенток остаются малоизученной темой, хотя могут влиять на исход лечения и удовлетворённость результатами.
Цель исследования. Изучить предоперационные страхи у пациенток со стрессовым недержанием мочи и выявить ассоциированные с ними факторы.
Материалы и методы. В исследование включены 720 женщин с диагнозом «СНМ», которым планировалось выполнение слинговой операции. Для оценки предоперационных страхов использовали авторскую анкету, а также шкалу тревоги и депрессии HADS.
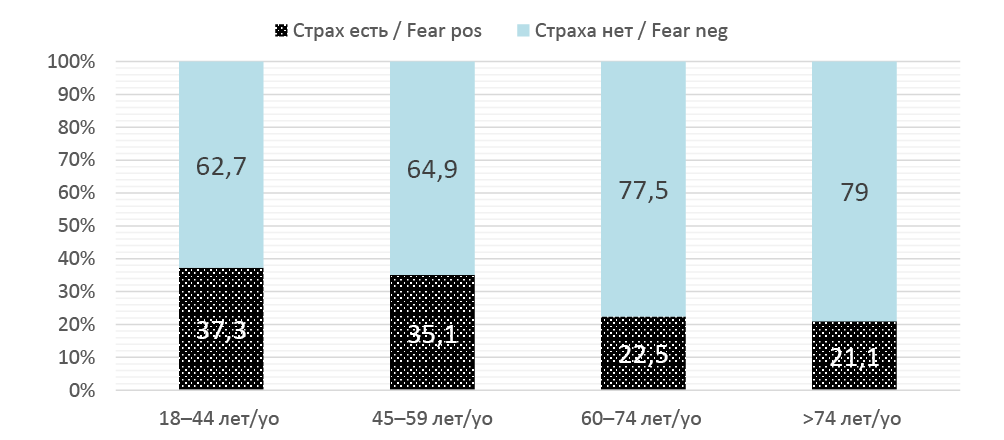
Результаты. До 77% женщин с СНМ сообщили о наличии одного или нескольких предоперационных страхов. Наиболее частыми были страх сохранения подтекания мочи (45,1%), осложнений, связанных с протезом (30,4%) и обезболиванием (25,8%). Женщины, испытывавшие страх, достоверно чаще были замужем (71% против 62,3%; p = 0,039), ранее перенесли реконструктивные операции (45,8% против 36,4%; p = 0,037). Чем выше уровень предоперационной тревоги / депрессии у пациенток с СНМ, тем больше у них страхов перед операцией. Страх осложнений с протезом чаще наблюдался у женщин моложе 60 лет, с высшим образованием, работающих и проживающих в городе. Страх, связанный с обезболиванием, был более распространён у работающих и ранее не оперированных женщин. Страх сохранения симптомов недержания чаще встречался у замужних женщин и тех, кто ранее проходил реконструктивное лечение. Результаты множественной логистической регрессии показали, что независимыми факторами, ассоциированными с предоперационными страхами, являются семейный статус, наличие / отсутствие депрессии и место проживания.
Заключение. Информация о наличии и характере предоперационных страхов у пациенток с СНМ может быть использована при подготовке женщин к операции с целью нормализации их психологического состояния и улучшения течения послеоперационного периода.
ОБЗОРЫ ЛИТЕРАТУРЫ
Введение. Стриктура пузырно-уретрального анастомоза является частым и клинически значимым осложнением радикальной простатэктомии, приводящим к инфравезикальной обструкции и выраженному снижению качества жизни. Несмотря на широкое применение эндоскопических, стентирующих и реконструктивных методов, частота рецидивов остаётся высокой, а выбор оптимальной тактики лечения – дискуссионным. Необходим всесторонний анализ эффективности и безопасности доступных подходов.
Цель исследования. Оценить и сопоставить результаты различных методов лечения стриктур пузырно-уретрального анастомоза (ПУА), развивающихся после радикальной простатэктомии с акцентом на эффективность восстановления проходимости, частоту рецидивов, риск развития недержания мочи и качество жизни пациента.
Материалы и методы. Проведён систематический обзор и метаанализ в соответствии с рекомендациями PRISMA. В базах Medline/PubMed, Embase и Cochrane Library был выполнен поиск оригинальных исследований, включавших ≥ 5 пациентов с подтверждёнными стриктурами ПУА, получавших лечение одним из трёх методов: эндоскопическим, стентированием или открытой реконструкцией. Основными исходами служили эффективность (отсутствие рестеноза), безопасность (осложнения, недержание), функциональные результаты и частота повторных вмешательств. Два рецензента независимо оценивали исследования, производили извлечение данных и оценку риска смещения (ROBINS-I). Качество доказательств определяли с использованием GRADE.
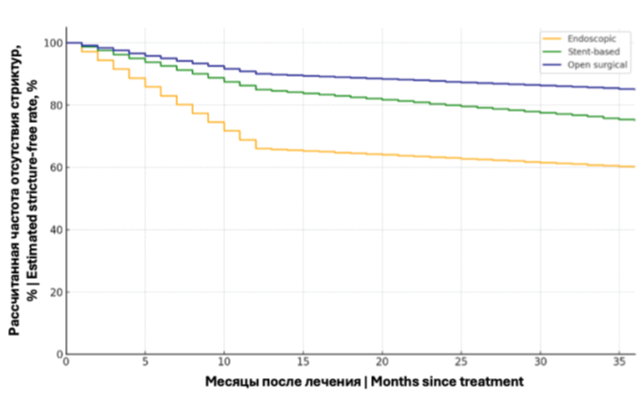
Результаты. В анализ включены 24 исследования (n = 745 пациентов), преимущественно ретроспективных серий случаев. Эндоскопические методы обеспечили первичную эффективность в 55% случаев (95% ДИ 40 – 70%), совокупную — до 91% при повторных вмешательствах. Риск рецидива в течение 1 – 2 лет — до 40%, de novo недержания — ≤ 5%. Временные стенты (Memokath®️, Allium®️) продемонстрировали проходимость до 93%, риск миграции — 7%, недержания — ≤ 10%. Открытые реконструкции, включая уретропластику с буккальным графтом, достигли успеха у 73 – 85% пациентов, однако сопровождались новым недержанием в 40 – 75% случаев. У пациентов после лучевой терапии эффективность снижалась почти в 5 раз (OR 0,20; 95% ДИ 0,05 – 0,80).
Заключение. Эндоскопия — оптимальный первичный подход с минимальным риском недержания, но высоким шансом рецидива. Стенты могут быть эффективным промежуточным решением при рецидивах. Открытая реконструкция – наиболее радикальный и результативный метод при сложных случаях, сопряжённый с высоким риском инконтиненции. Выбор метода должен быть индивидуализирован с учётом анамнеза, предшествующей лучевой терапии и цели сохранить континенцию.
Введение. Биопсия является стандартом верификации злокачественного новообразования простаты. Отрицательная первичная биопсия простаты не исключает отсутствие у пациента рака предстательной железы (РПЖ) при дальнейшем наблюдении. В настоящем обзоре рассмотрены различные методики выполнения повторной биопсии и результаты эффективности диагностики клинически значимого РПЖ.
Цель исследования. Изучить различные методики повторной биопсии простаты и оценить эффективность диагностики клинически значимого РПЖ.
Материалы и методы. Проведён обзор электронных баз данных PubMed, eLibrary с 2000 по 2024 год, чтобы выявить все соответствующие исследования. Электронный поиск был ограничен русским и английским языком, использовали ключевые слова: «повторная биопсия простаты», «клинически значимый рак предстательной железы», «fusion-биопсия».
Результаты. В настоящее время для выполнения повторной биопсии предстательной железы возможно использование следующих техник: сатурационная биопсия, микро-УЗИ, гистосканирование и fusion-биопсия. Сатурационная биопсия сопряжена с увеличением количества осложнений, гистосканирование не показало высокой эффективности, микро-УЗИ не так распространено и ограничено количеством исследований. Преимущество диагностики клинически значимого РПЖ у пациентов с предыдущим отрицательным гистологическим заключением на сегодняшний день за fusion-биопсией. Особенностью является возможность выбора одной из трёх техник выполнения: аппаратная, когнитивная и in bore.
Заключение. Наилучшие результаты эффективности диагностики клинически значимых форм РПЖ при повторной биопсии показывает fusion-техника. По данным литературы, различные способы выполнения fusion-биопсии сопоставимы между собой.
Введение. Рак предстательной железы (РПЖ) является одним из наиболее распространённых онкологических заболеваний среди мужчин, что делает актуальным поиск новых методов его ранней диагностики. Существующие подходы, такие как определение уровня простатического специфического антигена (ПСА), обладают ограниченной специфичностью и чувствительностью, что подчёркивает необходимость разработки более точных и неинвазивных диагностических методов.
Цель исследования. Анализ современных исследований, посвящённых применению газовой хроматографии в сочетании с масс-спектрометрией (ГХ-МС) для выявления летучих органических соединений (ЛОС) в моче как потенциальных биомаркеров РПЖ, а также оценка перспектив использования данного метода в клинической практике.
Материалы и методы. В работе проведён анализ научных публикаций, доступных через базы данных PubMed, Medscape и eLibrary, за период с 2019 года по 2024 год. Основное внимание уделено исследованиям, посвящённым метаболомному профилированию мочи с использованием ГХ-МС, а также изучению изменений метаболических путей в клетках РПЖ.
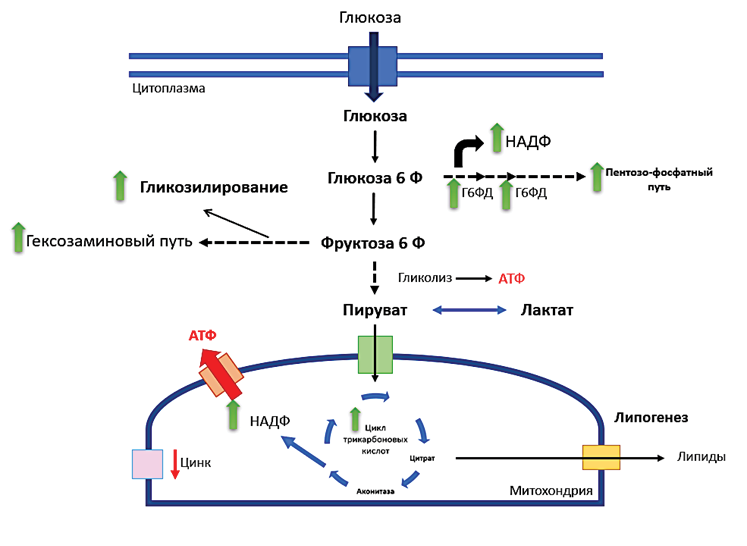
Результаты. Результаты исследований демонстрируют, что ГХ-МС позволяет выявить специфические ЛОС, ассоциированные с опухолевой трансформацией клеток предстательной железы. Показано, что данный метод обладает высокой диагностической точностью, превышающей традиционные подходы, такие как определение уровня ПСА. В частности, выявлены метаболиты, такие как саркозин, ацилкарнитин и арахидоноиламин, которые демонстрируют высокую чувствительность и специфичность в диагностике РПЖ. Также отмечены изменения в углеводном и липидном обменах, а также активация пентозофосфатного пути в клетках РПЖ.
Заключение. Применение ГХ-МС для анализа ЛОС в моче представляет собой многообещающий метод диагностики РПЖ, обладающий высокой точностью и неинвазивностью. Однако внедрение данного метода в клиническую практику требует решения ряда технических и методологических вопросов, включая стандартизацию протоколов и снижение стоимости оборудования. Дальнейшее развитие метаболомики и совершенствование аналитических методов могут существенно улучшить раннюю диагностику РПЖ, что положительно скажется на прогнозе и качестве жизни пациентов.
КЛИНИЧЕСКИЕ НАБЛЮДЕНИЯ
Введение. Редким, но клинически значимым осложнением лучевой терапии органов малого таза является лучевой цистит, проявляющийся упорной макрогематурией на фоне постепенного ишемического повреждения слизистой мочевого пузыря. Стандартные методы лечения, такие как промывание мочевого пузыря, инстилляции и эндоскопические коагуляционные методики, нередко дают лишь кратковременный эффект и не устраняют патогенетические механизмы процесса. Гипербарическая оксигенотерапия (ГБО), за счёт улучшения доставки кислорода в гипоксические ткани, рассматривается как перспективный вариант, стимулирующий ангиогенез и репарацию повреждённых тканей.
Описание наблюдения. Представлено наблюдение 77‑летнего пациента с длительной макрогематурией в течение двух недель; в анамнезе – рак предстательной железы, диагностированный в 2016 году, по поводу которого больной получал лучевую терапию (последний сеанс в 2018 году). При гибкой цистоскопии визуализирована диффузная кровоточивость и очаговые признаки раздражения слизистой мочевого пузыря. Лабораторно выявлена анемия (гемоглобин 9,6 г/дл) без признаков нарушения функции почек и коагулопатии. На фоне персистенции гематурии после промывания мочевого пузыря было начато лечение с применением ГБО; уже после десяти сеансов кровотечение полностью купировано. Отмечены лёгкие побочные эффекты в виде кратковременной тошноты и рвоты, успешно контролируемые медикаментозно. При последующем наблюдении рецидивов гематурии не зарегистрировано, что подтверждает устойчивый эффект проведённой терапии.
Заключение. Представленный случай демонстрирует эффективность и безопасность ГБО как неинвазивного метода лечения рефрактерного геморрагического цистита, являющегося осложнением лучевой терапии. У пациентов, не отвечающих на стандартные подходы, ГБО может рассматриваться как патогенетически обоснованная альтернатива, направленная на коррекцию ишемического повреждения стенки мочевого пузыря, а не только на купирование симптомов. Необходимы дальнейшие исследования для унификации протоколов применения ГБО и оценки отдалённых результатов.
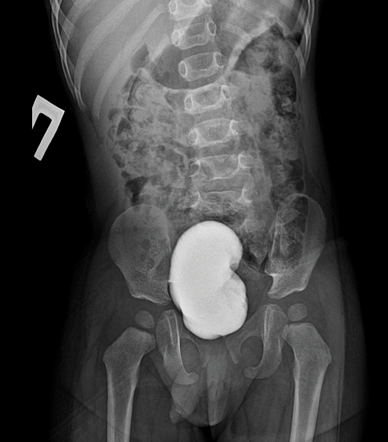
Воспалительная миофибробластная опухоль (ВМО) – редкая опухоль, характеризующаяся пролиферацией веретенообразных клеток с инфильтрацией воспалительными клетками. ВМО называют также воспалительной псевдоопухолью или псевдосаркоматозной миофибробластической опухолью. Несмотря на редкость (составляет менее 1% всех опухолей мочевого пузыря), мочевой пузырь является наиболее частой локализацией ВМО среди всех органов мочеполового тракта. В публикации мы описываем пациента М., 1 год 7 месяцев, у которого были жалобы на затруднения и боли при мочеиспускании в течение 2 месяцев. После проведённого обследования (УЗИ, микционной цистографии, КТ брюшной полости и малого таза, цистоуретроскопии, МРТ органов малого таза) ребёнку выполнено хирургическое лечение – иссечение (энуклеация) опухоли в пределах здоровых тканей. После гистологического исследования установлен диагноз «Воспалительная миофибробластная опухоль». В течение последних 2 лет ребёнку выполняли УЗИ, КТ, МРТ: признаков рецидива не выявлено, что подтверждается данными литературы о низком уровне рецидивов опухоли после щадящих видов хирургического лечения и отсутствия химиотерапии.
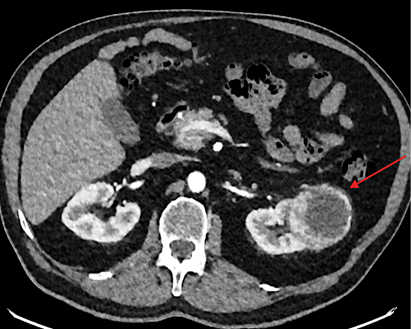
Кожные метастазы – редкая локализация вторичных очагов, ещё реже очаги вторичного генеза обнаруживаются в коже головы и шеи. В статье описан клинический случай выявления двух новообразований щёчной и поднижнечелюстной области у пациента 61 года без онкологических заболеваний в анамнезе. Данные обследования показали гиперваскулярную структуру образований, что позволило предположить диагноз сосудистой мальформации. Однако по результатам гистологического исследования были обнаружены метастазы светлоклеточной почечно-клеточной карциномы в кожу. Дальнейшее обследование привело к выявлению опухоли левой почки и вторичных очагов обоих легких. Описанный клинический случай призывает дерматологов и челюстно-лицевых хирургов проявлять настороженность в отношении пациентов с изолированными кожными образованиями с целью не пропустить нетипичные метастазы опухоли почки.
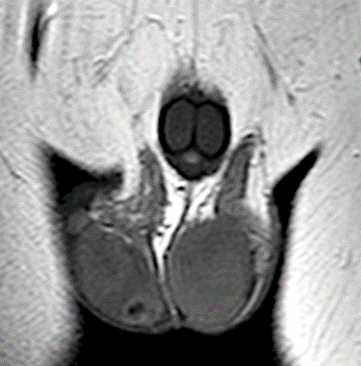
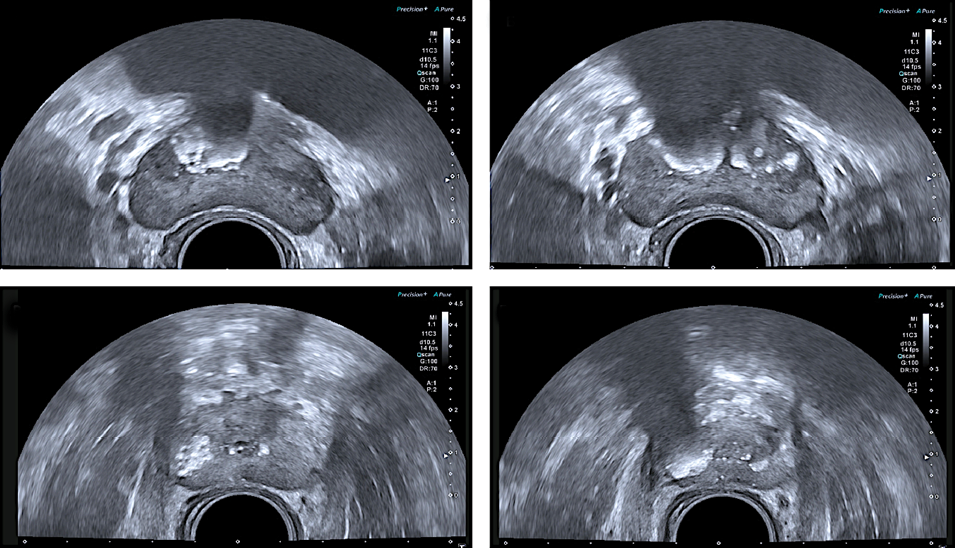
Интратестикулярные кисты в последние десятилетия стали нередкой находкой в клинической практике. По данным исследований, такие образования выявляются у 8,0 – 9,8% мужчин. Простые кисты паренхимы яичка не обладают злокачественным потенциалом и не требуют наблюдения или лечения. Однако важно дифференцировать их от кистозных новообразований, которые могут скрывать злокачественные процессы. В данной статье представлен клинический случай 30-летнего пациента, у которого при ультразвуковом исследовании выявлено кистозное образование правого яичка размером 7,1 × 6,9 × 8,5 мм с минимальным солидным компонентом. Первоначально была выбрана тактика динамического наблюдения с регулярным ультразвуковым контролем. Однако прогрессивное увеличение размеров образования потребовало хирургического вмешательства. С учётом малых размеров опухоли была предпринята попытка органосохраняющего лечения. Однако интраоперационное морфологическое исследование методом замороженных срезов выявило злокачественный характер образования, что привело к выполнению орхифуникулэктомии. Окончательное гистологическое исследование подтвердило диагноз «Эмбриональная карцинома». Данный клинический случай демонстрирует нетипичную манифестацию эмбрионального рака яичка в виде преимущественно кистозного образования с минимальным солидным компонентом. Представленное наблюдение дополняет существующие данные об ультразвуковой картине эмбрионального рака и подчёркивает важность тщательного динамического наблюдения даже за небольшими кистозными образованиями яичка.
Распространённость камней простаты, по данным различных исследований, варьируется от 7% до 99% и зависит от возраста пациентов. Простатические камни встречаются у 9% пациентов в возрасте 18 – 29 лет, у 32,3% пациентов – в возрасте 50 – 59 лет и у 66,7% пациентов – в возрасте 70 – 79 лет. Простатические камни, ассоциированные с гиперплазией предстательной железы (ГПЖ), часто остаются бессимптомными и являются случайной находкой во время трансуретральных вмешательств. Крупные и множественные простатические камни, а также камни, ассоциированные с хроническим воспалением в ткани простаты, могут вызывать неспецифические симптомы нижних мочевых путей (СНМП). Помимо этого считается, что у пациентов с наличием простатических камней может возникать гематурия, постмикционный дриблинг, недержание мочи, синдром хронической тазовой боли. Простатические камни, ассоциированные с хроническим воспалительным процессом в предстательной железе, могут являться субстратом бактериальной колонизации, способствуя селекции резистентных к антибактериальным препаратам микроорганизмов. Бессимптомные простатические камни не требуют специального лечения и чаще всего удаляются одномоментно во время оперативного лечения ГПЖ. В случае наличия симптоматических камней простаты эффективность консервативных методик, в частности антибактериальной терапии, ограничена в связи с тем, что камни сами по себе являются источниками персистирующей инфекции. В связи с этим для таких пациентов наиболее предпочтительным методом наряду с антибактериальной терапией является эндоскопическое удаление конкрементов. В рамках данной работы мы описали несколько собственных клинических наблюдений пациентов со множественными симптоматическими и бессимптомными камнями простаты, а также провели литературный обзор, посвящённый данной проблеме.