Перейти к:
Функциональное состояние детрузора при гиперплазии предстательной железы крупных и гигантских размеров до и после лапароскопической трансвезикальной аденомэктомии
https://doi.org/10.21886/2308-6424-2025-13-4-31-38
Аннотация
Введение. Лапароскопическая аденомэктомия является методом выбора в лечении гиперплазии предстательной железы (ГПЖ) крупных и гигантских размеров. Данный метод отличается эффективной коррекцией инфравезикальной обструкции, низкой частотой геморрагических осложнений и инконтиненции, уменьшением сроков послеоперационного восстановления, а также повышением качества жизни пациентов.
Цель исследования. Определить функциональное состояние детрузора до и после трансвезикальной аденомэктомии у пациентов с ГПЖ крупных и гигантских размеров.
Материалы и методы. В основу данного ретроспективного исследования включены результаты лечения 36 пациентов, которым была выполнена лапароскопическая трансвезикальная аденомэктомия по поводу ГПЖ. Критерии включения пациентов в исследование: объём предстательной железы свыше 80 см3; показатель максимальной скорости потока мочи ниже 15 мл/с; отсутствие инфекции нижних мочевых путей, нейрогенных расстройств мочеиспускания и трансуретральных оперативных вмешательств в анамнезе. Всем исследуемым пациентам выполняли цистометрию (наполнения и опорожнения) непосредственно до операции и через 3 – 6 месяцев после.
Результаты. Средний возраст больных составил 65,8 ± 4,21 года. Средний объём предстательной железы был равен 148,5 ± 17,9 см3, среднее значение суммарного балла симптоматики заболевания по шкале IPSS перед началом лечения — 19,4 ± 2,3 балла. Максимальная скорость потока мочи колебалась от 3,2 до 11,3 мл/с и в среднем составила 6,2 ± 1,6 мл/с. В раннем послеоперационном периоде ни у одного из исследуемых пациентов не отмечено осложнений тяжелее I степени по классификации Clavien-Dindo. После операции было отмечено статистически значимое снижение показателя детрузорного давления с 20,29 (± 2,9) до 11,24 (± 2,9) см вод. ст., а также увеличение максимальной скорости потока мочи с 6,24 (± 1,61) до 25,1 (± 5,05) мл/с.
Заключение. Лапароскопическая трансвезикальная аденомэктомия является эффективным и безопасным методом хирургического лечения ГПЖ как с позиции общих осложнений, так и с позиции функциональных расстройств детрузора при крупных и гигантских размерах предстательной железы.
Ключевые слова
Для цитирования:
Панферов А.С., Гаджиев Н.К., Ястребов В.С. Функциональное состояние детрузора при гиперплазии предстательной железы крупных и гигантских размеров до и после лапароскопической трансвезикальной аденомэктомии. Вестник урологии. 2025;13(4):31-38. https://doi.org/10.21886/2308-6424-2025-13-4-31-38
For citation:
Panferov A.S., Gadzhiev N.K., Yastrebov V.S. Evaluation of detrusor function in patients with large and giant benign prostatic hyperplasia pre- and post-laparoscopic transvesical adenomectomy. Urology Herald. 2025;13(4):31-38. (In Russ.) https://doi.org/10.21886/2308-6424-2025-13-4-31-38
Введение
Гиперплазия предстательной железы (ГПЖ) — полиэтиологическое заболевание, возникающее вследствие разрастания периуретральной железистой зоны предстательной железы, приводящее к обструкции нижних мочевыводящих путей и нарушению мочеиспускания [1 – 3]. В зависимости от объёма ГПЖ классифицируется следующим образом: < 25 см³ считается малой; 26 — 80 см³ — средней; > 80 см³ — крупной, > 250 см³ — гигантской [4]. Однако на сегодняшний день в мировой литературе не существует единого понятия и чёткой классификации о гигантском размере ГПЖ [5 – 7]. Согласно Российским клиническим рекомендациям, при малом объёме предстательной железы (менее 30 см³) рекомендуется выполнение трансуретральной инцизии простаты, при объёме простаты от 30 до 80 см³ — выполнение трансуретральной резекции или энуклеации предстательной железы, а у пациентов с объёмом простаты более 80 см³ следует выполнять трансуретральную энуклеацию предстательной железы [8]. Лапароскопические, робот-ассистированные и открытые операции рассматриваются как альтернативные методы лечения. Остаётся дискутабельным выбор метода хирургического лечения ГПЖ объёмом от 100 до 250 см³ и более. В настоящее время активно развиваются различные методы энергии, разрабатываются инструменты малого диаметра для энуклеативных методик с целью снижения рисков травматизации уретры. Несмотря на это, лапароскопическая аденомэктомия не теряет своей актуальности и все чаще становится методом выбора при лечении ГПЖ, превышающей объём 100 см³ [9]. Данный метод отличается эффективной коррекцией инфравезикальной обструкции (ИВО), низкой частотой геморрагических осложнений и инконтиненции, не превышая стандартных сроков послеоперационного восстановления [10]. Лапароскопический доступ также позволяет выполнять симультанные и сочетанные операции без отрицательного влияния на послеоперационную реабилитацию пациента.
Выделяют две основные лапароскопические техники: транскапсулярная (по Millin) (рис. 1) и трансвезикальная (по Freyer) (рис. 2) [11]. Оппоненты трансвезикального метода апеллируют к возможным нарушениям функции мочевого пузыря. В связи с чем нами принято решение о проведении исследования, включающего анализ данных пациентов, которым было проведено комплексное уродинамическое исследование (КУДИ) до и после оперативного вмешательства.
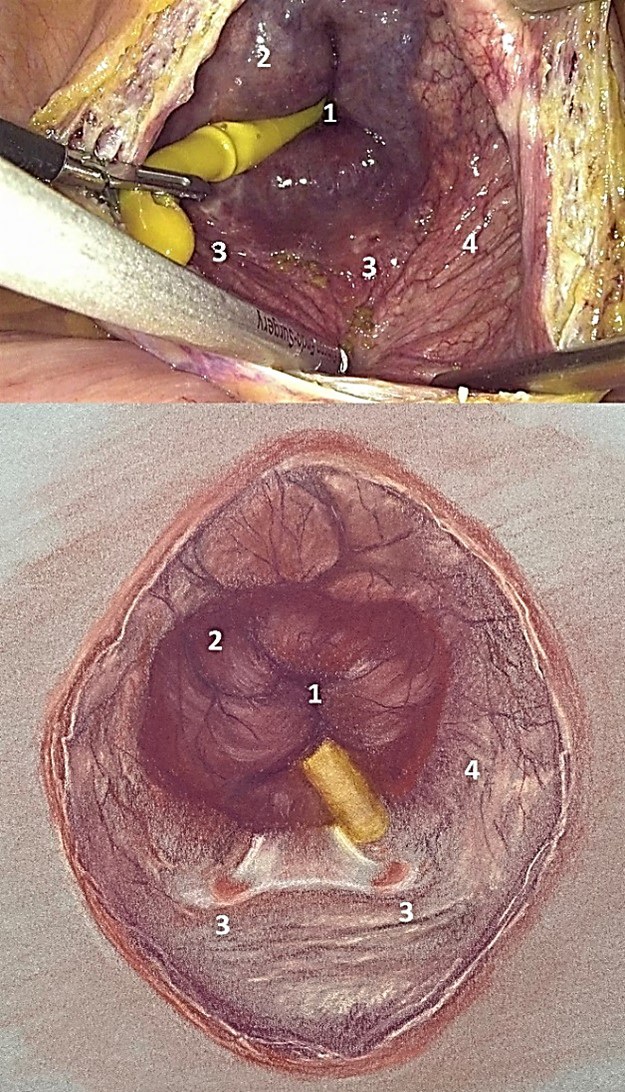
Рисунок 1. Цистотомия при лапароскопической трансвезикальной аденомэктомии: 1 — внутреннее отверстие уретры; 2 — интрапузырная протрузия гиперплазированных долей; 3 — устья мочеточников; 4 — слизистая мочевого пузыря
Figure 1. Cystotomy in laparoscopic transvesical adenomectomy: 1 — internal urethral orifice; 2 — intravesical protrusion of prostatic hyperplasia; 3 — ureteral orifices; 4 — bladder mucosa
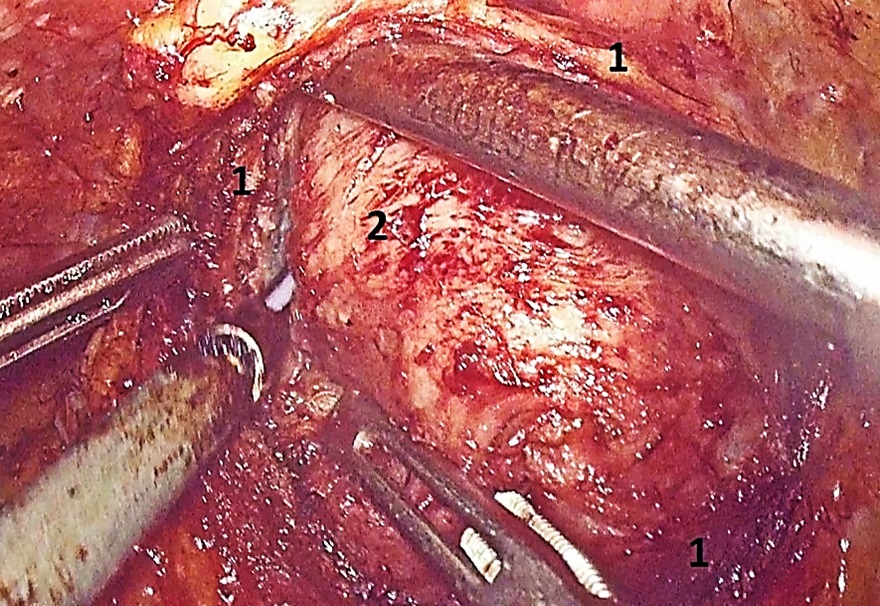
Рисунок 2. Энуклеация гиперплазированной ткани в апикальной области транскапсулярным доступом: 1 — хирургическая капсула простаты, 2 — гиперплазированная ткань
Figure 2. The apical enucleation of hyperplastic tissue via transcapsular approach: 1 — surgical capsule of the prostate, 2 — hyperplasic tissue
Цель исследования: определить функциональное состояние детрузора при лапароскопической трансвезикальной аденомэктомии у пациентов с ГПЖ крупных и гигантских размеров.
Материалы и методы
В основу данного ретроспективного исследования включены результаты лечения 36 пациентов, находившихся на стационарном лечении в клинике МЦ «Медассист» г. Курска с сентября 2023 по октябрь 2024 года, которым была выполнена лапароскопическая трансвезикальная аденомэктомия по поводу ГПЖ.
Критерии включения пациентов в исследование:
1) объём предстательной железы > 80 см³;
2) максимальная скорость потока мочи (Q max) < 15 мл/с;
3) отсутствие инфекции нижних мочевых путей;
4) отсутствие нейрогенных расстройств мочеиспускания в анамнезе;
5) отсутствие трансуретральных оперативных вмешательств в анамнезе.
Всем пациентам выполняли цистометрию наполнения и опорожнения («давление/поток») непосредственно до операции и через 3 – 6 месяцев после операции на уродинамической установке Dynamic UFM (“Medetron s.r.o.”, Zlín, Czech Republic). Терминология, оборудование и методы проведения уродинамических исследований, используемые в нашей работе, соответствовали рекомендациям Международного общества по проблемам недержания мочи (ICS) [12][13]. Интерпретацию результатов микционной цистометрии для определения ИВО и сократимости детрузора проводили по методике W. Shafer (1990) с использованием предложенной автором номограммы [14].
Хирургическая техника. Под многокомпонентной анестезией на 2 см выше пупка устанавливали оптический троакар 10 мм. Накладывали карбоксиперитонеум с давлением 12 мм рт. ст. Пациента переводили в положение Trendeleburg. В левой паховой области устанавливали два рабочих троакара 10 и 5 мм. В правой паховой области устанавливали два троакара 5 мм. Выполняли вертикальную цистотомию длиной до 10 см, визуализировали пролабирующие в просвет мочевого пузыря узлы гиперплазии (рис. 3). Слизистую над гиперплазированными долями надсекали при помощи УЗ-диссектора Harmonic® (“Ethicon”, Johnson & Johnson, Cincinnati, OH, USA). Далее выполняли энуклеацию узлов до апикальной части в хирургическом слое. Слизистую шейки мочевого пузыря и уретры ушивали циркулярно непрерывным швом, нитью Stratofix 3/0 (1/2 игла). Трансуретрально проводили 3-ходовой уретральный катетер Foley 20 Сh. Баллон при этом наполняли не более чем на 40 мл и оставляли в полости мочевого пузыря. Рану мочевого пузыря ушивали непрерывно нитью Stratofix 3/0 (1/2 игла). Препарат погружали в лапароскопический мешок и удаляли через доступ для оптического троакара. Устанавливали дренаж в пространство малого таза. Троакары поочередно удаляли с контролем гемостаза. Материал направляли на гистологическое исследование.
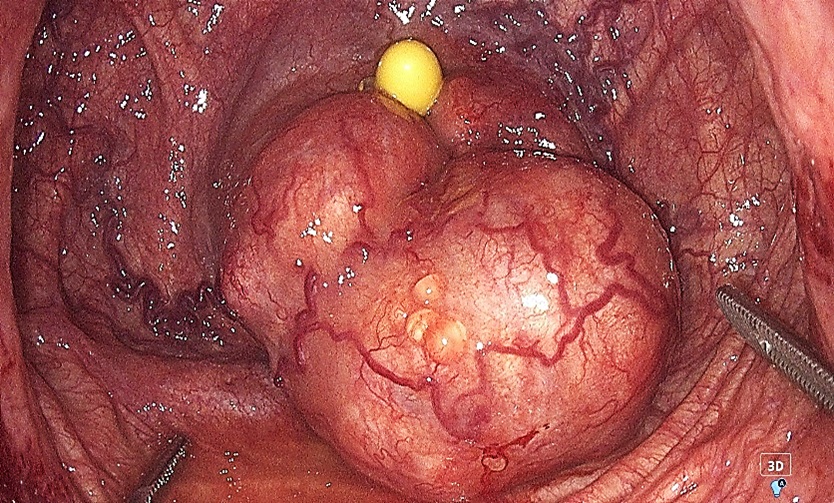
Рисунок 3. Визуализация гиперплазированной ткани через трансвезикальный доступ
Figure 3. Visualisation of hyperplastic tissue through the transvesical approach
Статистический анализ. Статистическую обработку данных производили с использованием прикладного программного обеспечения Microsoft Office Excel 365 (“Microsoft Corp.”, Redmond, WA, USA) и IBM SPSS Statistics v26.0 (SPSS: An IBM Company, IBM SPSS Corp., Armonk, NY, USA). Для проверки распределения количественных показателей на нормальность применяли критерий Shapiro-Wilk. Гипотеза о соответствии распределения нормальному была принята во всех случаях. Количественные показатели описывали средним значением и стандартным отклонением в формате — M ± SD. Качественные признаки (n) представлены в виде долей и частот выявления признака (%).
Анализ динамики показателей для сравнения двух периодов осуществляли на основе непараметрического теста Wilcoxon. Уровень значимости при проверке статистических гипотез был зафиксирован на уровне p < 0,05.
Результаты
Средний возраст больных составил 65,8 ± 4,21 года. Средний объём предстательной железы составил 148,5 ± 17,9 см³. Среднее значение суммарного балла симптоматики заболевания по шкале IPSS перед началом лечения составило 19,4 ± 2,3 балла. Максимальная скорость потока мочи колебалась от 3,2 до 11,3 мл/с и в среднем была равна 6,2 ± 1,6 мл/с.
В раннем послеоперационном периоде ни у одного из исследуемых пациентов не отмечено осложнений тяжелее Clavien-Dindo I (требовалось внутривенное введение анальгетиков). Характеристика результатов оперативного лечения представлена в таблице 1.
Таблица 1. Характеристика результатов оперативного лечения
Table 1. Surgical treatment outcomes overview
Характеристика операций } Characteristics of operations | Результаты | Results | |
Количество пациентов, n | Patinets, n | 36 | |
Продолжительность, мин. | Surgery time, min | 115,00 ± 38,12 | |
Кровопотеря, мл | Blood loss, mL | 124,34 ± 57,39 | |
Осложнения по Clavien-Dindo* Complications by Clavien-Dindo* | I | II – V |
32 (88,9) | 0 | |
Требовалось внутривенное введение анальгетиков Intravenous analgesia | ||
Сроки дренирования мочевого пузыря, дни | Timing of bladder drainage, days | 9,58 ± 1,49 | |
Койко-день, дни | Hospital stay, days | 5,09 ± 1,36 | |
Примечание. * — количество пациентов, n (%)
Note. * — number of patients, n (%)
По данным КУДИ (рис. 4), после операции было отмечено статистически значимое снижение показателя детрузорного давления (Pdet): с 20,29 (± 2,9) до 11,24 (± 2,9) см вод. ст. (p < 0,0001), а также увеличение Qmax: с 6,24 (± 1,61) мл/с до 25,1 (± 5,05) мл/с (p < 0,0001). Результаты функциональных исследований мочевого пузыря представлены в таблице 2.
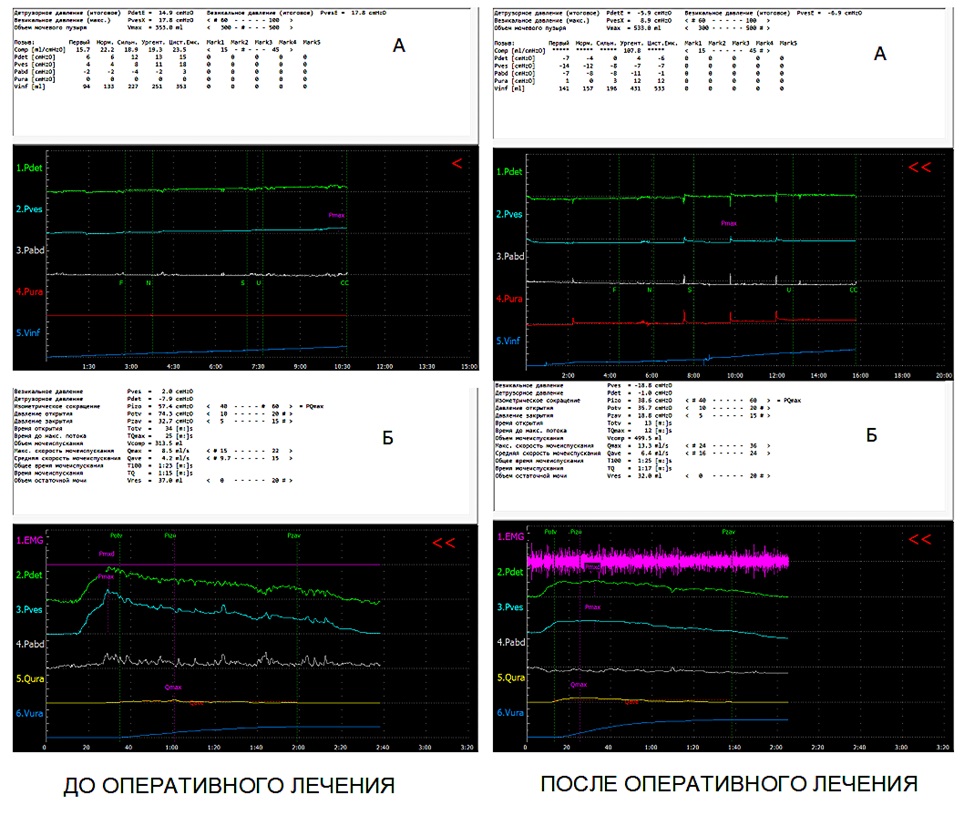
Рисунок 4. Цистометрия наполнения (А) и опорожнения (В) до и после оперативного лечения
Figure 4. Pre- and post-operative filling (A) and emptying (B) cystometry
Таблица 2. Результаты оценки функционального состояния детрузора
Table 2. Results of detrusor functional assessment
Критерии сравнения Comparison criteria | До операции Pre-op | После операции Post-op | P |
Детрузорное давление, см вод. ст. Detrusor pressure (Pdet), сm H20 | 20,3 (± 2,93) | 11,24 (± 2,95) | < 0,001 |
Детрузорное давление при Qmax, см вод. ст Pdet@Qmax, сm H20 | 54,19 (± 8,32) | 33,64 (± 9,92) | < 0,001 |
Цистометрическая ёмкость, мл MCC, mL | 415 (± 34,2) | 437,06 (± 76,26) | < 0,001 |
Qmax, мл/с Qmax, ml/s | 6,2 (± 1,61) | 25,12 (± 2,05) | < 0,001 |
Объём остаточной мочи, мл PVR, ml | 95,11 (± 52,49) | 19,46 (± 12,54) | < 0,001 |
Индекс инфравезикальной обструкции (индекс Абрамса-Гриффитса) BOO index (The Abrams-Griffiths index) | 41,70 (± 7,83) | -16,6 (± 14,07) | < 0,001 |
Примечание. Q max — максимальная скорость потока мочи
Note. Qmax — maximum urine flow rate; PVR — post voiding residual volume; BOO — bladder outlet obstruction, MCC — maximum cystometric capacity
Обсуждение
На сегодняшний день основными методами выбора лечения крупной и гигантской ГПЖ являются трансуретральная энуклеация, открытая или лапароскопическая / робот-ассистированная аденомэктомия [8]. Учитывая, что трансуретральные операции требуют большего количества времени, неизменно приводя к более длительному воздействию на уретру, что может способствовать более высокому проценту осложнений и инконтиненции [15], лапароскопические методы являются более предпочтительным вариантом при крупных и гигантских объёмах предстательной железы, так как при выполнении данных методик воздействие на уретру исключено. Из возможных вариантов исполнения лапароскопической аденомэктомии выделяют два основных: транскапсулярный и трансвезикальный, при этом последний вызывает критику у ряда урологов по причине широкой вертикальной цистотомии и, как следствие, развития возможных функциональных расстройств.
В нашем исследовании оценка работы мочевого пузыря производилась по результатам КУДИ до и после оперативного вмешательства (через 3 – 6 месяцев), так как при использовании для диагностики ИВО у больных с ГПЖ только стандартной урофлоуметрии высока частота как ложноотрицательных (12,6%), так и ложноположительных (18,1%) результатов [16].
Анализ наших результатов лапароскопической трансвезикальной аденомэктомии показал, что все 36 (100%) пациентов отмечали значительное улучшение своего состояния. У 4 (11,1%) из них после операции отмечалось сохранение расстройств мочеиспускания в виде императивных позывов, потребовавших коррекции М-холинолитиками (Солифенацин 10 мг), на протяжении 1 – 3 месяцев. По данным анализа КУДИ до и после операции, показатель Pdet достоверно снизился почти в два раза после операции, значимо увеличилась максимальная цистометрическая ёмкость и почти в 4 раза после операции увеличилась Qmax. У всех исследуемых пациентов в исследовании был проведён анализ данных показателя «давление/поток» с использованием индекса ИВО, также известным как индекс Abrams-Griffiths, рассчитываемый по формуле: Pdet@Qmax – 2*Qmax (норма менее 15). ИИО больше 40 был выявлен у 26 (72,2%) наблюдаемых нами больных, что свидетельствовало о наличии у них ИВО; у 10 (27,8%) больных значения ИВО оказались в интервале от 20 до 40, что говорит нам о «сомнительной обструкции». ИВО < 20 не был отмечен ни у одного из исследуемых.
Э.А. Зубков и М.Э. Ситдыкова (2011) в своей работе утверждают, что надлобковая чреспузырная аденомэктомия обеспечивает раннее восстановление мочеиспускания по уретре. По достижении двух недель у больных увеличивается объём мочеиспускания, возрастает максимальный и средний показатель объёмной скорости, сокращается время мочеиспускания, средняя объёмная скорость таких пациентов в среднем достигает 15,48 ± 2,7 мл/с [17]. А.В. Кнутов (2017) один из первых в отечественной литературе описывает преимущества лапароскопической трансвезикальной аденомэктомии, отмечая высокую эффективность и безопасность метода. В сравнении с позадилонным вариантом оперативного лечения автор отмечает возможность реконструкции шейки мочевого пузыря, выполнение симультанных вмешательств (дивертикулэктомия, цистолитотомия), обеспечение качественного, контролируемого гемостаза, а также отсутствие необходимости мобилизации мочевого пузыря. К относительным недостаткам можно отнести цистотомический разрез и работу в брюшной полости [18]
Р.Э. Амдий с соавт. (2012), оценивая результаты лечения ГПЖ у пациентов с СНМП, пришли к выводу, что у подавляющего большинства больных сохранение дизурии после оперативного лечения ГПЖ обусловлено гиперактивностью и/или снижением сократимости детрузора. Для установления причины нарушений мочеиспускания после оперативного лечения по поводу ГПЖ всем таким больным показано КУДИ, включающее в себя водную и микционную цистометрию, измерение профиля уретрального давления [19][20].
Более того, лапароскопическая трансвезикальная аденомэктомия обладает целым рядом преимуществ, среди которых:
– хорошая визуализация операционного поля;
– возможность симультанного лечения;
– панорамный контроль гемостаза по ходу операции;
– возможность везикализации шейки мочевого пузыря;
– низкая частота обструктивных осложнений и инконтиненции;
– возможность сохранения анатомической целостности пространства Retzius.
В то же время цистотомия, как один из этапов хирургического пособия, как показало наше исследование, не влечет за собой функциональных расстройств мочеиспускания.
Ограничения исследования. Данная работа включает всего 36 пациентов, оперированных в рамках одной клинической базы. Для большей статистической достоверности планируется продолжение исследования в этом направлении, расширение когорты пациентов. Кроме того, отбор пациентов производили без учёта коморбидной патологии, следовательно, результаты не могут быть применены ко всем пациентам с ГПЖ. Сравнивали только показатели, полученные при проведении цистометрии (наполнения, исследования «давление/поток»), а оценку результатов производили по прошествии ограниченного временного отрезка (3 – 6 месяцев), что также требует дальнейшего наблюдения.
Заключение
Лапароскопическая трансвезикальная аденомэктомия является эффективным и безопасным методом хирургического лечения ГПЖ крупных и гигантских размеров как с позиции общих осложнений, так и с позиции функциональных расстройств детрузора.
Список литературы
1. Jacobsen S.J., Girman C.J., Lieber M.M. Natural history of benign prostatic hyperplasia. Urology. 2001;58(6 Suppl 1):5-16; discussion 16. DOI: 10.1016/s0090-4295(01)01298-5
2. Пушкарь Д.Ю., Раснер П.И. Симптомы нижних мочевыводящих путей и доброкачественная гиперплазия предстательной железы. Урология. 2017;(прил. 3):4-18.
3. Emberton M., Fitzpatrick J.M., Garcia-Losa M., Qizilbash N., Djavan B. Progression of benign prostatic hyperplasia: systematic review of the placebo arms of clinical trials. BJU Int. 2008;102(8):981-986. DOI: 10.1111/j.1464-410X.2008.07717.x
4. Аляев Ю.Г., Глыбочко П.В., Пушкарь Д.Ю. Урология. Российские клинические рекомендации. М.: Медфорум; 2017.
5. Learney R.M., Malde S., Downes M., Shrotri N. Successful minimallyinvasive management of a case of giant prostatic hypertrophy associated with recurrent nephrogenic adenoma of the prostate. BMC Urol. 2013;13:18. DOI: 10.1186/1471-2490-13-18
6. Anglickis M., Platkevičius G., Stulpinas R., Miklyčiūtė L., Anglickienė G., Keina V., Štarolis E., Gradauskas A. Giant prostatic hyperplasia and its causes. Acta Med Litu. 2019;26(4):237-243. DOI: 10.6001/actamedica.v26i4.4209
7. Brockway W.J., Navetta A., Soni P., El Tayeb M.M. Two Cases of Spindle Cell Neoplasms in Patients Undergoing Holmium Laser Enucleation of the Prostate. J Endourol Case Rep. 2019;5(4):174-177. DOI: 10.1089/cren.2019.0048
8. Клинические рекомендации «Доброкачественная гиперплазия предстательной железы» (утверждены Минздравом России). 2024. Ссылка активна на 10.12.2024.
9. Lucca I., Shariat S.F., Hofbauer S.L., Klatte T. Outcomes of minimally invasive simple prostatectomy for benign prostatic hyperplasia: a systematic review and meta-analysis. World J Urol. 2015;33(4):563-570. DOI: 10.1007/s00345-014-1324-3
10. Панферов А.С., Котов С.В., Юсуфов А.Г., Елагин В.В., Бекреев Е.А., Бадаква Г.В., Семенов А.П. Лапароскопическая трансвезикальная аденомэктомия при крупных и гигантских размерах предстательной железы. Экспериментальная и клиническая урология. 2022;15(1):102-110.
11. Избранные лекции по урологии. Под ред. Мартова А.Г. М.: Мегаполис; 2024.
12. Abrams P., Cardozo L., Fall M., Griffiths D., Rosier P., Ulmsten U., Van Kerrebroeck P., Victor A., Wein A. Standardisation Sub-Committee of the International Continence Society. The standardisation of terminology in lower urinary tract function: report from the standardisation sub-committee of the International Continence Society. Urology. 2003;61(1):37-49. DOI: 10.1016/s0090-4295(02)02243-4
13. Schäfer W., Abrams P., Liao L., Mattiasson A., Pesce F., Spangberg A., Sterling A.M., Zinner N.R., van Kerrebroeck P. International Continence Society. Good urodynamic practices: uroflowmetry, filling cystometry, and pressure-flow studies. Neurourol Urodyn. 2002;21(3):261-274. DOI: 10.1002/nau.10066
14. Schäfer W. Principles and clinical application of advanced urodynamic analysis of voiding function. Urol Clin North Am. 1990;17(3):553-566. PMID: 1695782
15. Мартов А.Г., Ергаков Д.В., Турин Д.Е., Андронов А.С. Отдаленные результаты эндоскопической энуклеации доброкачественной гиперплазии предстательной железы больших размеров. Вестник Башкирского государственного медицинского университета. 2019;5:165-172.
16. Невирович Е.С. Значение комбинированного уродинамического исследования у больных доброкачественной гиперплазией предстательной железы: автореферат дис. … к.м.н. Санкт-Петербург; 2004. Ссылка активна на 10.12.2024.
17. Зубков Э.А., Ситдыкова М.Э. Состояние уродинамики после одномоментной и двухэтапной аденомэктомии с глухим швом мочевого пузыря. Медицинский вестник Башкортостана. 2011;6(2):76-78.
18. Кнутов А.В. Лапароскопическая чреспузырная аденомэктомия с тригонизацией 3600. Первые впечатления. Оригинальные исследования. 2017;7(4):14-21.
19. Аль-Шукри С.Х., Гиоргобиани Т.Г., Амдий Р.Э. Расстройства мочеиспускания после оперативного лечения доброкачественной гиперплазии предстательной железы. Нефрология. 2012;16(4):88-93.
20. Амдий Р.Э., Гиоргобиани Т.Г. Диагностика нарушений функции нижних мочевых путей у больных с неудовлетворительными результатами оперативного лечения доброкачественной гиперплазии предстательной железы. Урологические ведомости. 2012;2(2):32-37.
Об авторах
А. С. ПанферовРоссия
Александр Сергеевич Панферов – канд. мед. наук
Курск
Н. К. Гаджиев
Россия
Нариман Казиханович Гаджиев – д-р мед. наук
Санкт-Петербург
В. С. Ястребов
Россия
Виталий Сергеевич Ястребов
Курск
Рецензия
Для цитирования:
Панферов А.С., Гаджиев Н.К., Ястребов В.С. Функциональное состояние детрузора при гиперплазии предстательной железы крупных и гигантских размеров до и после лапароскопической трансвезикальной аденомэктомии. Вестник урологии. 2025;13(4):31-38. https://doi.org/10.21886/2308-6424-2025-13-4-31-38
For citation:
Panferov A.S., Gadzhiev N.K., Yastrebov V.S. Evaluation of detrusor function in patients with large and giant benign prostatic hyperplasia pre- and post-laparoscopic transvesical adenomectomy. Urology Herald. 2025;13(4):31-38. (In Russ.) https://doi.org/10.21886/2308-6424-2025-13-4-31-38













































