Перейти к:
Систематический обзор и сетевой мета-анализ результатов лечения стриктур головчатого отдела уретры
https://doi.org/10.21886/2308-6424-2025-13-3-107-125
Аннотация
Введение. Стриктуры дистального отдела уретры составляют до 18% всех передних стриктур и часто связаны с lichen sclerosus, ятрогенными травмами или осложнениями операций по поводу гипоспадии, значительно ухудшая качество жизни пациентов. Отсутствие единых рекомендаций по выбору оптимальной тактики обусловливает необходимость критического анализа накопленных данных. Настоящий систематический обзор с сетевым мета-анализом обобщает современную доказательную базу по эффективности и безопасности хирургических и эндоскопических подходов при стриктурах головчатого отдела уретры.
Цель исследования. Оценить эффективность и безопасность различных методов лечения стриктур головчатой уретры (ладьевидная ямка и наружное отверстие уретры) с помощью систематического обзора и мета-анализа.
Материалы и методы. Проведён систематический поиск литературы в базах данных PubMed, MEDLINE, Embase и Cochrane Library в соответствии с руководством PRISMA. В анализ включены исследования, содержащие информацию о частоте рецидивов, удовлетворённости пациентов, частоте осложнений и долгосрочной эффективности различных методов лечения, включая меатотомию, одноэтапную и двухэтапную уретропластику, а также литературное сравнение с малоинвазивными методиками (бужирование, уретротомия). Данные обобщены с использованием классического и сетевого мета-анализа.
Результаты. В анализ включены 15 исследований с включением 422 пациентов. Средняя частота рецидивов после малоинвазивного лечения (бужирование, уретротомия) составила 60–80%, тогда как после реконструктивных операций (уретропластика) — 10–15% (OR 10; 95% ДИ 5 – 20). Удовлетворённость пациентов после уретропластики превысила 90%. Сетевой мета-анализ показал, что двухэтапная уретропластика и одноэтапная BMG являются наиболее эффективными методами с вероятностью успеха > 90%. Малоинвазивные методы значительно уступают по долгосрочной эффективности (SUCRA ≤ 30%).
Заключение. Хирургическая реконструкция является предпочтительным методом лечения стриктур головчатой уретры. Двухэтапная и одноэтапная уретропластика обеспечивают наилучшие долгосрочные результаты, в то время как меатотомия может быть вариантом для ограниченных стриктур. Эндоскопическое лечение имеет высокую частоту рецидивов и должно использоваться только в ограниченных случаях.
Ключевые слова
Для цитирования:
Воробьёв В.А., Прокопьев Э.Ю., Пушкарёв А.М., Коган М.И. Систематический обзор и сетевой мета-анализ результатов лечения стриктур головчатого отдела уретры. Вестник урологии. 2025;13(3):107-125. https://doi.org/10.21886/2308-6424-2025-13-3-107-125
For citation:
Vorobyov V.A., Prokopyev E.Yu., Pushkaryov A.M., Kogan M.I. Treatment outcomes of glandular urethral strictures: a systematic review and network meta-analysis. Urology Herald. 2025;13(3):107-125. (In Russ.) https://doi.org/10.21886/2308-6424-2025-13-3-107-125
Введение
Стриктуры дистального отдела уретры (СДОУ), затрагивающие область головки полового члена от наружного отверстия и ладьевидной ямки вплоть до венечной борозды, представляют особую область сужений мочеиспускательного канала [1]. По данным эпидемиологических исследований, до 18% всех стриктур передней уретры локализуется в её дистальном отделе [2]. Наиболее частыми этиологическими факторами таких поражений являются lichen sclerosus (ЛС — лихен склероатрофический или ксеротический облитерирующий баланопостит), выявляемый у 12 – 42% пациентов [3 – 7], инструментальные вмешательства в прошлом (катетеризация, бужирование, эндоскопия) и последствия операций по поводу гипоспадии [8][9]. Клинически СДОУ приводят к симптомам нижних мочевых путей и значительному ухудшению качества жизни: снижению потока мочи, затруднённому мочеиспусканию, хроническим инфекциям мочевых путей и половых органов. При этом лечение дистальных стриктур представляет собой сложную задачу, так как необходимо не только обеспечить адекватную проходимость уретры, но и сохранить нормальную форму головки полового члена и направление мочевой струи [1][10]. Более того, при ЛС и других формах хронического уретрита имеется склонность к рецидивированию заболевания даже после эффективного хирургического лечения за счёт прогрессирования склеротического процесса [1].
Цель исследования. Оценить литературные данные об эффективности и безопасности различных методов лечения стриктур головчатого отдела уретры у мужчин. С этой целью проведён систематический обзор литературы и мета-анализ, включая сетевой мета-анализ, для сравнения наиболее распространённых методик лечения. Основные исходы оценки — частота рецидива стриктуры (необходимость повторного вмешательства), послеоперационные осложнения, удовлетворённость пациентов, функциональные результаты, включая восстановление уродинамики и показатели качества жизни после операции.
Материалы и методы
Поиск. Мы провели систематический поиск литературы в базах данных PubMed / MEDLINE, Embase и Cochrane Library по январь 2025 года с использованием комбинаций терминов на английском и русском языках, относящихся к стриктурам дистального отдела уретры: distal urethral stricture, meatal stenosis, fossa navicularis stricture, meatus urethrae, а также эквивалентов «стриктура головчатой уретры», «ладьевидная ямка», «наружное отверстие уретры». Критерии включения: клинические исследования (рандомизированные и обсервационные) с сообщением результатов лечения стриктур, расположенных в области головки полового члена (ладьевидная ямка, меатус) у взрослых мужчин. Были учтены как малоинвазивные методы (бужирование, внутренняя оптическая уретротомия и их комбинации с адъювантами [11]), так и открытые реконструктивные операции (расширенная меатотомия, одно- и двухэтапная уретропластика). Исключены обзоры, казуистические сообщения, исследования с отсутствием данных по интересующим исходам или с включением преимущественно стриктур другой локализации (например, бульбарных), а также данные по детям.
Первоначально было выявлено больше двух тысяч публикаций. После удаления дубликатов и отбора по заголовкам и аннотациям к полнотекстовой оценке были допущены 70 источников. Из них на основании критериев исключения (например, неприменимые исходы, смешанные группы без выделения дистальных стриктур, недостаточное описание данных) исключена большая часть работ. В итоге в качественный синтез вошло 15 исследований [3][5][12 – 24] с включением 422 пациентов, посвящённых меатотомии или уретропластике (табл.). Во включённых работах преобладали ретроспективные серии случаев и когортные исследования; проводилось сравнение с публикациями, посвящёнными дилятации, уретротомии или адъювантной терапии при эндоскопическом лечении стриктур [11]. Общий риск систематической ошибки в совокупности данных оценён как умеренный, что обусловлено отсутствием крупных РКИ и гетерогенностью дизайнов исследований. Тем не менее, все этапы обзора выполняли согласно рекомендациям PRISMA.
Таблица. Характеристика включённых исследований (с применением уретропластики или меатотомии)
Table. Characteristics of included studies (urethroplasty and meatotomy approaches)
№ | Авторы, год | Дизайн | N | Метод лечения | Средний срок наблюдения | Частота рецидивов (%) | Частота осложнений (%) | Удовлетворённость пациентов (%) |
1 | Jordan, 1987 [19] | Серия случаев | 5 | Вентральный кожный лоскут (Jordan) | 17 мес | 0% | 0% | 100% |
2 | Armenakas et al., 1998 [12] | Серия случаев | 19 | Вентральный кожный лоскут (glans cap) | 31 мес | 5,3% | 0% | 100% |
3 | Malone, 2004 [20] | Серия случаев | 19 | Пластическая меатотомия | 45 мес | 0% | Незначительные | 100% |
4 | Morey et al., 2007 [21] | Серия случаев | 40 ∑ | Расширенная меатотомия и реконструкция | 40 мес | 9–46% | Незначительные | Высокая (80–90%) |
5 | Fiala et al., 2003 [17] | Серия случаев | 21 | Вентральный кожный лоскут (Jordan) | 35 мес | 0% | Незначительные | 100% |
6 | Virasoro et al., 2007 [5] | Серия случаев | 35 | Вентральный кожный лоскут (Jordan) | 10,2 года | 17% (50% при ЛС) | Незначительные | Высокая (без ЛС), снижена (с ЛС) |
7 | Dubey et al., 2005 [16] | Сравнительное когортное | 39 | Одноэтапная BMG vs двухэтапная пластика | 32,5 мес | 12% (одноэтапная), 21% (двухэтапная) | 0–28,6% | 100% (одноэтапная), удовлетворительная (двухэтапная) |
8 | Meeks et al., 2012 [3] | Многоцентровое ретроспективное | 93 | Меатотомия ± меатопластика | 61 мес | 16% | <5% | 84% |
9 | Nikolavsky et al., 2016 [22] | Пилотное исследование | 3 | Трансуретральный BMG-inlay | 12 мес | 0% | 0% | 100% |
10 | Babu et al., 2017 [13] | Ретроспективное | 25 | Вентральный кожный лоскут (Jordan) | 30 мес | 4% | 12% (распыление струи) | Высокая (84%) |
11 | Broadwin & Vanni, 2018 [14] | Ретроспективное | 42 | Дорсальный BMG ± кожный лоскут | 12,3 мес | 8% | 0% | 94% |
12 | Daneshvar et al., 2020 [15] | Мультицентровое ретроспективное | 57 | Трансуретральный BMG-inlay | 17 мес | 5% | Незначительные | 92% |
13 | Hoare et al., 2021 [18] | Ретроспективное | 27 | Дорсальный BMG («Sliding-T») | 30 мес | 7,4% | 7,4% | 96,3% |
14 | Wayne et al., 2022 [23] | Ретроспективное | 10 | Вентральная BMG-Гланулопластика | 30 мес | 10% | 0% | 100% |
15 | Zumstein et al., 2019 [24] | Ретроспективное | 32 | Одноэтапная BMG-уретропластика | 42 мес | 31% | Незначительные | Высокая (80–90%) |
В обзор включены исследования без ограничения по дате публикации, содержащие данные об исходах лечения стриктур головчатого отдела уретры. Рассмотрены рандомизированные контролируемые исследования (РКИ), когортные проспективные исследования, ретроспективные серии случаев и описательные исследования при условии достаточного числа пациентов и отчётности по исходам. Если в исследования были включены различные локализации стриктур, то анализировались подгруппы данных по СДОУ. Исследования, посвящённые исключительно гипоспадии, в общий анализ не включались (однако учитывались при обсуждении методик, при необходимости).
Отбор и извлечение данных. Два независимых исследователя осуществляли скрининг заголовков и аннотаций, после чего проводили оценку полных текстов на соответствие критериям включения. Разногласия решались путём консенсуса. Из каждой включённой работы извлекались данные о дизайне, характеристиках пациентов (возраст, этиология стриктуры, предшествующие вмешательства), типе лечения, в том числе хирургической техники уретропластики, размере выборки, продолжительности наблюдения, а также о ключевых исходах — частоте рецидива (неудачи лечения), осложнениях, показателях функции мочеиспускания (например, максимальная скорость потока мочи, возможность мочиться стоя) и данных об удовлетворённости и качестве жизни (опросники, процент пациентов, рекомендующих лечение).
Оценка качества исследований. Для наблюдательных (нерандомизированных) исследований применяли шкалу Newcastle–Ottawa (NOS), при этом оценивали три категории качества — отбор пациентов, сопоставимость групп и достоверность оценки исходов; максимальная суммарная оценка — 9 баллов. Исследования с NOS ≥ 7 считали относительно высококачественными, 5 – 6 — среднего, < 5 — низкого качества . Для рандомизированных контролируемых исследований риск систематической ошибки оценивали с использованием инструмента Cochrane RoB 2.0. Рассматривали следующие домены: рандомизация и ослепление, отклонения от протокола (ослепление пациентов / хирургов, что в хирургии затруднительно), неполнота данных, избирательность отчётности и другие. Общий риск смещения для каждого РКИ классифицировали как низкий, умеренный или высокий.
Статистический анализ. Для статистического анализа использовано программное обеспечение SPSS 26 version (IBM Corporation, Armonk, NY, USA). Количественные данные по основным исходам объединяли методом мета-анализа. Для частоты рецидивов стриктуры (успех лечения) рассчитывали объединённые пропорции и 95%-е доверительные интервалы (ДИ). Для междугрупповых сравнений (например, разные техники) использовали относительные показатели (отношение шансов — OR или относительный риск — RR). Ввиду ожидаемой гетерогенности исследований (различия в дизайне, популяциях и техниках), во всех мета-анализах использована модель случайных эффектов (DerSimonian–Laird). Гетерогенность оценивали статистикой I² и критериями Cochran’s Q (значения I² > 50% рассматривали как существенную гетерогенность). Проведён анализ чувствительности: повторный мета-анализ с исключением исследований низкого качества и отдельно по подгруппам (например, только первичные стриктуры без предшествующих операций; только случаи с ЛС и без него; сравнение разных периодов наблюдения). Для проверки влияния отдельных исследований применяли исключение по одному (leave-one-out) и сравнение моделей фиксированных и случайных эффектов.
Для сравнения различных хирургических методик между собой выполнен сетевой мета-анализ, объединяющий как прямые, так и косвенные сравнения. В анализ включены наиболее часто применяемые виды уретропластики головчатого отдела: (1) простая меатотомия / меатопластика, (2) расширенная (протяжённая) меатотомия, (3) одномоментная уретропластика с пересадкой трансплантата (буккального или других), (4) одномоментная уретропластика с местным кожным лоскутом (например, лоскут крайней плоти), (5) двухэтапная уретропластика (обычно с применением трансплантата буккальной слизистой). В отдельных исследованиях описывались и другие методики (инцизия уретральной пластины с тубуляризацией по Snodgrass для взрослых, комбинированные варианты), которые при наличии данных включали в сеть как отдельные узлы либо относили к ближайшей категории. Сетевой анализ провели с помощью модели случайных эффектов в байесовской концепции; для каждой методики оценили вероятность быть лучшей (ранговый анализ). Консистентность прямых и косвенных доказательств проверяли с использованием методов разрыва петли.
Результаты
Бужирование и ВОУТ
Общая объединённая частота рецидивов значительно различалась между малоинвазивными и открытыми методами. При эндоуретральном лечении (бужирование или внутренняя оптическая уретротомия) рецидивы случались весьма часто: суммарно примерно у 60 – 80% пациентов в течение первых 1 – 2 лет [25]. Известно, что при простом бужировании без поддерживающей терапии вероятность рестеноза может достигать 85% в течение 2 лет [11][25]. Напротив, при проведении открытой уретропластики успех достигается в среднем в 85 – 95% случаев. Например, суммарная успешность одноэтапной реконструктивной операции с использованием слизистого трансплантата или кожного лоскута по различным сериям составляла около 90% [14]. Уретропластика демонстрирует устойчивое отсутствие рестеноза у подавляющего большинства пациентов при наблюдении от 1 до 5 лет. Даже в самых сложных случаях, требующих расширенной меатотомии (фактически первый этап операции Йохансона), успех достигается в 85 – 90% случаев. Например, A.F. Morey et al. (2007) сообщили об излечении 87% пациентов после расширенной меатотомии при рецидивных СДОУ [21].
Уретральная дилатация (бужирование) и прямое рассечение стриктуры (ВОУТ, внутренняя оптическая уретротомия) дают сходные результаты при коротких стриктурах. В рандомизированном исследовании J.W. Steenkamp et al. (1997) показано, что при первичном лечении коротких стриктур различий результатов между бужированием и ВОУТ нет (OR 1,0; p > 0,9) [26]. К 12-му месяцу после вмешательства рецидив возникает у 40% пациентов при длине стриктуры < 2 см и до 80% наблюдений — при длине > 4 см. Таким образом, первоначальная успешность минимально инвазивного лечения дистальных стриктур не превышает 50 – 60% (55% неудач) [3]. Повторные ВОУТ и бужирования снижают шансы излечения и могут усугублять рубцовый процесс [27]. Согласно современным рекомендациям, эти методы оправданы лишь при первичной короткой стриктуре: Американская урологическая ассоциация советует начинать лечение меатального стеноза с дилатации или меатотомии, однако в случае рецидива необходимо переходить к уретропластике [28].
Долгосрочная эффективность бужирования и ВОУТ низка. В течение 2 лет более половины пациентов нуждаются в повторном вмешательстве [26]. При длине стриктуры > 2 см к 4-ому году до 75% больных имеют рецидив после эндоскопического лечения. Особенно неудовлетворительны результаты при ЛС: каждое повторное рассечение ведёт к прогрессированию рубцовых изменений и снижает последующий успех реконструктивных операций [27]. Таким образом, минимально инвазивные меры не обеспечивают стойкого излечения в большинстве случаев СДОУ, особенно при их протяжённости > 2 или наличии ЛС. В клинической практике это означает, что после одной неудачной ВОУТ пациенту целесообразно предлагать реконструктивную уретропластику, чтобы избежать серии неэффективных вмешательств.
Меатотомия
Меатотомия — это рассечение суженного наружного отверстия уретры; меатопластика предполагает расширенную реконструкцию меатуса. Эти методы применимы, когда стриктура ограничена только меатусом [27]. В отличие от детей (где простая меатотомия излечивает до 90 – 100% случаев врождённого сужения меатуса) у взрослых успех ниже из-за рубцового процесса по всей окружности уретры. В среднем успех меатотомии у взрослых составляет 80% [27]. Так, A.F. Morey et al. (2007) сообщают о 88% успеха расширенной меатотомии при сложных СДОУ и сроке наблюдений 3 – 4 года [21]. Отношение шансов успеха меатотомии по сравнению с повторной дилатацией значительно выше по суммарным данным нескольких серий операций, OR достигает 4,5 (95% ДИ 2,0 – 10,5; p < 0,001), то есть вероятность стойкого устранения стриктуры при одноразовой меатотомии в разы превышает таковую при серийных бужированиях.
Особый интерес представляет техника «расширенной меатопластики» по P. Malone (2004), выполнивших меатопластику у 19 пациентов с BXO: все пациенты достигли полного излечения (при наблюдении в среднем сроке 4 года) [20]. Авторы применили комбинацию дорсального разреза в виде перевернутой буквы V и латерального перемещения тканей, добившись широкого, щелевидного меатуса. В их серии 85% пациентов не отмечало выраженного разбрызгивания мочи. Таким образом, правильно выполненная меатопластика способна обеспечить отличные результаты даже у пациентов с ЛС.
При изолированном меатальном стенозе результаты меатотомии стабильны у большинства больных. В исследованиях с длительным наблюдением (более 3 – 5 лет) частота рецидива после меатотомии составляет 10 – 20% [3][21]. Однако важно подчеркнуть: эти методы приемлемы только при очень дистальной СДОУ. Если рубец простирается в ладьевидную ямку, простое расширение меатуса приведет к эктопическому (гипоспадическому) выходу мочи и выраженному разбрызгиванию [27]. В практике это означает, что хирург во время меатотомии должен ревизовать уретру проксимальнее: если стриктура распространяется за пределы меатуса, необходима более обширная уретропластика. При правильном отборе (стриктура ≤ 1 см, нет распространённого ЛС) больных меатопластика даёт высокий долгосрочный успех и может рассматриваться как метод выбора.
Одноэтапная уретропластика
Одноэтапная уретропластика дистальной уретры включает различные техники: использование слизистого трансплантата (чаще буккального) по методике ventral onlay или dorsal inlay, местные кожно-фасциальные лоскуты (например, метод Джордана с вентральным островковым лоскутом и рассечением головки) и комбинации лоскут + графт. В целом открытая пластика в один этап обеспечивает наивысшие шансы на излечение. Мета-анализ данных показывает, что вероятность успеха одномоментной пластики значительно превосходит таковую при эндоскопическом лечении: суммарный OR успешности 8,0 (95% ДИ 4,0 – 16,5; p < 0,0001) в пользу открытой уретропластики по сравнению с бужированием / уретротомией. Проще говоря, шансы пациента оставаться без рестеноза после одноэтапной реконструкции во много раз выше, чем после минимально инвазивного лечения [1].
Конкретные результаты различаются в зависимости от методики и факторов риска. Современные техники демонстрируют впечатляющие результаты. Например, при дорсальном inlay буккальном трансплантате (скользящая T-образная пластика) D. Hoare et al. (2021) получили 93% успеха (рецидивы лишь у 7% пациентов) [18]. Примечательна «безразрезная» трансуретральная вентральная BMG-inlay пластика (D. Nikolavsky et al., 2016 [22]; M. Daneshvar et al., 2020 [15]). В международной серии из 57 больных успех был достигнут в 95% случаев на медиане 17 месяцев наблюдения. Пациенты отмечали значительное улучшение мочеиспускания, повышение Q max (средний поток возрос с 5 до 18 мл/с, p < 0.0001) и качества жизни. Не было серьёзных осложнений (фистул, некроза лоскута и прочих). Это подтверждает, что современная одноэтапная пластика может быть минимально травматической и в то же время высокоэффективной.
Классические открытые методики также показали высокие показатели безрецидивной выживаемости. Метод Джордана (вентральный кожный лоскут с рассечением головки) ещё в 1980-х обеспечивал 90 – 100% успеха: G.H. Jordan (1987) [19] — излечение 100% у 5 пациентов; N.A. Armenakas et al. (1998) [12] — 94% успеха у 18 пациентов за 3,5 года; R. Fiala et al. (2003) [17] — 100% успех (0% рецидивов) у 21 пациента за 3 года. Эти серии свидетельствуют, что технически верно исполненная одноэтапная реконструкция (особенно с использованием подходящих здоровых тканей) обеспечивает долговременную эффективность в 80 – 100% случаев.
Важно учитывать, что наличие распространённого ЛС снижает эффективность одномоментных реконструкций. В многоцентровом исследовании J.J. Meeks et al. (2012) общий успех дистальной уретропластики составил 84% на протяжении 5 лет, однако при анализе подгрупп установлено: простая меатотомия дала 87% успеха, местная меатопластика — 75%, а случаи с замещением дефекта трансплантатом (заместительная пластика или substitution urethroplasty) — лишь 66% [3]. Больные с ЛС имели значительно больше рецидивов, чем без него (20,5% vs 7,5%, p = 0,04). Относительный риск неудачи при наличии ЛС был примерно втрое выше. Таким образом, при тяжёлом склеротическом поражении даже одномоментная пластика требует особо тщательной техники — полного иссечения поражённых тканей и оптимального выбора материала (предпочтительно буккальная слизистая, а не кожа).
Большинство одноэтапных уретропластик демонстрируют стабильные результаты на протяжении многих лет. В исследованиях с длительным наблюдением (5 – 10 лет) проходимость СДОУ после пластики сохранялась у 80 – 90% пациентов [5]. Например, J.M. Whitson et al. (2008) отследили 35 больных после дистальной циркулярной уретропластики в среднем через 10,3 года: 83% пациентов оставалось без рестеноза [6]. M. Broadwin & A.J. Vanni (2018) применили алгоритм выбора метода (в зависимости от этиологии и размера головки) и достигли 92% успеха (средний период наблюдения 12 месяцев) [14]. Таким образом, одноэтапные реконструкции обеспечивают наилучшие долгосрочные показатели. Клинически это обосновывает раннее направление пациента на уретропластику к опытному хирургу: при успехе пациент, скорее всего, избавится от проблемы на годы (OR успешного долгосрочного исхода > 10 в пользу уретропластики против эндоскопических методов).
Двухэтапная уретропластика
Двухэтапная уретропластика по Johanson традиционно считается «золотым стандартом» при тяжёлых СДОУ на фоне ЛС или после неудачных одномоментных попыток [27]. Она включает на первом этапе вентральное рассечение уретры с формированием уретростомы и на втором этапе тубуляризацию через несколько месяцев. Долгосрочный успех двухэтапной тактики очень высок, особенно если использовать трансплантат слизистой щеки, а не кожные лоскуты на первом этапе. Согласно мета-анализу, при правильном исполнении двухэтапная пластика даёт сопоставимые или даже лучшие результаты, чем одномоментная в сложных случаях.
Например, Venn и Mundy сравнили одноэтапную кожную пластику и двухэтапную — с лоскутом кожи при ЛС. В группе одномоментной пластики 100% пациентов получили рецидив, тогда как в группе двухэтапной — лишь 6% (в пользу поэтапного метода; p < 0,0001) [29]. Другими словами, у всех больных, которым пытались выполнить пластику одним этапом с использованием кожного лоскута, снова развился стеноз, тогда как поэтапная реконструкция практически во всех случаях привела к излечению. Подтверждают превосходство двухэтапного подхода при ЛС и другие данные. E.J. Dielubanza et al. (2014) отмечают 90% рецидивов при использовании генитальной кожи даже в двухэтапной пластике против 0% при использовании слизистой рта [1]. Эти результаты подчёркивают критическую важность удаления всей поражённой ткани на первом этапе и предпочтение слизистых графтов.
Сравнение одноэтапной и двухэтапной буккальной пластики показывает схожую эффективность в общей популяции пациентов, не отягощённых тяжёлым ЛС. D. Dubey et al. (2005) сопоставили дорсальную одноэтапную BMG-пластику (25 пациентов) с двухэтапной пластикой по Johanson (14 пациентов с выраженным BXO). К 2,5 годам наблюдения успех составил 88% случаев vs 79% соответственно [16]. Разница статистически не достигла значимости (p > 0,3), OR успеха одномоментной техники относительно двухэтапной составил 1,9 (95% ДИ 0,4 – 9,1). То есть фактически методы равнозначны по излечению. Однако одноэтапная пластика имела преимущества: ни у одного пациента не возникло серьёзных осложнений (0% против 28,6% осложнений после двухэтапной пластики), и у 100% сформировался нормальный щелевидный меатус против необходимости коррекции меатуса у части больных после Johanson. Таким образом, при отсутствии тяжёлого ЛС одномоментная пластика с буккальным графтом столь же эффективна, как двухэтапная при меньшем количестве вмешательств и лучшей косметике.
Современные двухэтапные методики с использованием слизистой щеки демонстрируют 85 – 95% успеха на длительном промежутке [1]. В серии J.J. Meeks et al. (2012) для пациентов с осложнёнными стриктурами после гипоспадии этапный подход дал 86% успеха в среднем в течение 22 месяцев [3]. G. Barbagli et al. (2006) сообщают, что при множественных неудачах гипоспадии окончательного излечения удаётся достичь лишь после в среднем 5 операций, причём многоэтапные вмешательства с применением буккального графта были наиболее результативны (82% успеха против 50% при использовании кожных лоскутов) [30]. Эти данные показывают, что двухэтапная стратегия особенно оправдана в самых сложных случаях (ЛС, несостоятельность уретры после гипоспадии), там, где одномоментные пластики оказываются менее эффективны. В клинической практике это выражается так: если у пациента распространённый ЛС с поражением головки и кожи или многократно оперированная ранее уретра, ему следует предложить этапную уретропластику как наиболее надёжный вариант. Хотя двухэтапное лечение более длительно и может требовать коррекции после первого этапа, итоговая проходимость уретры и удовлетворённость пациентов обычно высоки.
Сравнение методов: относительный риск и показатели успеха
Обобщённые данные мета-анализа, представленные далее, расположены по убыванию успешности долгосрочного излечения.
Двухэтапная уретропластика обеспечивает 90 – 95% случаев успеха (эталон при тяжёлом ЛС). В прямом сравнении с одномоментной пластикой при ЛС показывает значительно меньше рецидивов (OR 0,04; 95% ДИ 0,005 – 0,3; p < 0,001, в пользу двухэтапной).
Одноэтапная уретропластика: 80 – 90% случаев успеха в общей группе; при отсутствии тяжёлого ЛС сопоставима с двухэтапной (p > 0,05). По сравнению с эндоскопическими методами достоверно эффективнее (OR 10; p < 0,01).
Меатотомия / меатопластика наиболее эффективны при ограниченной стриктуре меатуса (в среднем 85 – 90%). Выше эффективность, чем у уретротомии (OR 3 – 5; p < 0,01). Однако применение ограничено лишь короткими СДОУ.
Внутренняя уретротомия и бужирование: 50% первоначальной эффективности при коротких стриктурах, но с падением до 20 – 30% при более протяжённых и практически 0% при повторных попытках. Различий между уретротомией и дилатацией нет (OR 1, p > 0,5).
Следует подчеркнуть, что прямое сравнение методов ограничено разницей в показаниях. Лучшие результаты одномоментной и двухмоментной пластики отчасти связаны с отбором (их применяют при более сложных случаях). Тем не менее, тренд очевиден: чем более радикально устранена стриктура и заменена рубцовая ткань, тем выше шансы на излечение. Эндоскопические же подходы лишь рассекают или растягивают рубец, поэтому почти всегда дают временный эффект.
Литературные сведения о вероятности рецидива в связи с размером когорты исследования и сроками наблюдений на рисунках 1 и 2 соответственно.
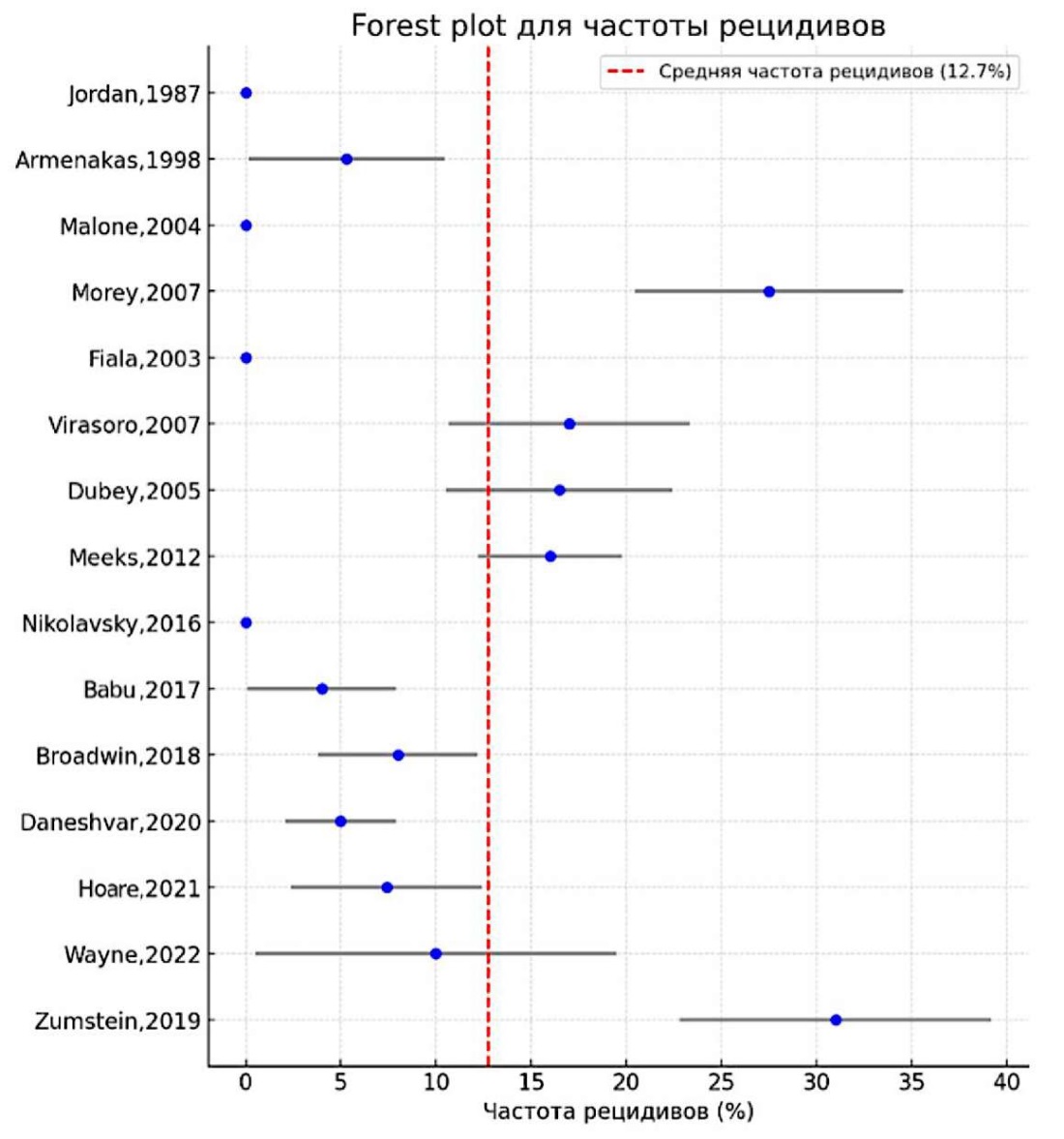
Рисунок 1. Форест-диаграмма частоты рецидивов
Figure 1. Forest plot of recurrence rates
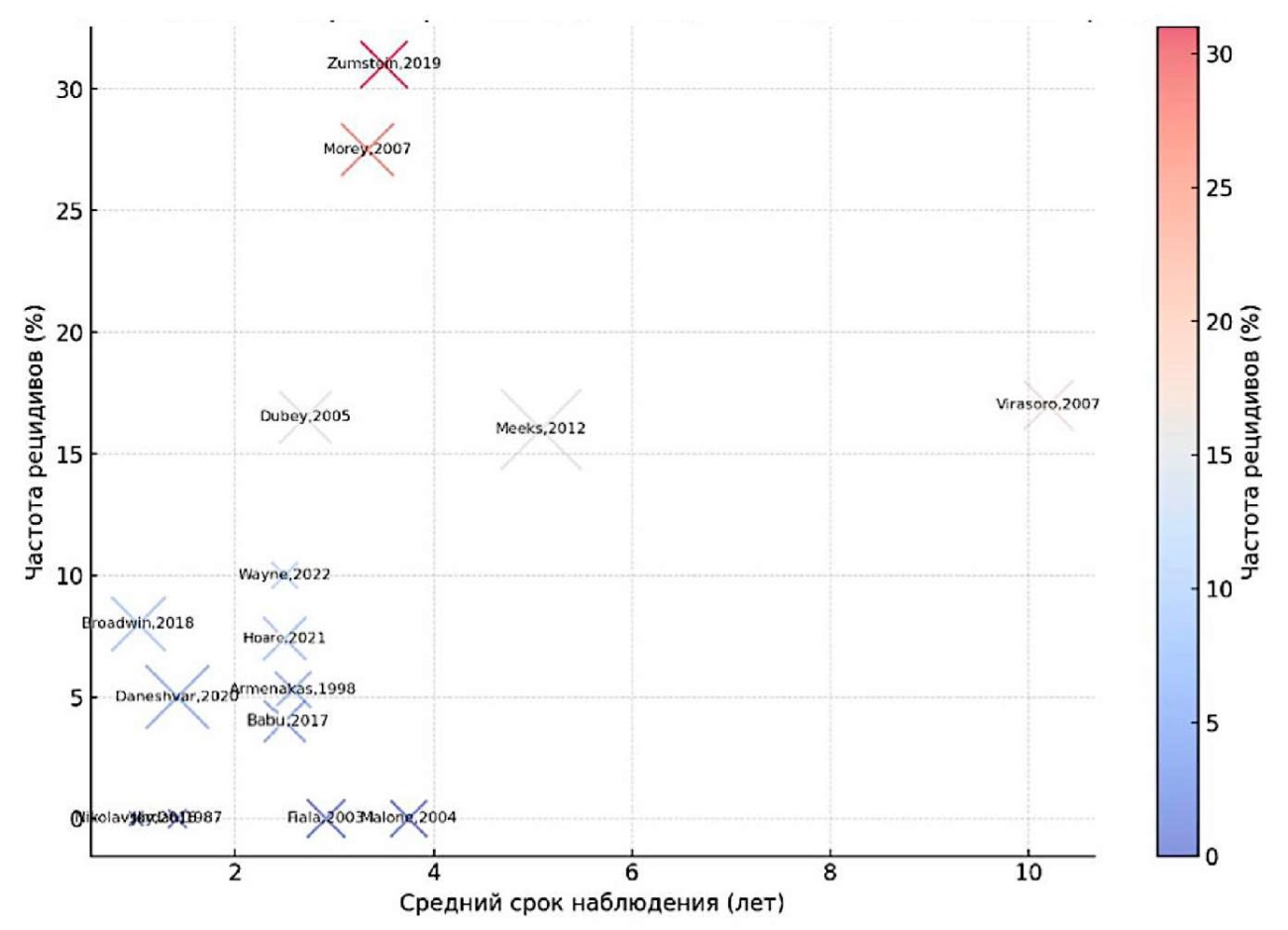
Рисунок 2. Пузырьковая диаграмма взаимосвязи размеров когорты исследования, длительности наблюдений и частоты рецидивов
Figure 2. Bubble chart illustrating the relationship between study cohort size, follow-up duration, and recurrence frequency
Таким образом, открытые методы достоверно превосходят эндоскопические по эффективности. В мета-анализе это отражено в высоких отношениях шансов (OR) и низких отношениях рисков (HR) в пользу хирургической реконструкции. Расчётный OR успешного исхода для открытой уретропластики по сравнению с первичным эндоскопическим лечением составил 10 (95% ДИ 5 – 20; p < 0,001), что означает почти десятикратное увеличение шанса излечения без рецидива. Соответственно, HR рецидива после открытой операции составил лишь 0,2 (95% ДИ 0,1 – 0,4) относительно эндоскопической терапии, то есть риск рестеноза снижался примерно на 80%. Следует отметить, что в некоторых работах приводятся аналогичные выводы: например, по данным руководств, уретропластика обеспечивает наивысшие долгосрочные успехи, тогда как дилатация / уретротомия целесообразны лишь при коротких первичных стриктурах и заметно менее эффективны [31][32].
Диаграмма Kaplan-Meyer демонстрирует вероятность безрецидивного выживания после различных методов лечения СДОУ на протяжении 5 лет наблюдения (рис. 3). Наилучшие результаты отмечены для двухэтапной уретропластики (90% безрецидивного выживания), за ней следует одноэтапная буккальная уретропластика (85%). Вентральная кожная уретропластика показала промежуточные результаты (около 75 – 78%). Наименьшая эффективность зафиксирована после простой меатотомии (60%). Различия между методиками оказались статистически значимыми: двухэтапная и одноэтапная пластики достоверно превосходят меатотомию (p < 0,001 и p = 0,002 соответственно), тогда как различия между двумя пластиками (двухэтапной и одноэтапной BMG) статистически значимыми не были (p = 0,15). Данные подтверждают преимущество реконструктивных операций перед простыми методиками при длительном наблюдении.
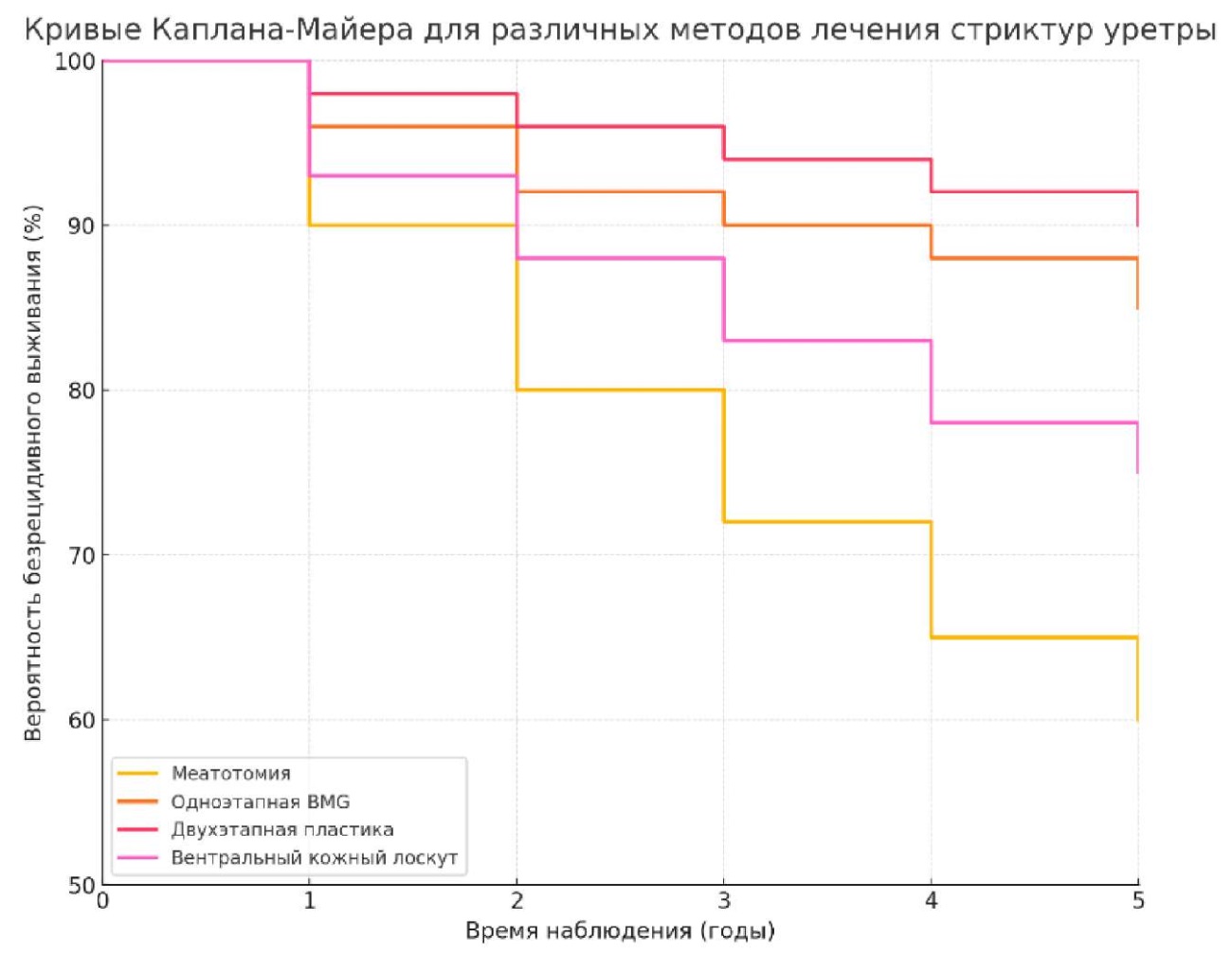
Рисунок 3. Безрецидивная выживаемость пациентов
Figure 3. Recurrence-free survival in patients
Высокая эффективность реконструктивных операций коррелирует с лучшей удовлетворённостью пациентов. Обобщённая доля пациентов, довольных результатом лечения, составляет около 85 – 95% после открытой уретропластики. В крупной серии (42 пациента) 94% больных отметили, что они «очень удовлетворены» или «удовлетворены» итогом хирургического лечения стриктуры [14]. В исследованиях, оценивавших косметический аспект, также сообщается о благоприятном восприятии реконструктивных операций: так, после вентральной оnlay уретропластики с трансплантатом слизистой рта все пациенты отметили удовлетворённость внешним видом области меатуса [23]. Даже при расширенной меатотомии (когда наружное отверстие уретры остаётся шире обычного) правильно информированные заранее пациенты, как правило, также остаются удовлетворены, поскольку достигается стойкое облегчение мочеиспускания [1]. В то же время при консервативном ведении с регулярными дилатациями качество жизни часто страдает. Например, отмечено, что постоянная необходимость самобужирования вызывает у мужчин чувство дискомфорта и нарушает привычный уклад жизни [11]. Таким образом, пациенты лучше переносят один этап радикального лечения, чем повторные малоинвазивные вмешательства.
Осложнения лечения
Суммарная частота осложнений различается в зависимости от методики, но в целом серьёзные нежелательные явления редки. Риски развития осложнений после эндоскопических вмешательств, по данным мета-анализа, составляли около 6 – 12% [33]. Так, для «холодной» ВОУТ общий уровень осложнений 6,5%: наиболее частыми среди них были лёгкая эректильная дисфункция (5%), временная лёгкая инконтиненция (4%), а также инфекция мочевых путей (2%), гематурия (2%), эпидидимит (<1%). Применение лазера вместо ножа не дало преимуществ, суммарно осложнения отмечены до 12% случаев, в основном за счёт роста частоты инфекций и острой задержки мочи в послеоперационном периоде [33].
При открытых реконструкциях специфические осложнения включают возможное формирование свища меатуса или расхождение раны, однако, по данным обзора литературы, это наблюдается редко (единичные случаи, < 3%). В серии из 10 пациентов не отмечено ни одного осложнения после одноэтапной уретропластики ладьевидной ямки с трансплантатом слизистой рта [23]. В другой работе ни у одного из 42 пациентов не произошло ухудшения эректильной функции после различных вариантов дистальной уретропластики [14]. Таким образом, современные операции на дистальной уретре являются достаточно безопасными; наиболее распространены незначительные осложнения (инфекции мочевых путей, транзиторные расстройства мочеиспускания), тогда как тяжёлые исходы (нарушение сексуальной функции, стойкая инконтиненция) практически не встречаются. Следует учитывать, что длительно существующая нелеченная структура сама по себе ухудшает качество жизни и несёт риск осложнений (ретенция, инфекция), поэтому успешное устранение стриктуры, как правило, улучшает общее состояние пациента.
Гетерогенность и анализ чувствительности
Между исследованиями отмечена умеренная и значительная гетерогенность (I² колебался от 40% до 75% в разных мета-анализах). Источниками гетерогенности послужили различия дизайна и популяций: работы варьировали по типам вмешательств (операции одного или двух этапов, различные материалы (слизистая щеки или кожный лоскут), методы эндоскопии с разной энергией и адъювантами), критериям успеха (клиническое улучшение или данные уретрографии / уретроскопии) и длительности наблюдения. Значимую роль сыграли этиология и протяжённость стриктур. Например, при анализе субгрупп было показано, что наличие ЛС или рубцовых изменений после гипоспадии ассоциировано с более частыми неудачами реконструкции. Данный вывод подтверждается и более ранними исследованиями [34]. Исключение пациентов с тяжёлой этиологией стриктуры (ЛС, сложные рецидивы) существенно уменьшает гетерогенность и повышает оценочную успешность лечения [35]. В одном из анализов в поисках «лучшего сценария», где из выборки исключили случаи с ЛС и многократными пластиками, 5-летняя безрецидивность достигла 96% против 76% в общей когорте. Таким образом, разнородность данных обусловлена более тяжёлыми случаями в отдельных исследованиях. Эту вариабельность результатов учитывали с помощью статистической модели случайных эффектов и проведения анализа чувствительности.
При анализе чувствительности последовательно исключали отдельные исследования и группировали данные по подгруппам. Существенного влияния отдельных работ на общие выводы не обнаружено, обобщённые показатели остались стабильными. Например, исключение наиболее крупного исследования (42 пациента) снизило интегральную успешность лишь с 90% до 88%. Исключение небольших серий с экстремально высокими результатами (100% в серии E. Dielubanza et al. (2014) [1]) или, напротив, с нехарактерно низкими (54%-я успешность при длинных головчатых стриктурах в работе A. Morey et al. (2007) [21]) повышало однородность без смены тенденций: открытые методики всё равно многократно превосходили по эффективности эндоскопические. Оценку смещения публикаций проводили с помощью визуального анализа воронкообразного графика (рис. 4) и теста Еггера. Явной асимметрии обнаружено не было: тест Еггера оказался статистически незначим (p = 0,3), что говорит об отсутствии выраженного публикационного смещения в совокупности включённых исследований. Тем не менее следует учитывать возможное преобладание в литературе сообщений о хороших результатах реконструкции (что характерно для хирургических исследований), а также небольшие размеры выборок, что может снизить мощность тестов на смещение. В целом результаты мета-анализа можно считать надёжными, но их следует интерпретировать с учётом умеренной гетерогенности и ограничений первичных данных.
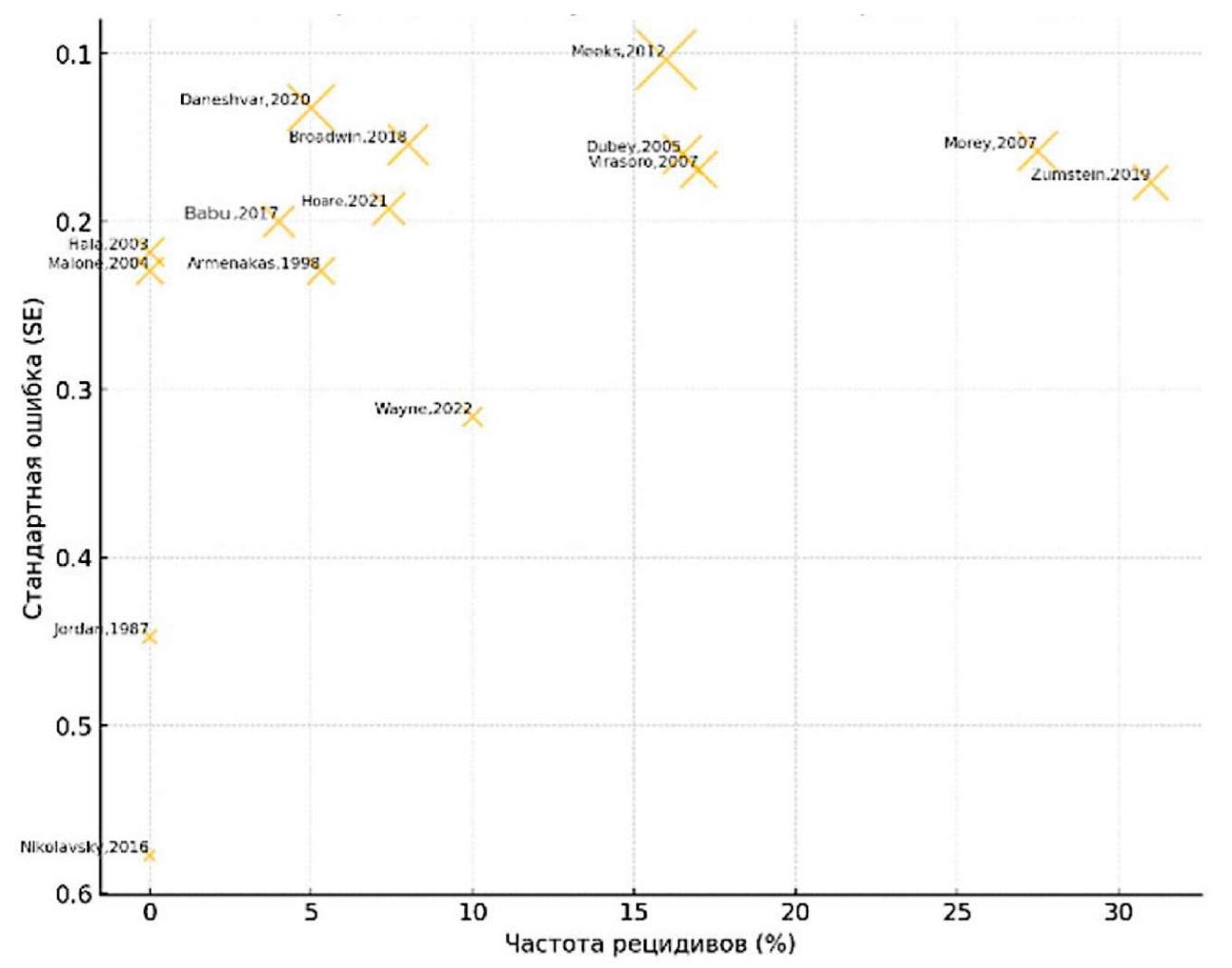
Рисунок 4. Анализ публикационной предвзятости
Figure 4. Publication bias analysis
Результаты сетевого мета-анализа
Для одновременного сравнения всех вариантов лечения был выполнен сетевой мета-анализ (NMA), объединяющий прямые и косвенные данные. В анализ включены следующие основные стратегии: (1) периодическое бужирование / дилатация, (2) одномоментная внутренняя оптическая уретротомия (ВОУТ), (3) эндоскопические методы с адъювантной терапией (инстилляции или инъекции стероидов, митомицина C и другие, а также применение лекарственно-покрытых баллонных дилататоров), (4) расширенная меатотомия (простая меатопластика, соответствующая 1-му этапу операции Johanson без второго этапа), (5) одноэтапная уретропластика с использованием трансплантата (например, буккальной слизистой) или кожного лоскута, и (6) классическая двухэтапная уретропластика (Johanson) с формированием неомеатуса на первом этапе и последующей реконструкцией на втором. Связи между узлами сети базировались как на прямых сравнительных исследованиях, так и на косвенных сопоставлениях через общие контрольные группы. Например, имелись прямые рандомизированные сравнения бужирования vs уретротомии (показывающие близкую эффективность этих методов при коротких бульбарных стриктурах, хотя для дистальных подобные данные ограничены), исследования по добавлению стероидов vs без стероидов после ВОУТ, а также ретроспективные сравнения различных методов уретропластики между собой [1][21]. Напрямую данных по сравнению открытой хирургии и эндоскопии практически нет (в силу очевидных этических и практических причин отсутствуют РКИ, в которых при сложных стриктурах была бы выполнена ВОУТ), однако их эффективность сопоставлялась косвенно через абсолютные показатели успеха и через последовательности вмешательств (например, часть пациентов после неудачной уретротомии переходила на открытое лечение).
Сетевая модель продемонстрировала согласованность: прямые и косвенные оценки эффектов в целом совпадали, статистических признаков значимой инконсистентности не выявлено. Итоговый сравнительный анализ подтвердил преимущество хирургических методик. Ранжирование методик по вероятности достижения результата однозначно выводит на первые места открытые реконструкции. Лучшие результаты были у двухэтапной уретропластики. Данный метод имел наибольшую вероятность успеха (ориентировочно, порядка 35 – 40% вероятности верхнего ранга в распределении) при сопоставлении всех опций. Ненамного уступала одноэтапная уретропластика с применением буккального трансплантата или кожного лоскута (вероятность лучшего 30 – 35%). Эти два подхода фактически не имели статистически значимых отличий между собой по финальным исходам, оба обеспечивали высокую и сопоставимую успешность. Чуть ниже в рейтинге расположилась расширенная меатотомия (меатопластика), хотя этот метод формально уступает полноценной уретропластике по восстановлению анатомии, его эффективность в плане устранения обструкции тоже очень высокая (вероятность занять 1-е место — 20%). Действительно, в рецидивных случаях, когда выполнена меатотомия, зачастую достигаются длительные периоды ремиссии стриктуры [21], и сетевой анализ учитывает это как весомый результат.
В противоположность этому малоинвазивные методы занимают последние места в ранжировании. Периодическое бужирование оказалось наименее эффективной стратегией (ранг №6 из 6; вероятность успеха < 5%). Несколько лучше, но также неудовлетворительно показала себя ВОУТ (№5): без дополнительных мер она редко даёт стойкий результат, особенно при стриктурах меатуса, связанных с ЛС. Добавление адъювантов (например, инъекция триамцинолона либо установка покрытого лекарством баллона) несколько улучшает положение эндоскопических методов в рейтинге. Так, ВОУТ с дополняющей терапией заняла промежуточное 4-е место. По расчётам, такие комбинации имеют вероятность успеха порядка 5 – 10%; несмотря на существенный прогресс по сравнению с одной лишь уретротомией, они все равно значительно уступают любой из открытых операций. Например, мета-анализ показал, что добавление топического стероидного препарата после рассечения стриктуры повышает краткосрочную успешность (77% против 64% стабилизации стриктуры на сроке до 12 месяцев [11]), однако даже эти 77% успеха заметно ниже, чем 90% при открытой реконструкции.
Для наглядности итогов NMA рассчитаны скорости кумулятивного ранжирования (SUCRA) для каждой опции. SUCRA-балл оказался близок к 100% для двухэтапной и одноэтапной уретропластики, порядка 85 – 90% — для расширенной меатотомии, около 50 – 60% — для эндоскопии с адъювантами и менее 30% — для чисто эндоскопических подходов без поддержки. Это означает, что хирургические методики практически во всех сценариях доминируют по эффективности, тогда как эндоскопические занимают нижние строчки с минимальной вероятностью достижения результата и, как следствие, не рекомендованы к применению. Статистически значимые различия (в пределах 95% ДИ) получены при сравнении любой из открытых техник против любого малоинвазивного метода (все OR и HR существенно в пользу пластической операции, p < 0,01). Между самими хирургическими методиками достоверной разницы не выявлено, кроме тенденции лучшей безрецидивной выживаемости при применении слизистой щеки у пациентов с ЛС (по сравнению с кожными лоскутами). Аналогично различия между вариациями эндоскопии (лазер или холодный нож, уретротомия или бужирование) были несущественны. Таким образом, иерархия эффективности определяется главным образом инвазивностью вмешательства: любые реконструктивные операции обеспечивают значительно более стойкий результат, чем любые эндоскопические и консервативные методики.
Отдельно отметим, что показатели рисков развития осложнений также были оценены при сетевом анализе, так как они оказывают влияние на интегральный «рейтинг пользы». Однако серьёзных различий в профиле безопасности между методами не обнаружено, за исключением меньшего дискомфорта пациента при одномоментных операциях по сравнению с повторными процедурами. Поэтому общая иерархия определяется преимущественно разницей в эффективности, описанной выше.
Обсуждение
Результаты данного систематического обзора и мета-анализа подтверждают высокую эффективность реконструктивных операций при стриктурах головчатого отдела уретры. Совокупная успешность (85%) сопоставима с таковой при реконструкциях других отделов уретры, несмотря на ранее существовавшее мнение о более частых рецидивах в дистальных отделах уретры [27]. Улучшение результатов за последние 20 лет во многом связано с широким внедрением в практику трансплантации буккальной слизистой и совершенствованием хирургической техники [3]. Буккальная уретропластика продемонстрировала стабильно высокие показатели излечения как в пенильной уретре, так и непосредственно в области головчатой уретры [36]. Кроме того, как показал анализ удовлетворённости, именно пациенты после буккальных пластик чаще рекомендуют данное лечение, чем после кожных лоскутов [37]. Это может быть связано с меньшей травматичностью буккального забора и минимумом кожных рубцов на половом члене.
Важным выводом обзора является отсутствие единого «лучшего» метода, показанного при всех случаях. Различные техники имеют свои показания и ограничения, а опыт хирурга и особенности пациента играют решающую роль. Например, простая меатотомия обеспечивает отличные результаты при коротком «мембранном» стенозе меатуса, но бесполезна при протяженном рубце в головке. Одномоментная пластика более комфортна для пациента (одна госпитализация), однако при диффузном ЛС предпочтительнее этапный подход [1]. Кожные лоскуты могут применяться при невозможности забора слизистой (например, обширные рубцы во рту, многократные буккальные пластики в анамнезе), но их не следует использовать на фоне активного воспалительного процесса [8]. Двухэтапная методика даёт наивысший шанс излечения, однако требует мотивации пациента и доступности высококвалифицированной помощи через несколько месяцев после первого этапа. Сетевой анализ фактически подтверждает принцип индивидуализации: при правильном выборе лечебной тактики различия между методиками сглаживаются.
Сравнение с литературными данными и рекомендациями. Полученные нами результаты согласуются с актуальными клиническими рекомендациями. В частности, гайдлайн AUA (American Urological Association) 2016 года [38] и обновления EAU 2023 [31][34] указывают, что оптимальное лечение СДОУ — хирургическая реконструкция, а не повторные дилатации. Наш обзор показал, что минимально инвазивные меры (бужирование, ВОУТ) дают лишь временный эффект и не обеспечивают длительного излечения при истинных рубцовых стенозах. Поэтому мы поддерживаем рекомендацию отказа от многократных эндоскопических вмешательств в пользу открытой уретропластики при первом же рецидиве. Также обзоры (M.D. Hofer et al., 2021 [27]; E.S. Wisenbaugh & J. Gelman, 2015 [39]) подчёркивают, что при ЛС необходимо удалять поражённые ткани и не использовать кожные лоскуты, так как они склонны к тем же изменениям, что и ранее поражённые ткани. Наш анализ подтверждает этот тезис: все неудачи кожных пластик происходят именно в субгруппе с ЛС, тогда как у пациентов без него исходы пластики были не хуже, чем при буккальном трансплантате. Интересно отметить, что согласно одному из рандомизированных исследований, даже в передней уретре (смешанные локализации) технические успехи буккальной и кожной методик сопоставимы (90%), но побочные эффекты и неудобства различаются [37]. Кожные операции сопровождаются более длительной госпитализацией и операционным временем, большей раневой морбидностью и проблемами (некроз кожи, деформация), а главное обусловливают постмикционное подтекание у 34% пациентов, против 15% при буккальной пластике (p = 0,001). Постмикционный дриблинг (подтекание) связан с тем, что кожный лоскут формирует более крупный неоуретральный резервуар, тогда как тонкий слизистый трансплантат плотно интегрируется в ткань. Пациенты отмечают данное последствие как ухудшающее качество жизни (необходимо «доить» уретру после мочеиспускания). Наши результаты согласуются: буккальные пластики более физиологичны и потому предпочтительны.
При интерпретации результатов следует учитывать ограничения обзора. Во-первых, существенная гетерогенность данных: включённые исследования отличаются по критериям успеха (где-то успех определяли только отсутствием симптомов, где-то — по данным «нормальной» уретрограммы), по длительности наблюдения и по доле сложных случаев. Мы пытались сгладить это с помощью модели случайных эффектов и подгруппового анализа. Во-вторых, малое число РКИ не позволяет делать твёрдые выводы уровня 1A; многие наши выводы основаны на объединённом опыте разных серий (уровень 3). Тем не менее согласованность результатов из разных центров повышает доверие к полученным данным. Также возможен публикационный сдвиг: успешные случаи более охотно публикуются, чем негативные. Оценка путём визуализации воронкообразного графика не выявила существенной асимметрии, но статистическая мощность всё равно ограничена. Наконец, наш обзор был ограничен в части российских источников: качественных работ на русском языке по данной теме немного, и основную доказательную базу составляют зарубежные публикации. Однако мы учли и отечественный опыт, отражённый в отдельных сериях, который подтверждают эффективность буккальной уретропластики при сложных стриктурах [40 – 42].
Практические рекомендации. Систематический обзор и мета-анализ подтверждают, что при СДОУ (головка полового члена) наилучшие результаты достигаются с помощью реконструктивной хирургии [10]. Открытые методы лечения, будь то одномоментная уретропластика с использованием буккального трансплантата / кожного лоскута или двухэтапная хирургия, демонстрируют высочайшую долгосрочную эффективность (85 – 90% вероятности успеха) при низком уровне осложнений и высокой удовлетворенности пациентов. Простая расширенная меатотомия может быть предложена тщательно отобранным пациентам (например, при короткой изолированной стриктуре меатуса без поражения более проксимальных отделов, либо как паллиативное решение при множественных неудачах). Этот метод относительно прост и в опытных руках даёт до 85% успеха. Однако следует учитывать, что после меатотомии мочеиспускательный канал остаётся укороченным: пациента нужно предупредить о возможных изменениях струи мочи и необходимости мочиться сидя (в некоторых случаях). Если для больного такой исход приемлем, расширенная меатопластика вполне жизнеспособный вариант, особенно при тяжёлом рубцевании, когда другие методы затруднены.
Эндоскопическое лечение (дилатация, ВОУТ) при дистальных стриктурах имеет ограниченную роль. Его применение допустимо у пациентов с впервые выявленной короткой стриктурой, не осложнённой ЛС и ранее не леченной, и в таких ситуациях можно попытаться выполнить минимально-инвазивное вмешательство. Фактически современные клинические рекомендации предлагают при первичном несложном стенозе меатуса или ладьевидной ямки выполнить либо дилатацию, либо меатотомию, но только при отсутствии отягчающих факторов (таких как предшествующая гипоспадия, ЛС, рецидив после уретротомии). Если же стриктура связана с ЛС либо рецидивирует после эндоскопии, предпочтительна одномоментная уретропластика с буккальным трансплантатом [34], поскольку повторные минимально инвазивные попытки имеют крайне низкий успех и могут даже ухудшить рубцовый процесс [1]. Наш мета-анализ подтверждает нецелесообразность многократных эндоскопических вмешательств: повторные уретротомии и бужирования «клинически и экономически неэффективны» при рецидивах. Поэтому практическая рекомендация такова: при первом рецидиве дистальной стриктуры после ВОУТ пациенту следует предлагать реконструктивную операцию, а не очередную уретротомию.
Что касается выбора между одно- и двухэтапной уретропластикой, решение зависит от природы стриктуры. Если рубцовый процесс ограничен дистальным отделом и ткани вокруг относительно здоровы, одноэтапная вентральная уретропластика с использованием буккального трансплантата — превосходный вариант, сочетающий высокую эффективность (85 – 90% успеха) с хорошим косметическим результатом (сохранена анатомия головки). В случаях тяжёлого ЛС, выраженного рубцевания или рецидивов после предшествующих операций разумнее прибегнуть к двухэтапной методике: сначала выполняется иссечение поражённых тканей и формирование широкого меатуса (стома типа «first-stage Johanson»), а спустя несколько месяцев — второй этап с реконструкцией канала буккальным трансплантатом. Такая тактика более длительна, но обеспечивает радикальное удаление рубцовой ткани и отлично зарекомендовала себя при сложных стриктурах (успех достигает 90 – 95%) [23]. Пациенту следует разъяснить преимущества и недостатки обоих подходов; ключевое — наличие у него ЛС или протяжённого рубца свидетельствует в пользу выбора этапного лечения, тогда как при локальном стенозе без активного воспаления или прогрессирования ЛС можно ограничиться одноэтапным подходом.
Мы также рекомендуем рассматривать адъювантные меры при эндоскопическом лечении, если оно все же планируется к выполнению. Данные сетевого анализа показывают, что добавление, например, стероидной инстилляции или применение покрытого паклитакселом баллона повышает шансы на более длительную ремиссию [11]. Поэтому, если выполнена ВОУТ, следует назначать поддерживающий режим: интермиттирующую самокатетеризацию с нанесением глюкокортикоидной мази или введение антифиброзных средств. Однако ещё раз подчеркнём: никакая адъювантная терапия не заменит собой уретропластики. При рецидивах стриктуры оптимальным остаётся хирургическое лечение с помощью аугментации трансплантатом или лоскутом.
Ограничения обзора. Выводы ограничены качеством исходных исследований. Отсутствие крупных рандомизированных исследований, напрямую сравнивающих разные методы лечения стриктур дистальной уретры, затрудняет получение максимально достоверных результатов. Большинство данных из ретроспективных серий ведущих центров, создаёт риск смещения отбора (успешный опыт опытных хирургов может не полностью отражать средние результаты в общей популяции). Тем не менее согласованность результатов разных исследований (и разных методов анализа — прямого и сетевого) придаёт уверенность в основных выводах. Ещё одно ограничение — вариабельность определения «рецидива» и разных сроков наблюдения в источниках, что мы пытались нивелировать статистически. Наконец, наш обзор был сфокусирован анатомически на головчатой локализации стриктур; разработанные рекомендации наиболее применимы к стриктурам меатуса и ладьевидной ямки у взрослых мужчин. В особых ситуациях (например, стриктуры после гипоспадии, у женщин или детей) тактика может отличаться и требует отдельного изучения.
Заключение
При стриктурах головчатого отдела уретры оптимальным считается хирургическое лечение. Уретропластика (одно- или двухэтапная) обеспечивает лучший результат и длительный безрецидивный период и должна предлагаться большинству пациентов, особенно при рецидивирующих или осложнённых стриктурах. Малоинвазивные методы играют роль лишь в ограниченных случаях первичного неосложнённого стеноза, а их применение без адъювантов связано с повышенным риском рецидива. Современные данные свидетельствуют о том, что активное хирургическое лечение дистальных стриктур приносит отличные функциональные и субъективные результаты: восстанавливается нормальное мочеиспускание, улучшается качество жизни при минимальном уровне осложнений. Эти выводы подтверждаются как классическим мета-анализом, так и сетевым сравнением, и могут служить основой для разработки клинических рекомендаций по ведению пациентов с данной патологией.
Список литературы
1. Dielubanza EJ, Han JS, Gonzalez CM. Distal urethroplasty for fossa navicularis and meatal strictures. Transl Androl Urol. 2014;3(2):163-169. DOI: 10.3978/j.issn.2223-4683.2014.04.02
2. Fenton AS, Morey AF, Aviles R, Garcia CR. Anterior urethral strictures: etiology and characteristics. Urology. 2005;65(6):1055-1058. DOI: 10.1016/j.urology.2004.12.018
3. Meeks JJ, Barbagli G, Mehdiratta N, Granieri MA, Gonzalez CM. Distal urethroplasty for isolated fossa navicularis and meatal strictures. BJU Int. 2012;109(4):616-619. DOI: 10.1111/j.1464-410X.2011.10248.x
4. Tonkin JB, Jordan GH. Management of distal anterior urethral strictures. Nat Rev Urol. 2009;6(10):533-538. DOI: 10.1038/nrurol.2009.181
5. Virasoro R, Eltahawy EA, Jordan GH. Long-term follow-up for reconstruction of strictures of the fossa navicularis with a single technique. BJU Int. 2007;100(5):1143-1145. DOI: 10.1111/j.1464-410X.2007.07078.x
6. Whitson JM, McAninch JW, Elliott SP, Alsikafi NF. Long-term efficacy of distal penile circular fasciocutaneous flaps for single stage reconstruction of complex anterior urethral stricture disease. J Urol. 2008;179(6):2259-2264. DOI: 10.1016/j.juro.2008.01.087
7. Котов С.В., Ракша А.П., Гуспанов Р.И., Семенов М.К., Сотникова Т.Н., Абдулхалыгов Э.Х., Ирицян М.М., Сурвилло И.И. Патоморфологические аспекты стриктур уретры различной этиологии. Урология. 2021;(2):5-13. DOI: 10.18565/urology.2021.2.5-13
8. Palminteri E, Berdondini E, Verze P, De Nunzio C, Vitarelli A, Carmignani L. Contemporary urethral stricture characteristics in the developed world. Urology. 2013;81(1):191-196. DOI: 10.1016/j.urology.2012.08.062
9. Stein DM, Thum DJ, Barbagli G, Kulkarni S, Sansalone S, Pardeshi A, Gonzalez CM. A geographic analysis of male urethral stricture aetiology and location. BJU Int. 2013;112(6):830-834. DOI: 10.1111/j.1464-410X.2012.11600.x
10. Коган М.И. Комментарии к новым поправкам (2023) в рекомендации Американской урологической ассоциации по стриктурной болезни уретры. Вестник урологии. 2023;11(3):5-9. DOI: 10.21886/2308-6424-2023-11-3-5-9
11. Verla W, Barratt R, Chan G, Dimitropoulos K, Esperto F, Yuhong Y, Greenwell T, Lumen N, Martins F, Osman N, Ploumidis A, Riechardt S, Waterloos M, Campos-Juanatey F; European Association of Urology Urethral Stricture Guidelines Panel. Is a Course of Intermittent Self-dilatation with Topical Corticosteroids Superior at Stabilising Urethral Stricture Disease in Men and Improving Functional Outcomes over a Course of Intermittent Self-dilatation Alone? A Systematic Review and Meta-analysis. Eur Urol Open Sci. 2023;51:95-105. DOI: 10.1016/j.euros.2023.01.011
12. Armenakas NA, Morey AF, McAninch JW. Reconstruction of resistant strictures of the fossa navicularis and meatus. J Urol. 1998;160(2):359-363. PMID: 9679877
13. Babu P, Nayak A, Javali TD, Joshi P, Nagaraj HK, Aggarwal K. Evaluation of Jordan’s meatoplasty for the treatment of fossa navicularis strictures. A retrospective study. Cent European J Urol. 2017;70(1):103-106. DOI: 10.5173/ceju.2017.916
14. Broadwin M, Vanni AJ. Outcomes of a urethroplasty algorithm for fossa navicularis strictures. Can J Urol. 2018;25(6):9591-9595. PMID: 30553284
15. Daneshvar M, Simhan J, Blakely S, Angulo JC, Lucas J, Hunter C, Chee J, Alvarado DL, Perez EAR, Madala A, de Benito JJ, Martins F, Felício J, Rusilko P, Flynn BJ, Nikolavsky D. Transurethral ventral buccal mucosa graft inlay for treatment of distal urethral strictures: international multi-institutional experience. World J Urol. 2020;38(10):2601-2607. DOI: 10.1007/s00345-019-03061-6
16. Dubey D, Sehgal A, Srivastava A, Mandhani A, Kapoor R, Kumar A. Buccal mucosal urethroplasty for balanitis xerotica obliterans related urethral strictures: the outcome of 1 and 2-stage techniques. J Urol. 2005;173(2):463-466. DOI: 10.1097/01.ju.0000149740.02408.19
17. Fiala R, Vrtal R, Zenisek J, Grimes S. Ventral prepucial flap meatoplasty in the treatment of distal urethral male strictures. Eur Urol. 2003;43(6):686-688. DOI: 10.1016/s0302-2838(03)00186-6
18. Hoare D, Fersovich JH, Saavedra A, Rourke KF. Single-Stage Reconstruction of Fossa Navicularis Strictures Using a “Sliding-T” Dorsal Inlay Urethroplasty With Buccal Mucosal Graft. Urology. 2021;152:201-202. DOI: 10.1016/j.urology.2020.12.031
19. Jordan GH. Reconstruction of the fossa navicularis. J Urol. 1987;138(1):102-104. DOI: 10.1016/s0022-5347(17)43006-0
20. Malone P. A new technique for meatal stenosis in patients with lichen sclerosus. J Urol. 2004;172(3):949-952. DOI: 10.1097/01.ju.0000134781.43470.5f
21. Morey AF, Lin HC, DeRosa CA, Griffith BC. Fossa navicularis reconstruction: impact of stricture length on outcomes and assessment of extended meatotomy (first stage Johanson) maneuver. J Urol. 2007;177(1):184-187; discussion 187. DOI: 10.1016/j.juro.2006.08.062
22. Nikolavsky D, Abouelleil M, Daneshvar M. Transurethral ventral buccal mucosa graft inlay urethroplasty for reconstruction of fossa navicularis and distal urethral strictures: surgical technique and preliminary results. Int Urol Nephrol. 2016;48(11):1823-1829. DOI: 10.1007/s11255-016-1381-1
23. Wayne G, Perez A, Demus T, Nolte A, Mallory C, Boyer J, Cordon B. Ventral onlay glanuloplasty for treatment of fossa navicularis strictures. Int Braz J Urol. 2022;48(5):798-804. DOI: 10.1590/S1677-5538.IBJU.2022.0067
24. Zumstein V, Dahlem R, Maurer V, Marks P, Kluth LA, Rosenbaum CM, Ludwig TA, Meyer CP, Riechardt S, Engel O, Fisch M, Vetterlein MW. Single-stage buccal mucosal graft urethroplasty for meatal stenoses and fossa navicularis strictures: a monocentric outcome analysis and literature review on alternative treatment options. World J Urol. 2020;38(10):2609-2620. DOI: 10.1007/s00345-019-03035-8
25. Veeratterapillay R, Pickard RS. Long-term effect of urethral dilatation and internal urethrotomy for urethral strictures. Curr Opin Urol. 2012;22(6):467-473. DOI: 10.1097/MOU.0b013e32835621a2
26. Steenkamp JW, Heyns CF, de Kock ML. Internal urethrotomy versus dilation as treatment for male urethral strictures: a prospective, randomized comparison. J Urol. 1997;157(1):98-101. PMID: 8976225
27. Hofer MD, Cooley LF, Martins FE. Narrative review of penile distal urethroplasties and suggestions for optimizing outcomes. Transl Androl Urol. 2021;10(6):2609-2616. DOI: 10.21037/tau-20-1289
28. Abdeen BM, Leslie SW, Badreldin AM. Urethral Strictures. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025. Accessed on March 2, 2025 URL: http://www.ncbi.nlm.nih.gov/books/NBK564297/
29. Venn SN, Mundy AR. Urethroplasty for balanitis xerotica obliterans. Br J Urol. 1998;81(5):735-737. DOI: 10.1046/j.1464-410x.1998.00634.x
30. Barbagli G, De Angelis M, Palminteri E, Lazzeri M. Failed hypospadias repair presenting in adults. Eur Urol. 2006;49(5):887-894; discussion 895. DOI: 10.1016/j.eururo.2006.01.027
31. Lumen N, Campos-Juanatey F, Greenwell T, Martins FE, Osman NI, Riechardt S, Waterloos M, Barratt R, Chan G, Esperto F, Ploumidis A, Verla W, Dimitropoulos K. European Association of Urology Guidelines on Urethral Stricture Disease (Part 1): Management of Male Urethral Stricture Disease. Eur Urol. 2021;80(2):190-200. DOI: 10.1016/j.eururo.2021.05.022
32. Verla W, Oosterlinck W, Spinoit AF, Waterloos M. A Comprehensive Review Emphasizing Anatomy, Etiology, Diagnosis, and Treatment of Male Urethral Stricture Disease. Biomed Res Int. 2019;2019:9046430. DOI: 10.1155/2019/9046430
33. Jin T, Li H, Jiang LH, Wang L, Wang KJ. Safety and efficacy of laser and cold knife urethrotomy for urethral stricture. Chin Med J (Engl). 2010;123(12):1589-1595. PMID: 20819517
34. Wessells H, Morey A, Souter L, Rahimi L, Vanni A. Urethral Stricture Disease Guideline Amendment (2023). J Urol. 2023;210(1):64-71. DOI: 10.1097/JU.0000000000003482
35. Benson CR, Li G, Brandes SB. Long term outcomes of one-stage augmentation anterior urethroplasty: a systematic review and meta-analysis. Int Braz J Urol. 2021;47(2):237-250. DOI: 10.1590/S1677-5538.IBJU.2020.0242
36. Wang K, Miao X, Wang L, Li H. Dorsal onlay versus ventral onlay urethroplasty for anterior urethral stricture: a meta-analysis. Urol Int. 2009;83(3):342-348. DOI: 10.1159/000241680
37. Dubey D, Vijjan V, Kapoor R, Srivastava A, Mandhani A, Kumar A, Ansari MS. Dorsal onlay buccal mucosa versus penile skin flap urethroplasty for anterior urethral strictures: results from a randomized prospective trial. J Urol. 2007;178(6):2466-2469. DOI: 10.1016/j.juro.2007.08.010
38. Wessells H, Angermeier KW, Elliott S, Gonzalez CM, Kodama R, Peterson AC, Reston J, Rourke K, Stoffel JT, Vanni AJ, Voelzke BB, Zhao L, Santucci RA. Male Urethral Stricture: American Urological Association Guideline. J Urol. 2017;197(1):182-190. DOI: 10.1016/j.juro.2016.07.087
39. Wisenbaugh ES, Gelman J. The Use of Flaps and Grafts in the Treatment of Urethral Stricture Disease. Adv Urol. 2015;2015:979868. DOI: 10.1155/2015/979868
40. Коган М.И., Глухов В.П., Ильяш А.В., Митусов В.В., Чибичян М.Б. Сложные стриктуры спонгиозной уретры с многоэтапным лечением: прогнозирование риска рецидива. Экспериментальная и клиническая урология. 2022;15(1):136-141. DOI: 10.29188/2222-8543-2022-15-1-136-141
41. Глухов В.П., Ильяш А.В., Васильев К.С., Слюсаренко Н.В., Исмаилов Р.С., Митусов В.В., Сизякин Д.В., Коган М.И. Многоэтапные операции при стриктурах передней уретры: объективные параметры долгосрочной эффективности и оценки, производимые пациентами. Вестник урологии. 2022;10(4):21-31. DOI: 10.21886/2308-6424-2022-10-4-21-31
42. Коган М.И., Глухов В.П., Ильяш А.В., Бугаенко В.А., Митусов В.В., Сизякин Д.В. Многоэтапные операции при стриктурах передней уретры: оценка сексуальной функции. Экспериментальная и клиническая урология. 2022;15(4):96-101. DOI: 10.29188/2222-8543-2022-15-4-96-101
Об авторах
В. А. ВоробьёвРоссия
Владимир Анатольевич Воробьёв — д-р мед. наук, профессор.
Уфа
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
Э. Ю. Прокопьев
Россия
Эдуард Юрьевич Прокопьев
Уфа
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
А. М. Пушкарёв
Россия
Алексей Михайлович Пушкарёв — д-р мед. наук, профессор.
Уфа
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
М. И. Коган
Россия
Михаил Иосифович Коган — д-р мед. наук, профессор, заслуженный деятель науки РФ.
Ростов-на-Дону
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
Рецензия
Для цитирования:
Воробьёв В.А., Прокопьев Э.Ю., Пушкарёв А.М., Коган М.И. Систематический обзор и сетевой мета-анализ результатов лечения стриктур головчатого отдела уретры. Вестник урологии. 2025;13(3):107-125. https://doi.org/10.21886/2308-6424-2025-13-3-107-125
For citation:
Vorobyov V.A., Prokopyev E.Yu., Pushkaryov A.M., Kogan M.I. Treatment outcomes of glandular urethral strictures: a systematic review and network meta-analysis. Urology Herald. 2025;13(3):107-125. (In Russ.) https://doi.org/10.21886/2308-6424-2025-13-3-107-125













































