Перейти к:
Собственный взгляд на роль уретроскопии в диагностике и выборе тактики лечения при коротких стриктурах бульбозной уретры
https://doi.org/10.21886/2308-6424-2025-13-3-39-51
Аннотация
Введение. Значимость уретроскопии в диагностике стриктуры уретры была занижена в последнее время вследствие приоритета в пользу уретрографии. Однако данный метод позволяет выявить различные аспекты стриктуры уретры, которые могут существенно повлиять на выбор объёма оперативного вмешательства.
Цель исследования. Оценить диагностические возможности уретроскопии и результаты выбранной на её основе тактики лечения у пациентов со стриктурой уретры.
Материалы и методы. В исследование включены 7 мужчин с короткой стриктурой (< 2 см) бульбозной уретры, у которых проводили лечение путём удаления фибриновых тканей уретры в ходе уретроскопии. Возраст пациентов варьировался от 19 до 73 лет при среднем значении 44,6 ± 19,4 лет. Длина стриктуры по данным ретроградной уретрографии колебалась от 0,5 до 1,5 см при среднем значении 1,0 ± 0,3 см. У 4 (57,1%) пациентов стриктура уретры носила первичный характер, у 3 (42,9%) — рецидивный. У 4 (57,1%) пациентов имело место наличие цистостомического дренажа. Уретроскопию выполняли по стандартной технике с использованием уретероскопа размером 9,5 Ch, в ходе неё исследовали характер изменений слизистой и степень сужения просвета уретры. Далее оценивали возможность лёгкого (без приложения сильного давления) разобщения фибриновых сращений от стенки уретры с помощью уретероскопа. Затем инструмент удаляли и устанавливали уретральный силиконовый катетер диаметром 18 Ch на 21 день.
Результаты. У всех пациентов в ходе проведения уретроскопии в бульбозном отделе уретры были выявлены фибриновые перепонки (n = 5) либо тяжи (n = 2), которые практически полностью закрывали просвет уретры в данной зоне. При этом не отмечалось кольцевидное (истинное) сужение уретры в этой области, характерное для спонгиофиброза или истинного поражения слизистой уретры. Фибриновые перепонки и тяжи имели тонкий слой и рыхлую структуру, что позволяло провести через них эндоурологический проводник. После этого плавным движением уретероскопа легко удалось у всех пациентов снять фибриновые сращения по всему периметру стенки уретры, так как они имели неплотный (рыхлый) характер соединений со слизистой уретры. Ни в одном наблюдении не проводили холодное либо лазерное рассечение фибриновых волокон или самой стенки уретры на этом участке, а при удалении фибриновых тканей эндоскопом надрыва слизистой уретры не возникло. После освобождения от фибриновых сращений стенка уретры имела хорошую эластичность, что позволило свободно провести катетер Foley 18 Ch. Продолжительность манипуляции колебалась от 5 до 10 минут и составила в среднем 7,6 ± 1,7 минут. Сроки наблюдения после лечения пациентов варьировались от 8 до 24 месяцев при среднем значении 13,6 ± 5,3 месяцев. Каких-либо осложнений во время или после манипуляции, а также рецидива стриктуры уретры за весь период наблюдения ни у одного пациента не отмечено.
Заключение. Уретроскопия позволяет выявить те случаи стриктуры уретры, которые можно корректировать без проведения уретропластики либо внутренней уретротомии. В связи с этим целесообразно более активно использовать уретроскопию при обследовании пациентов со стриктурой уретры.
Для цитирования:
Катибов М.И., Богданов А.Б., Лоран О.Б. Собственный взгляд на роль уретроскопии в диагностике и выборе тактики лечения при коротких стриктурах бульбозной уретры. Вестник урологии. 2025;13(3):39-51. https://doi.org/10.21886/2308-6424-2025-13-3-39-51
For citation:
Katibov M.I., Bogdanov A.B., Loran O.B. Personal perspective on the role of urethroscopy in the diagnosis and treatment strategy selection for short strictures of the bulbar urethra. Urology Herald. 2025;13(3):39-51. (In Russ.) https://doi.org/10.21886/2308-6424-2025-13-3-39-51
Введение
Стриктура уретры является одним из достаточно часто встречающихся среди мужчин урологических заболеваний. Её распространённость в мужской популяции составляет примерно 229–627 случаев на 100 000 человек [1]. Уретропластика с её многочисленными вариантами в зависимости от характеристик стриктуры является единственным радикальным методом лечения данного заболевания, так как подразумевает полное иссечение рубцово-измененных тканей с последующим соединением здоровых концов уретры (с замещением части уретры лоскутом или трансплантатом из другой ткани в случае такой необходимости) [2]. Различные малоинвазивные методики (холодная или лазерная внутренняя уретротомия, дилатация уретры и другие) носят паллиативный характер, потому что при их использовании происходит только лишь рассечение либо растяжение рубца, а не его иссечение. Поэтому последние имеют ограниченные показания к применению [3 – 5]. Однако следует понимать, что и в случае использования уретропластики достаточно часто отмечается рецидив стриктуры уретры. К примеру, C.R. Benson et al. (2019) сообщили, что частота рецидива стриктуры уретры после передней и задней уретропластики в течение первого года достигает 25% и 18%, в течение 5 лет — 40% и 25% соответственно [6]. Эти обстоятельства обусловливают актуальность изучения различных подходов к снижению рисков рецидива стриктуры уретры.
Ключевыми факторами улучшения результатов лечения таких пациентов являются точная предоперационная оценка особенностей стриктуры уретры и выбор адекватного объёма оперативного вмешательства. С учётом этого необходимо на предоперационном этапе в максимальной степени использовать диагностические возможности различных методов, в число которых входит и уретроскопия. Значимость данного метода в диагностике стриктуры уретры была занижена за последнее время вследствие приоритета в этом вопросе в пользу уретрографии. Подтверждением этому служат положения отечественных и международных рекомендаций по стриктуре уретры, в которых уретроскопия рассматривается как дополнительный, а не обязательный метод диагностики [7–10]. На важность усиления роли эндоскопии в диагностике стриктуры уретры указывает М.И. Коган (2023), отмечая, что данный метод позволяет определить не только локализацию и границы сужения, но и величину просвета и жёсткость стенок уретры [11].
Таким образом, с учётом вышеизложенных данных целью исследования служила оценка диагностических возможностей уретроскопии и результатов выбранной на её основе тактики лечения у пациентов со стриктурой бульбозной уретры.
Материалы и методы
Дизайн исследования. В проспективное обсервационное неконтролируемое исследование включены 7 мужчин со стриктурой бульбозной уретры, у которых в период с сентября 2022 года по декабрь 2023 года проводили лечение путём удаления фибриновых тканей уретры в ходе уретроскопии.
Критерием включения пациентов в исследование служила совокупность следующих клинических факторов: 1) короткая (< 2 см) стриктура бульбозной уретры, по данным ретроградной уретрографии; 2) обструктивный тип мочеиспускания, по данным урофлоуметрии, или наличие цистостомического дренажа; 3) информированное согласие пациента. Критериями исключения считали: 1) выраженный спонгиофиброз при стриктуре бульбозной уретры; 2) локализацию стриктуры вне бульбозной уретры; 3) воспалительные заболевания органов мочеполовой системы в стадии обострения; 4) нейрогенные расстройства мочевого пузыря; 5) инкурабельные сопутствующие заболевания.
В обязательный объём обследования перед лечением входили следующие методы: оценка жалоб и анамнеза; физикальное исследование; общий анализ и посев мочи; урофлоуметрия (Urocap III; "Laborie Medical Technologies", Mississauga, Ontario, Canada); УЗИ органов мочеполовой системы с измерением объёма остаточной мочи (Toshiba Nemio XG SSA – 580A; "Toshiba Medical Systems Corp.", Otawara, Japan); ретроградная уретрография.
Контрольное обследование после лечения проводили через 3, 6, 12, 18 и 24 месяца. В эти сроки выполняли урофлоуметрию и УЗИ с измерением объёма остаточной мочи. Всем пациентам при максимальном сроке наблюдения для каждого из них (сроки — от 8 до 24 месяцев после лечения) выполняли ретроградную уретрографию.
Критериями успеха лечения считали отсутствие жалоб на затрудненное мочеиспускание и необходимости в проведении любого варианта хирургического вмешательства (в том числе бужирования уретры) в связи с сужением уретры.
Конечные точки. Первичными конечными точками исследования являлась оценка эффективности и безопасности лечения коротких стриктур бульбозной уретры путём удаления фибриновых тканей из просвета уретры в ходе уретроскопии. Исследовательские конечные точки — оценка степени изменения максимальной скорости мочеиспускания (Q max) и средней скорости мочеиспускания (Q ave) после данной манипуляции относительно их значений до лечения.
Методика проведения манипуляции. Уретроскопию выполняли по стандартной технике с использованием ригидного уретероскопа с диаметром тубуса 9,5 Ch ("Karl Storz SE & Co. KG" , Tuttlingen, Germany) в литотомическом положении пациента под внутривенной анестезией. В зоне стриктуры уретры оценивали характер фибриновых скоплений (толщина фибриновых образований, плотность их сращений со стенкой уретры) и степень сужения просвета уретры вследствие данных изменений. По сохранившемуся точечному просвету уретры между фибриновыми скоплениями проводили эндоурологический проводник, под контролем которого осуществляли попытку проведения уретероскопа через зону фибриновых образований. При этом оценивали возможность лёгкого (без приложения сильного давления) разобщения фибриновых сращений от стенки уретры с помощью уретероскопа. Только в случае тонкого слоя фибриновых элементов и рыхлости их соединения со стенкой уретры плавным движением уретероскопа отделяли фибриновые скопления от слизистой уретры. После освобождения просвета уретры от фибриновых сращений оценивали степень растяжимости стенки уретры в данной зоне и далее проводили исследование проксимальных отделов уретры. Затем инструмент удаляли и устанавливали уретральный силиконовый катетер Foley диаметром 18 Ch сроком 3 недели. Такой длительный срок нахождения уретрального катетера был выбран исходя из предположений, что за это время произойдет полное отторжение либо лизис остатков фибриновых образований за счёт компрессии последних катетером, а наличие катетера будет препятствовать повторному сращению остатков фибриновых элементов между собой и со стенкой уретры и будет способствовать полноценному восстановлению эпителия слизистой уретры на данном участке. С целью профилактики инфекционно-воспалительных осложнений на время нахождения уретрального катетера пациенты получали пероральную антибактериальную терапию с учётом чувствительности выявленной при посеве мочи микрофлоры либо эмпирически (левофлоксацин 500 мг или ломефлоксацин 400 мг в сутки) при отсутствии роста микрофлоры.
Статистический анализ. Статистическая обработка результатов проведена c использованием программы Statistica v.13.3 (StatSoft Inc., Tulsa, OK, USA). Все показатели проверены на нормальность распределения с помощью теста Shapiro-Wilk. Так как распределение указанных количественных признаков в представленной выборке пациентов соответствовало закону нормального распределения, все параметры были представлены в виде среднего значения (M) ± стандартного отклонения (SD): M ± SD. Качественные признаки были описаны в виде абсолютных (n) и относительных (%) их значений. Изменения Q max и Q ave после манипуляции относительно их значений до лечения оценивали с помощью t-критерия Student. Принятый уровень значимости p < 0,05 при α = 0,05.
Результаты
Результаты обследования перед лечением. Возраст пациентов варьировался от 19 до 73 лет при среднем значении 44,6 ± 19,4 лет. Были установлены 3 вида причин стриктуры уретры: ятрогенная (n = 2), травматическая (n = 1) и идиопатическая (n = 4). Ятрогенная стриктура в одном наблюдении была связана с выполнением уретроцистоскопии (пациент № 5), в другом наблюдении — с установкой уретрального катетера (пациент № 7). У трёх пациентов по результатам посева мочи была выявлена микрофлора в количестве ≥ 50 тыс. КОЕ/мл: Proteus mirabilis — в двух случаях, Staphylococcus epidermidis — в одном случае. Все они получили перед манипуляцией антибактериальную терапию с учётом чувствительности культуры к антибиотикам. Длина стриктуры, по данным ретроградной уретрографии, колебалась от 0,5 до 1,5 см при среднем значении 1,0 ± 0,3 см. Уретрограммы всех пациентов до лечения представлены на рисунках 1–7. В четырёх наблюдениях (57,1%) стриктура уретры носила первичный характер, в трёх наблюдениях (42,9%) — рецидивный. Рецидив стриктуры уретры после предшествовавших операций произошел у двух пациентов после анастомотической уретропластики (пациенты № 1 и № 2), у одного — внутренней оптической уретротомии (пациент № 7). У 4 (57,1%) пациентов имело место наличие цистостомического дренажа. У остальных трёх пациентов с сохранённым самостоятельным мочеиспусканием объём остаточной мочи в среднем составлял 92,0 ± 10,6 мл (80 – 100 мл), Q max — 9,1 ± 0,2 мл/с (8,9 – 9,3 мл/с), Q ave — 6,0 ± 0,3 мл/с (5,7 – 6,3 мл/с). Детализация данных обследования перед лечением по каждому пациенту приведена в таблице.
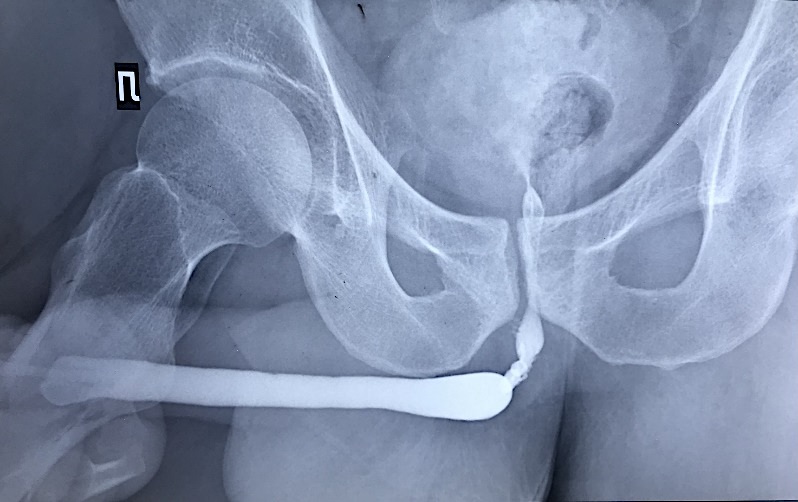
Рисунок 1. Уретрограмма пациента № 1
Figure 1. Urethrogram of patient No. 1
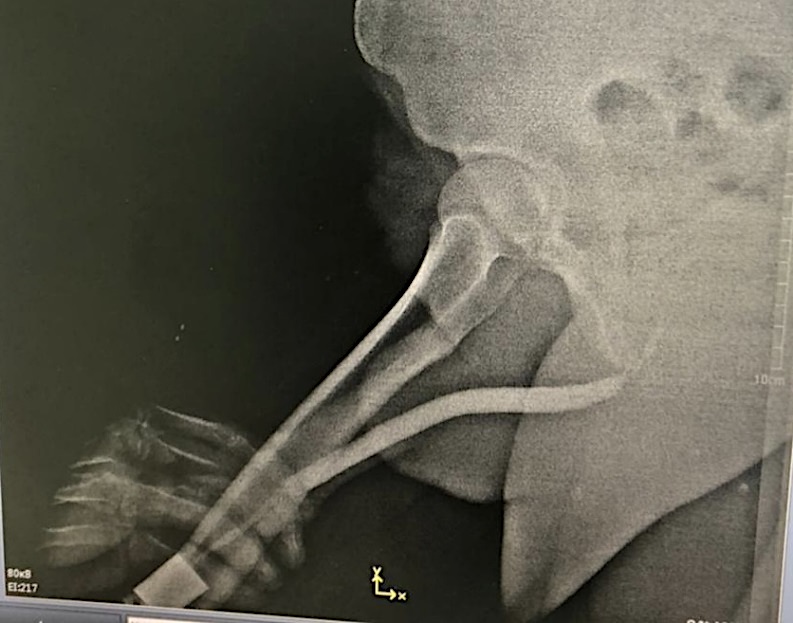
Рисунок 2. Уретрограмма пациента № 2
Figure 2. Urethrogram of patient No. 2
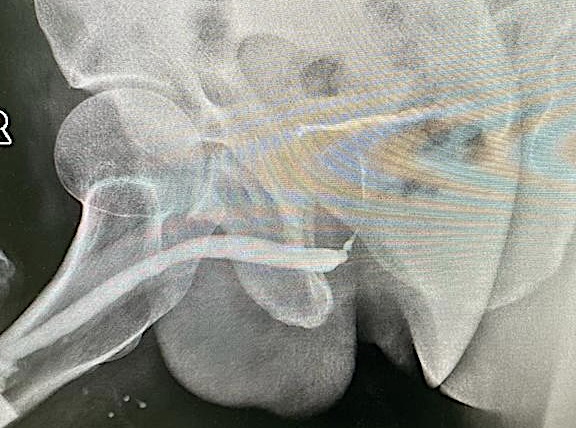
Рисунок 3. Уретрограмма пациента № 3
Figure 3. Urethrogram of patient No. 3
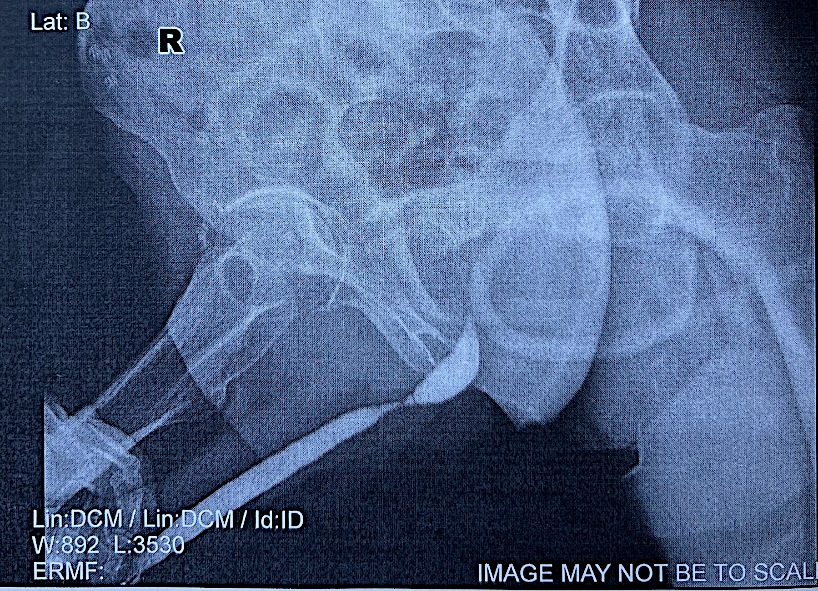
Рисунок 4. Уретрограмма пациента № 4
Figure 4. Urethrogram of patient No. 4
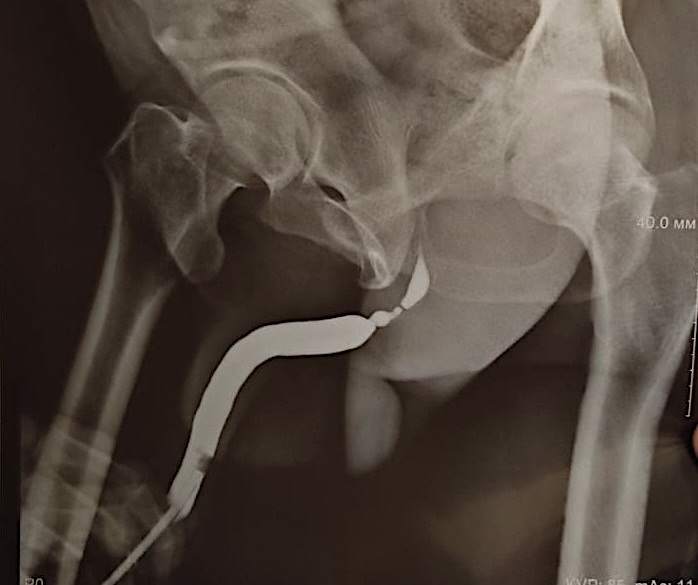
Рисунок 5. Уретрограмма пациента № 5
Figure 5. Urethrogram of patient No. 5
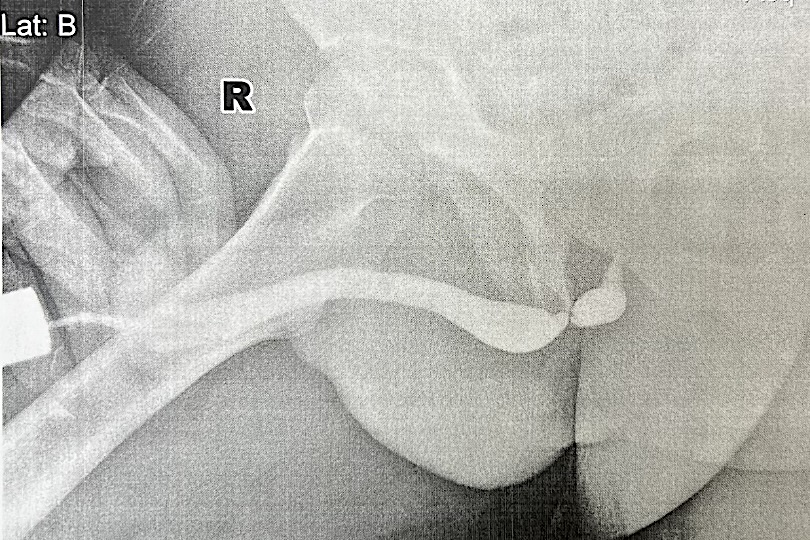
Рисунок 6. Уретрограмма пациента № 6
Figure 6. Urethrogram of patient No. 6
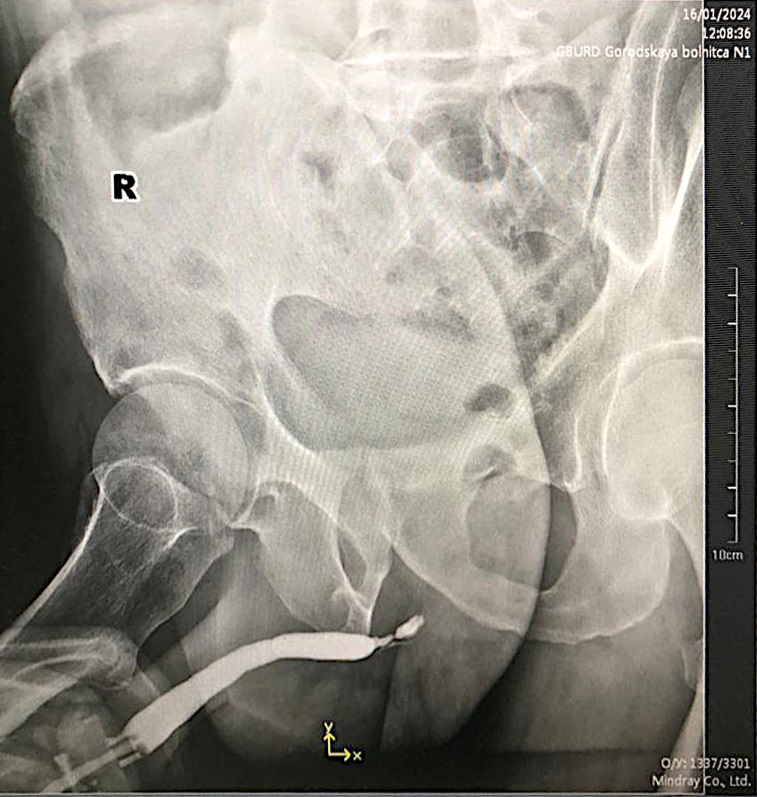
Рисунок 7. Уретрограмма пациента № 7
Figure 7. Urethrogram of patient No. 7
Таблица. Данные пациентов до лечения
Table. Patient data before treatment
Порядковый номер пациента Ordinal number patient | Возраст, лет Age, years | Этиология стриктуры уретры Urethral stricture etiology | Длина стриктуры, см Stricture length, cm | Характер стриктуры уретры Nature of urethral stricture | Наличие цистостомы Cystostomy | Объём остаточной мочи, мл Post-void residual urine volume, ml | Q max, мл/с Q max, ml/s | Q ave, мл/с Q ave, ml/s |
1 | 44 | Идиопатическая Idiopathic | 1,0 | Рецидивный Recurrent | Нет Not | 96 | 8,9 | 5,7 |
2 | 19 | Травматическая Traumatic | 1,0 | Рецидивный Recurrent | Да Yes | – | – | – |
3 | 51 | Идиопатическая Idiopathic | 0,5 | Первичный Primary | Да Yes | – | – | – |
4 | 73 | Идиопатическая Idiopathic | 1,5 | Первичный Primary | Да Yes | – | – | – |
5 | 41 | Ятрогенная Iatrogenic | 1,1 | Первичный Primary | Да Yes | – | – | – |
6 | 23 | Идиопатическая Idiopathic | 0,7 | Первичный Primary | Нет Not | 100 | 9,1 | 6,3 |
7 | 61 | Ятрогенная Iatrogenic | 1,2 | Рецидивный Recurrent | Нет Not | 80 | 9,3 | 5,9 |
Примечание. Q max — максимальная скорость мочеиспускания, Q ave — средняя скорость мочеиспускания
Note. Q max — maximum flow rate, Q ave — average flow rate
Результаты лечения. У всех 7 пациентов в ходе проведения уретроскопии в бульбозном отделе уретры были выявлены фибриновые скопления, которые практически полностью закрывали просвет уретры в данной зоне: в виде перепонки — у 5 пациентов, в виде множества тяжей — у 2 пациентов (рис. 8). При этом не отмечалось характерное для «классической» стриктуры кольцевидное сужение уретры в этой области, хотя указанные фибриновые перепонка и тяжи в незначительной степени натягивали стенку уретры. Фибриновые перепонки и тяжи имели тонкий слой и рыхлую структуру, что позволяло провести через них эндоурологический проводник (рис. 9). После этого плавным движением уретероскопа легко удалось у всех пациентов снять фибриновые сращения по всему периметру стенки уретры, так как они имели неплотный характер соединений со слизистой уретры (рис. 10). У ряда пациентов фибриновые перепонки / тяжи удавалось снимать одним движением эндоскопа в проксимальном направлении, а у части пациентов для снятия остатков фибриновых образований (рис. 11) приходилось после первого движения выдвигать эндоскоп в обратном направлении за пределы области локализации патологического процесса и затем повторно проводить инструмент в проксимальном направлении, то есть двумя-тремя движениями уретероскопа отделяли все части фибриновых скоплений от стенки уретры. Ни в одном наблюдении не проводили холодное либо лазерное рассечение фибриновых сращений или самой стенки уретры на этом участке, а при удалении фибриновых образований эндоскопом надрыва слизистой уретры не возникло. После освобождения от фибриновых сращений стенка уретры имела хорошую эластичность, что позволило свободно провести катетер Foley 18 Ch. Продолжительность манипуляции колебалась от 5 до 10 минут и составила в среднем 7,6 ± 1,7 минут.
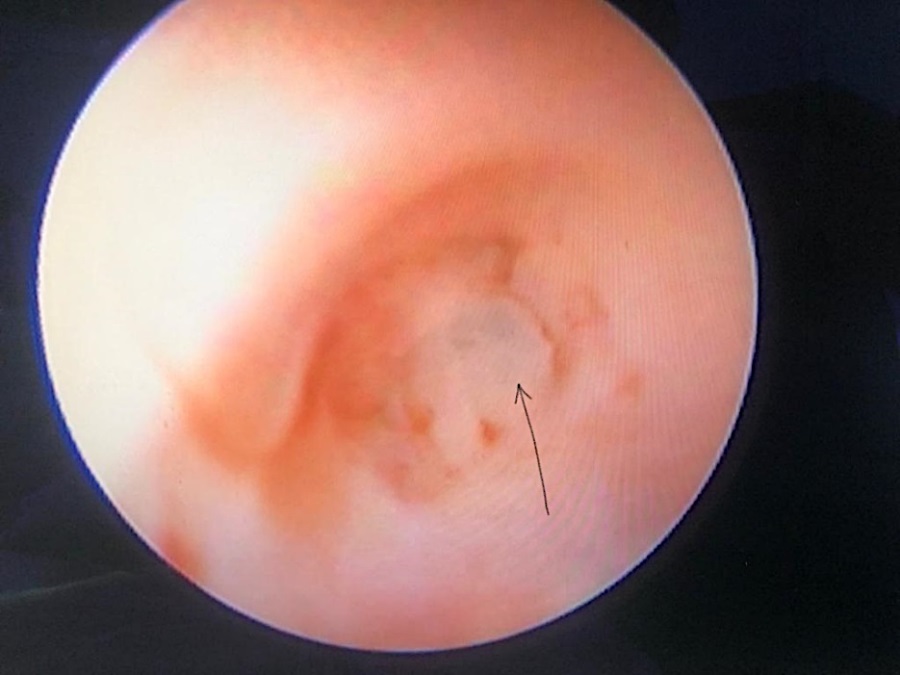
Рисунок 8. Фибриновая перепонка бульбозной уретры, по данным уретроскопии (указана стрелкой)
Figure 8. Urethroscopy view. Fibrin membrane in the bulbous urethra (indicated by an arrow)
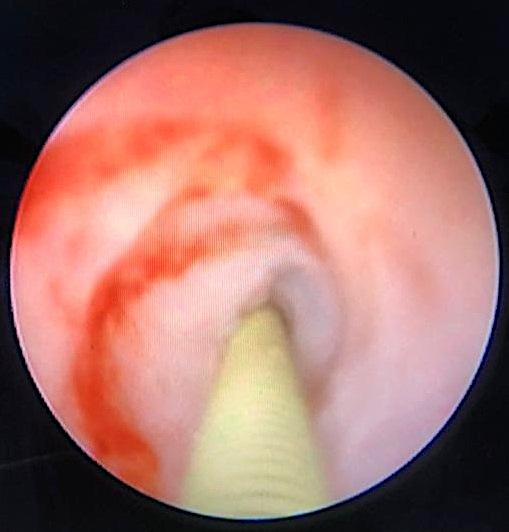
Рисунок 9. Проведение проводника Lunderquist через фибриновую перепонку
Figure 9. Urethroscopy view. Passing the Lunderquist guidewire through the fibrin membrane

Рисунок 10. Вид бульбозной уретры после удаления фибриновой перепонки
Figure 10. Urethroscopy view. Bulbous urethra after removal of the fibrin membrane

Рисунок 11. Частичное снятие фибриновой перепонки (стрелка указывает на сохранившуюся часть перепонки)
Figure 11. Urethroscopy view. Partial removal of the fibrin membrane (arrow indicates the remaining part of the membrane)
Сроки наблюдения пациентов после лечения варьировались от 8 до 24 месяцев при среднем значении 13,6 ± 5,3 месяцев. При этом у двух пациентов к настоящему времени не достигнуто 12 месяцев наблюдения, но с учётом небольшого объёма выборки пациентов было решено учитывать весь первоначальный опыт в этом направлении.
Каких-либо осложнений во время манипуляции или после неё, а также рецидива стриктуры уретры в виде наличия жалоб на затрудненное мочеиспускание за весь период наблюдения ни у одного пациента не отмечено. Следовательно, необходимости в проведении какого-либо оперативного вмешательства, в том числе методов дилатации уретры, ни в одном наблюдении не возникло. Таким образом, эффективность проведенного лечения составила 100% при нулевом уровне осложнений.
В целом по всей группе пациентов средние показатели Q max и Q ave после лечения оказались достоверно выше, чем данные до лечения (рис. 12 – 13). Данные урофлоуметрии по каждому пациенту показаны в таблице 2. С целью проведения статистических расчётов у пациентов с наличием цистостомы показатели Q max и Q ave до лечения отмечены как нулевые (отсутствие самостоятельного мочеиспускания), а значения Q max и Q ave после лечения у всех пациентов указаны по приведённому для каждого пациента максимальному сроку наблюдения. При этом только у двух пациентов (пациенты № 4 и № 7) значения Q max и Q ave после лечения не достигли референсных значений, хотя были выше величин до лечения. У пациента № 4 перед лечением вовсе отсутствовало самостоятельное мочеиспускание (была установлена цистостома), а после лечения достигнуто восстановление самостоятельного мочеиспускания с близкими к референсным значениям показателями Q max и Q ave. Пациент № 7 полностью был удовлетворен качеством мочеиспускания и не выражал жалоб на присутствие обструктивных симптомов нижних мочевых путей. С учётом данных аспектов, а также отсутствия применения дополнительных методов оперативного лечения эти два случая нами также был отнесены к категории успешных.
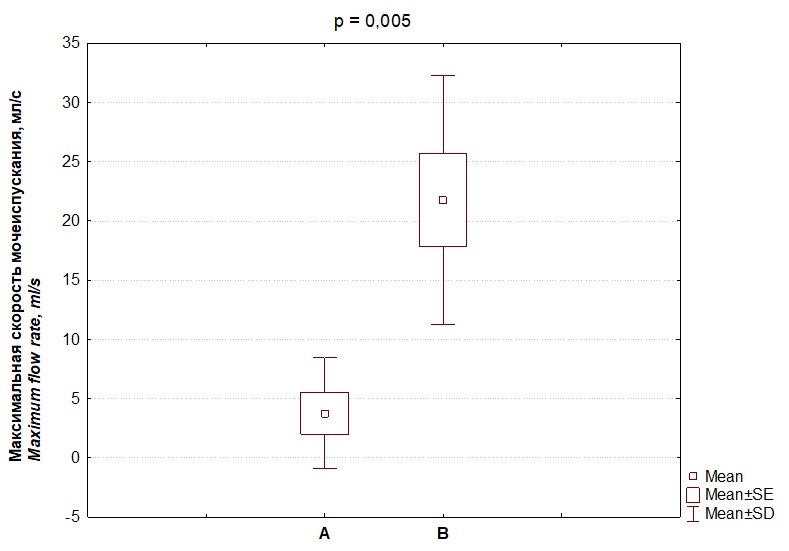
Рисунок 12. Максимальная скорость мочеиспускания: A – до лечения; B – после лечения
Figure 12. Maximum flow rate: A — before treatment; B — after treatment
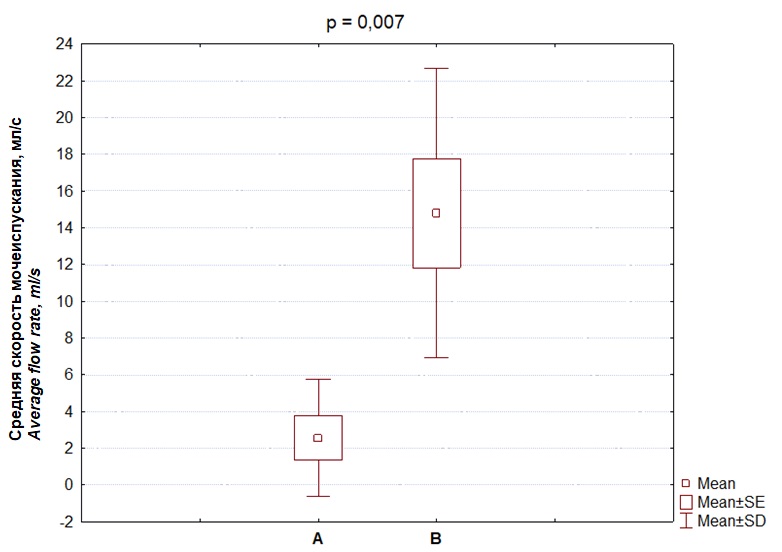
Рисунок 13. Средняя скорость мочеиспускания: A — до лечения; B — после лечения
Figure 13. Average flow rate: A — before treatment; B — after
Согласно уретрограммам, после лечения у всех пациентов также отмечена положительная динамика в виде расширения просвета уретры в зоне вмешательства по сравнению с состоянием уретры до лечения. Такие изменения по данным ретроградной уретрографии на примере одного из наших наблюдений продемонстрированы на рисунке 14.
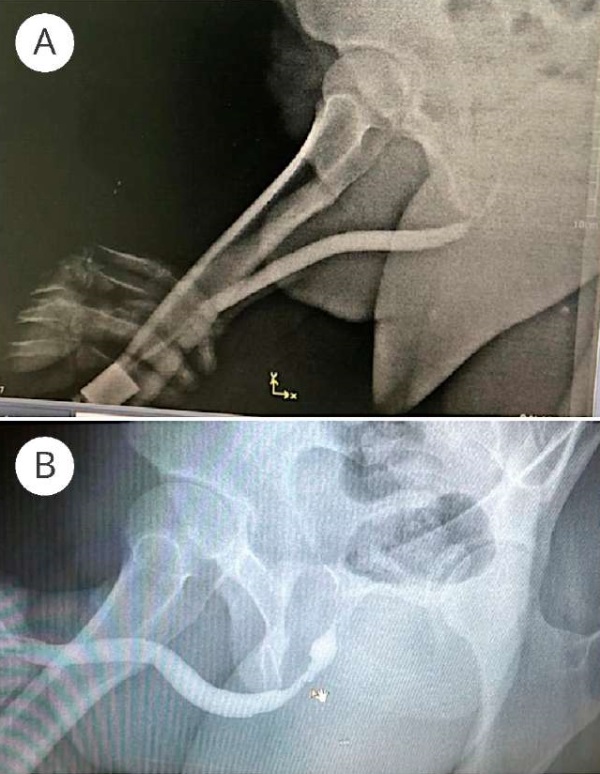
Рисунок 14. Уретрограмма пациента № 2: A — до лечения; B — после лечения
Figure 14. Urethrogram of patient No. 2: A — before treatment; B — after treatment
Обсуждение
Как уже было выше отмечено, российские и международные клинические рекомендации не требуют выполнения в обязательном порядке уретроскопии при стриктуре передней уретры [7 – 10]. Если исходить из клинических рекомендаций и не проводить уретроскопию всем пациентам со стриктурой уретры, можно пропустить важную информацию о характере стриктуры уретры, которую невозможно получить с помощью уретрографии. Поэтому выявленная в ходе уретроскопии информация имеет принципиальное значение и коренным образом влияет на выбор тактики лечения пациентов со стриктурой уретры. На примере представленной выборки пациентов показано, насколько выбор варианта лечения по результатам уретрографии может отличаться от ситуации, когда дополнительно проводится уретроскопия. Чтобы понять это различие, мы решили представить все уретрограммы до лечения, согласно которым большинству пациентов была бы предложена уретропластика. При этом следует подчеркнуть, что данная выборка пациентов не представляла собой специально отобранную группу, имеющую противопоказания к уретропластике. Выбранная тактика была обсуждена со всеми пациентами наряду с традиционными методами лечения, однако наши пациенты по тем или иным причинам выбрали именно такой путь лечения и наблюдения.
Тот факт, что наши выводы основаны на небольшом числе наблюдений (7 пациентов), не должен вызывать скептическое отношение или критические оценки. Малое число наблюдений в данном исследовании связано с тем, что ранее мы, руководствуясь требованиями клинических рекомендаций, решение о выборе объёма хирургического вмешательства принимали главным образом на основе данных уретрографии и зачастую обходились без уретроскопии. Когда всем без исключения пациентам была выполнена уретроскопия, удалось получить дополнительные данные об особенностях стриктуры уретры. Поэтому, предполагая, что после набора крупной выборки пациентов могут быть получены такие же закономерности, мы решили опубликовать наши первоначальные данные.
Предположения о существенных дополнительных возможностях эндоскопического исследования при диагностике стриктуры уретры получили подтверждение в работе, где отмечено, что данный метод позволяет оценить состояние уретры, в том числе эластичность стенок уретры, за пределами рентгенологически видимой стриктуры [11]. В ней было указано, что просвет уретры может быть узким (2–3 мм), но стенки могут быть растяжимы, то есть сохранять некоторую эластичность, и, напротив, при таком просвете стенки могут быть крайне жесткими [11]. Следовательно, эндоскопическая оценка зоны сужения уретры позволит более точно определить показания для применения каждого вида (открытого или малоинвазивного) оперативного вмешательства на основе определения истинной протяженности стриктуры и состояния стенок уретры. В противном случае при игнорировании возможностей уретроскопии значительно возрастают риски неудачи операции и рецидива заболевания. Если проводить уретропластику только на основе данных уретрографии без выполнения уретроскопии, то можно не диагностировать присутствие фибриновых сращений во время оперативного вмешательства. При подведении катетера либо бужа к месту предполагаемого сужения уретры происходит отсоединение фибриновых скоплений от стенки уретры за счёт давления катетером или бужом, в результате чего теряется ориентир по определению локализации сужения уретры и возникают трудности с точностью выбора места разреза стриктуры уретры, поэтому может быть нанесена избыточная операционная травма стенке уретры, что, безусловно, негативно отразится на результатах операции. С другой стороны, выявление «жёсткого» (истинного) характера сужения просвета уретры с помощью уретроскопии означает наличие спонгиофиброза и / или обширного поражения слизистой, что определяет бесперспективность внутренней холодной или лазерной уретротомии, так как рассечение рубцовой ткани провоцирует развитие ещё более грубого рубцового процесса [3][12]. Тем самым на основе данных уретроскопии может быть обоснована приоритетность уретропластики и отказ от эндоскопических методов лечения стриктуры уретры.
На основе своих наблюдений мы предполагаем, что в определенных случаях развития стриктуры уретры имеет место присутствие поверхностных воспалительных изменений слизистой уретры, в результате которых в просвете уретры в избыточном количестве накапливается фибрин, выполняя просвет уретры и плотно фиксируясь на слизистой уретры, тем самым закрывая тотально или субтотально просвет уретры. Возможно, это первоначальная фаза формирования стриктуры уретры. Патогенез данного феномена предстоит выяснить в ходе дальнейших научных работ. Такое скопление фибрина нарушает уродинамику в нижних мочевых путях, вызывая характерные для стриктуры уретры обструктивные симптомы, а также препятствует полноценному перемещению контрастного вещества при выполнении уретрографии, создавая ложную картину присутствия стриктуры уретры на уретрограммах. Только путём проведения уретроскопии можно выявить и дифференцировать подобные изменения в уретре. В подтверждение данного тезиса мы приводим результаты ещё одного наблюдения, которое не вошло в вышеуказанную группу из 7 пациентов. Этому пациенту перед уретроскопией были выполнены ретроградная уретрография и статическая магнитно-резонансная томография уретры по нашей методике [13], на которых были выявлены признаки сужения уретры в бульбозном отделе, однако, по данным магнитно-резонансной томографии, не были установлены характерные для спонгиофиброза изменения (рис. 15). У данного пациента при проведении уретроскопии отмечено отсутствие истинного сужения уретры и наличие только лишь фибриновой пленки, которая была удалена по вышеуказанной технике.
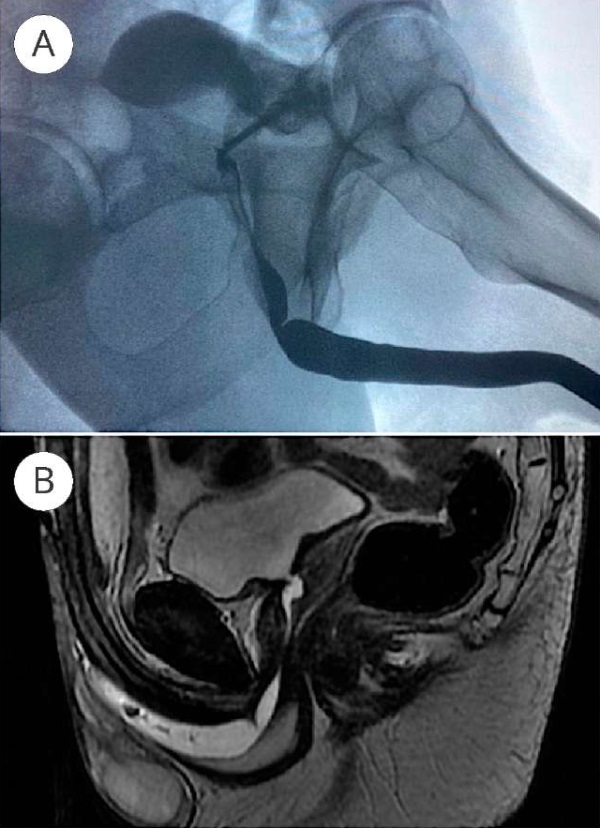
Рисунок 15. Стриктура бульбозной уретры: A — уретрограмма; B — МРТ-скан
Figure 15. Stricture of bulbous urethra: A — urethrogram; B — MRI-scan
Кроме того, нам хотелось бы обратить внимание ещё на один важный аспект при интерпретации наших результатов. Он касается того, что наш подход может быть отднесен к дилатирующим уретру методам (бужированию уретры) либо к внутренней оптической / лазерной уретротомии или приравнен к ним. Наш метод имеет принципиальные отличия от этих указанных вариантов лечения стриктуры уретры, поэтому представляется некорректным отождествление его с ними. Дилатирующие методы подразумевают растяжение, а внутренняя уретротомия — рассечение рубцовых тканей для обеспечения временного расширения просвета уретры. Так как оба метода не устраняют полностью рубцовые изменения, их эффект носит временный и паллиативный характер. В отличие от них предложенный нами подход применяется при отсутствии грубых рубцовых изменений в стенке уретры и позволяет полностью устранить существующие поверхностные изменения, тем самым избавляя пациента от клинических проявлений заболевания, что даёт основание считать этот метод патогенетически обоснованным и вполне радикальным для данной категории пациентов. Это означает, что уретроскопия является не только методом визуализации и оценки стриктур уретры, но и может быть частью минимально-инвазивного «терапевтического» лечения, когда мы, возможно, выявляем стриктуру уретры не в привычном понимании, а в фазе первичных пролиферативных изменений слизистой. Поэтому считаем крайне важной идентификацию пациентов с такими поверхностными изменениями уретры, которые могут выявлены и корректированы с помощью уретроскопии.
Таким образом, все отмеченные выше аргументы свидетельствуют о том, что на предоперационном этапе надо активно использовать возможности уретроскопии наравне с другими методами диагностики. Данная стратегия, возможно, позволит дифференцировать различные категории пациентов со стриктурой уретры и оптимизировать выбор тактики лечения у них. Безусловно, мы понимаем, что наша гипотеза в определенной степени идет вразрез с существующими клиническими рекомендациями и традиционными подходами к ведению пациентов со стриктурой уретры. Поэтому мы не рассматриваем свой опыт как предписание к действию и только выносим предложенную тактику на обсуждение профессионального сообщества. В связи с этим выражаем надежду, что получим обратную связь от коллег после оценки возможностей нашей методики, так как она легко воспроизводима и несложна для реализации в своей практике.
Ограничения исследования. Малый размер выборки пациентов, короткие сроки наблюдения после лечения, отсутствие контрольной группы пациентов для сравнения результатов предложенного подхода, отсутствие четкого обоснования по выбору сроков установления уретрального катетера при данном подходе к лечению.
Заключение
Проведение уретроскопии у всех пациентов со стриктурой уретры позволяет выявить случаи заболевания, когда развитие рубцового процесса в стенке уретры носит поверхностный характер, что может быть корригировано без проведения уретропластики либо других методов лечения. В связи с этим целесообразным представляется рассмотрение вопроса о включении уретроскопии в обязательные, а не дополнительные методы обследования пациентов со стриктурой уретры. Такой подход к использованию уретроскопии будет способствовать выбору оптимальной тактики лечения и снижению рисков рецидива данного заболевания. Однако с учётом небольшого числа наблюдений и отсутствия контрольной группы пациентов для оценки эффективности предложенного подхода выдвинутая гипотеза нуждается в дальнейшем изучении.
Ключевые моменты. Предложен новый подход к оценке патологических изменений в уретре и выбору тактики лечения при коротких стриктурах бульбозной уретры. Данное исследование указывает на необходимость переоценки диагностических возможностей уретроскопии при стриктуре уретры и возможность оптимизации результатов лечения пациентов со стриктурой бульбозной уретры на основе использования уретроскопии. Метод легко воспроизводим, что даёт возможность широкого внедрения в клиническую практику различных лечебных учреждений.
Список литературы
1. Alwaal A, Blaschko SD, McAninch JW, Breyer BN. Epidemiology of urethral strictures. Transl Androl Urol. 2014;3(2):209-213. DOI: 10.3978/j.issn.2223-4683.2014.04.07
2. Wood DN, Andrich DE, Greenwell TJ, Mundy AR. Standing the test of time: the long-term results of urethroplasty. World J Urol. 2006;24(3):250-254. DOI: 10.1007/s00345-006-0057-3
3. Коган М.И., Митусов В.В., Красулин В.В., Шангичев А.В., Глухов В.П., Аметов Р.Э., Митусова Е.В. Внутренняя оптическая уретротомия при стриктурной болезни уретры усложняет последующую реконструктивную операцию. Урология. 2012;(3):27-30. eLIBRARY ID: 18065089; EDN: PFIHBD
4. Santucci R, Eisenberg L. Urethrotomy has a much lower success rate than previously reported. J Urol. 2010;183(5):1859-1862. DOI: 10.1016/j.juro.2010.01.020
5. Naudé AM, Heyns CF. What is the place of internal urethrotomy in the treatment of urethral stricture disease? Nat Clin Pract Urol. 2005;2(11):538-545. DOI: 10.1038/ncpuro0320
6. Benson CR, Goldfarb R, Kirk P, Qin Y, Borza T, Skolarus TA, B Brandes S. Population Analysis of Male Urethral Stricture Management and Urethroplasty Success in the United States. Urology. 2019;123:258-264. DOI: 10.1016/j.urology.2018.06.059
7. Клинические рекомендации. Стриктура уретры. 2021. Ссылка активна на 05.10.2024. URL: https://cr.minzdrav.gov.ru/schema/651_1.
8. Campos-Juanatey F, Osman NI, Greenwell T, Martins FE, Riechardt S, Waterloos M, Barratt R, Chan G, Esperto F, Ploumidis A, Verla W, Dimitropoulos K, Lumen N. European Association of Urology Guidelines on Urethral Stricture Disease (Part 2): Diagnosis, Perioperative Management, and Follow-up in Males. Eur Urol. 2021;80(2):201-212. DOI: 10.1016/j.eururo.2021.05.032
9. Wessells H, Morey A, Souter L, Rahimi L, Vanni A. Urethral Stricture Disease Guideline Amendment (2023). J Urol. 2023;210(1):64-71. DOI: 10.1097/JU.0000000000003482
10. Abbasi B, Shaw NM, Lui JL, Li KD, Low P, Hakam N, Nabavizadeh B, Breyer BN. Comparative review of the guidelines for anterior urethral stricture. World J Urol. 2022;40(8):1971-1980. DOI: 10.1007/s00345-022-03988-3
11. Коган М.И. Комментарии к новым поправкам (2023) в рекомендации Американской урологической ассоциации по стриктурной болезни уретры. Вестник урологии. 2023;11(3):5-9. DOI: 10.21886/2308-6424-2023-11-3-5-9
12. Пушкарь Д.Ю., Живов А.В., Лоран О.Б., Карпович А.В., Багаудинов М.Р., Исмаилов М.Р. Сравнительная частота и факторы риска рецидива стриктуры уретры при различных методах оперативного лечения. Андрология и генитальная хирургия. 2012;13(4):37-44. eLIBRARY ID: 18437830; EDN: PNMIZB
13. Богданов А.Б., Катибов М.И., Велиев Е.И., Монаков Д.М., Гончарук Д.А., Ахвердиева Г.И., Полякова А.С., Варданян В.А. Статическая МРТ в диагностике стриктур бульбозной уретры и оценке степени спонгиофиброза. Вестник урологии. 2023;11(2):5-17.
Об авторах
М. И. КатибовРоссия
Магомед Исламбегович Катибов — д-р мед. наук, доцент.
Махачкала
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
А. Б. Богданов
Россия
Андрей Борисович Богданов — канд. мед. наук.
Москва
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
О. Б. Лоран
Россия
Олег Борисович Лоран —д-р мед. наук, профессор, заслуженный деятель науки РФ, акад. РАН.
Москва
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
Рецензия
Для цитирования:
Катибов М.И., Богданов А.Б., Лоран О.Б. Собственный взгляд на роль уретроскопии в диагностике и выборе тактики лечения при коротких стриктурах бульбозной уретры. Вестник урологии. 2025;13(3):39-51. https://doi.org/10.21886/2308-6424-2025-13-3-39-51
For citation:
Katibov M.I., Bogdanov A.B., Loran O.B. Personal perspective on the role of urethroscopy in the diagnosis and treatment strategy selection for short strictures of the bulbar urethra. Urology Herald. 2025;13(3):39-51. (In Russ.) https://doi.org/10.21886/2308-6424-2025-13-3-39-51













































