Перейти к:
Существует ли целесообразность фармакотерапевтической подготовки слизистой полости рта к аугментационной уретропластике?
https://doi.org/10.21886/2308-6424-2020-8-3-38-46
Аннотация
Введение. Аугментационная уретропластика с использованием буккальной слизистой в настоящее время является оптимальным методом лечения протяженных стриктур уретры. Тем не менее, данная хирургия сопряжена с довольно высокой частотой рецидивов и осложнений. Одной из причин, что может определять успех или негативных исход операции является морфологическая структура трансплантата, что требует более углубленных исследований.
Цель исследования. Оценить исходное морфологическое состояние буккальной слизистой у мужчин и определить целесообразность ее фармакотерапевтической подготовки, как предиктора улучшения качества приживления аутотрансплантата при аугментационной уретропластике.
Материалы и методы. У 20 пациентов с протяженными стриктурами спонгиозной уретры изучена морфологическая структура фрагментов буккальной слизистой. Объектами морфологического исследования являлись: интактная слизистая оболочка полости рта перед аугментационной уретропластики (1 биопсия) и фрагменты слизистой после 7 дневной обработки полости рта раствором антисептика «Листерин» (2 биопсия). Биопсийный материал исследовали микроскопически при стандартных окрасках (гематоксилин-эозин) и иммуногистохимическими методиками.
Результаты. Исходная гистоструктура буккальной слизистой у каждого третьего больного сопровождалась воспалительной инфильтрацией на уровне субэпителиального слоя с десквамацией эпителия. после недельной обработки полости рта антисептиком гистологически и иммуногистохимически доказано выраженное увеличение и усиление межклеточных контактов в трансплантатах, характеризующееся выраженной экспрессией антитела во всей толщине эпителиального пласта. при этом происходит «самоорганизация» подслизистой основы за счет снижения отёка, усиления межклеточных и фокальных адгезионных контактов, с усилением компонентов сосудистого русла и количеством сосудистых «почек».
Выводы. Таким образом, недельная предоперационная обработка полости рта позволяет купировать повреждения покровного эпителия и воспалительную инфильтрацию в подслизистой основе с улучшением ее васкуляризации, что может быть расценено как положительный фактор для последующего приживления трансплантата.
Ключевые слова
Для цитирования:
Митусов В.В., Воронова О.В., Коган М.И., Мирзаев З.А., Глухов В.П., Амирбеков Б.Г. Существует ли целесообразность фармакотерапевтической подготовки слизистой полости рта к аугментационной уретропластике? Вестник урологии. 2020;8(3):38-46. https://doi.org/10.21886/2308-6424-2020-8-3-38-46
For citation:
Mitusov V.V., Voronova O.V., Kogan M.I., Mirzaev Z.A., Glukhov V.P., Amirbekov B.G. Is there a feasibility of pharmacotherapeutic preparation of the oral mucosa for augmentation urethroplasty? Urology Herald. 2020;8(3):38-46. (In Russ.) https://doi.org/10.21886/2308-6424-2020-8-3-38-46
Введение
Клиническая статистика последних 3-х десятилетий отмечает существенный рост числа протяженных стриктур и облитераций передней уретры (СУ), чему есть абсолютно доказанные объективные причины [1][2]. Следствием этого, в структуре методов хирургии СУ значительно увеличилось количество выполняемых аугментационных уретропластик (АУП) с использованием тканевых лоскутов и трансплантатов [3][4][5][6].
Современная реконструкция уретры предполагает 3 вида размещения трансплантата с целью аугментации органа: вентральное, дорсо-латеральное или дорзальное. А в качестве наилучшего трансплантата (графта) признается слизистая оболочка ротовой полости, изъятая со щеки, нижней губы или подъязычной области пациента [7][8][9].
Показатель успешности различных техник АУП составляет 75 - 92%, а конкретный выбор методики является правом выбора оперирующего хирурга [10][11][12].
Несмотря на относительно высокий уровень успешности АУП, изучение отдаленных результатов (после 6 месяцев с момента операции) выявляет осложнения в 19 - 23% случаев, основными из которых являются: сужения в зонах проксимального (56 - 59%) и дистального (20 - 28%) анастомозов; 9 - 19% — контрактуры трансплантата, мочевые свищи (4 - 6%), а также дриблинг после мочеиспускания и эректильная дисфункция [13][14][15][16][17].
Двумя основными причинами осложнений являются: прогрессия спонгиофиброза в нативной уретре после операции и исходное «качество» самого трансплантата, о чем свидетельствует ряд публикаций в последние годы [18][19][20]. Но как следует отметить, состояние графта перед трансплантацией практически не изучено, в частности его морфологическая структура.
Цель исследования: оценить исходное морфологическое состояние буккальной слизистой у мужчин, подлежащих оперативному лечению протяженных СУ и определить целесообразность её фармакотерапевтической подготовки для повышения качества приживления к операционному ложу.
Материалы и методы
Основу проспективного исследования составило гистологическое и иммуногистохимическое изучение буккальной слизистой у 20 больных с протяжёнными стриктурами уретры в возрасте 23 - 69 лет (медиана — 39 лет), которым предстояло выполнить аугментационную уретропластику.
Биопсийные фрагменты слизистой оболочки у каждого из больных изучены дважды:
- 1 биопсия — с целью оценки исходного состояния;
- 2 биопсия — с целью оценки терапевтического эффекта 7 дневной обработки полости рта раствором антисептика «Листерин» 3 раза в сутки, которую выполняли в ходе выполнения операции АУП. Антисептик был выбран согласно рекомендациям стоматологической ассоциации России1 и авторами других исследований в области стоматологии [21].
Техника 1-й биопсии. Под местной анестезией 1% раствором лидокаина производили «захват» фрагмента слизистой оболочки полости рта щипцами Blakesley с прямой браншей. Отсечение ткани, оказавшейся в браншах осуществляли скальпелем вокруг инструмента, получая таким образом фрагмент размером 3 х 3 мм. Биопсию проводили со стороны противоположной забору донорского фрагмент слизистой для АУП.
Техника 2-й биопсии. В ходе заготовки трансплантата при проведении АУп в одном из его краев иссекали фрагмент (3 х 3 мм) для сравнения морфологического состояния с первично взятым биоптатом слизистой.
Из биопсийных материалов изготавливали гистологические срезы толщиной 3 - 4 микрона, с последующей их окраской гематоксилин-эозином.
Иммуногистохимические исследования проводили на иммуногистостейлере LEICA BOND- MAX (Gemany) с использованием оригинальных антител cD34 клон QBEnd/10 фирмы Leica Bond; Gemany (ready to use) - для оценки степени васкуляризации подслизистой основы и E-Cadherin'a 36B5 фирмы Leica Bond; Gemany (ready to use) — для изучения клеточной адгезии в эпителиальном пласте слизистой оболочки ротовой полости. Характер воспалительных инфильтратов определяли с помощью антител CD3 клон LN10 фирмы Leica Bond; Gemany (ready to use).
Верификацию полученных результатов осуществляли с помощью светового микроскопа "LEICA DM4000B" (Германия) и увеличением: х 100, х 200, х 400.
Результаты
Исходно во всех случаях буккальная слизистая представлена рыхлым слоем многослойного плоского неороговевающего эпителия с фокальной или субтотальной десквамацией эпителиоцитов и межклеточным отёком разной степени выраженности. В ядрах эпителиоцитов имеет место сморщивание и гиперхромазия, кариорексис, апоптотические тельца, а также набухание и вакуолизация цитоплазмы в промежуточном и поверхностном слоях (рис. 1).
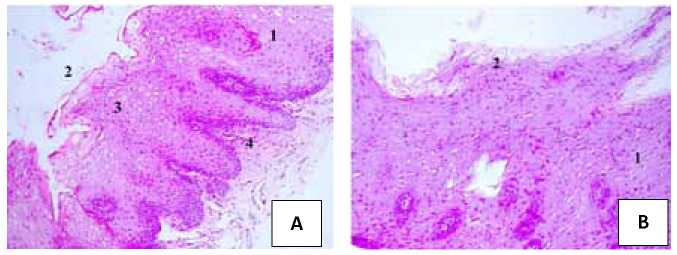
Рисунок 1. Эпителий слизистой оболочки полости рта: 1 — многослойный плоский неороговевающий эпителий; 2 — участки десквамации; 3 — дегенеративные изменения эпителиоцитов; 4 — воспалительная инфильтрация (лимфоциты, плазмоциты, гистиоциты). Окраска: Гематоксилин-эозин. Увеличение: А − х 200; Б − х 400
Figure 1. The epithelium of the mucous membrane of the oral cavity: 1 — multilayer flat non-corneal epithelium; 2 — areas of desquamation; 3 — degenerative changes of epithelial cell; 4 — inflammatory infiltration (lymphocytes, plasmocytes, histiocytes). Staining: Hematoxylin-eosin. Magn.: A − x 200; B − x 400
В подслизистой основе визуализируется рыхлая структура коллагенового каркаса с преимущественно дискретно расположенными воспалительными инфильтратами. Определяется обилие разнокалиберных сосудов, в большей степени щелевидных за счёт отёка стромы, с неравномерной, местами уплощенной, а местами гиперплазированной эндотелиальной выстилкой. Отмечается формирование сосудистых почек, фокусов разволокнения и дистрофии коллагенового каркаса стромы (рис. 2).

Рисунок 2. Субэпителиальный пласт слизистой оболочки полости рта: 1 — воспалительная инфильтрация (лимфоциты, плазмоциты, гистиоциты); 2 — отёк подслизистой основы; 3 — участки субэпителиального фиброза. Окраска: Гематоксилин-эозин. Увеличение: А — х 100; Б — х 400
Figure 2. The epithelial layer of the mucous membrane of the oral cavity: 1 — inflammatory infiltration (lymphocytes, plasmocytes, histiocytes); 2 — oedema of the submucosa; 3 — the subepithelial areas of fibrosis. Staining: Hematoxylin-eosin. Magn.: A – x 100; B – x 400
В трети случаев выявлено наличие множественных обширных воспалительных инфильтратов с локализацией их непосредственно под базальным слоем эпителиального пласта.
После недельной фармакотерапии эпителиальный пласт имеет четкий верхний (свободный) контур с отсутствием десквамации покровного эпителия, уплотнением клеток поверхностного слоя по типу коагуляционного метаморфоза. Эпителиоциты располагаются компактно между собой на всем протяжении, с отсутствием межклеточного отёка, вакуолизации и воспалительной инфильтрации. Ядра клеток в них на большем протяжении пикнотичны, цитоплазма плотная, эозинофильная, что представлено на рисунке 3.

Рисунок 3. Эпителий слизистой оболочки полости рта после 7 дневного применения антисептика: 1 — многослойный плоский неороговевающий эпителий (ровный контур); 2, 3 — гиперплазия базального и промежуточных слоёв. Окраска: Гематоксилин-эозин. Увеличение: А − х 200; Б − х 400
Figure 3. Epithelium of the oral mucosa after 7 days of antiseptic usage: 1 — multilayer flat non-corneal epithelium (smooth contour); 2, 3 — hyperplasia of the basal and intermediate layers. Stainig: Hematoxylin-eosin. Magn.: A – x 200; B – x 400
Качественное «улучшение» структуры эпителия скорее всего связано с изменениями подслизистой основы, где отсутствовали лимфогистиоцитарные инфильтраты и отёк, а соединительнотканная строма представлена компактно расположенными эластическими и коллагеновыми волокнами, обилием разнокалиберных четко визуализируемых сосудов с большим количеством капилляров и сосудистых почек (рис. 4).

Рисунок 4. Субэпителиальный пласт слизистой оболочки полости рта после 7 дневного применения антисептика: 1 — обилие капилляров и неоангиогенез; 2 — отсутствие отёка. Окраска: Гематоксилин-эозин. Увеличение: А – х 100; Б – х 400
Figure 4. Subepithelial layer of the oral mucosa after 7 days of antiseptic usage: 1 — abundance of capillaries and neoangiogenesis; 2 — no oedema. Stainig: Hematoxylin-eosin. Magn.: A – x 100; B – x 400
В полной мере результаты гистологической картины соотносятся с результатами гистохимических исследований. Так, изначально в субэпителиальном слое, выявляется неравномерная пролиферация эндотелия капилляров с набуханием клеток и потерей межклеточных связей, что коррелирует со слабо выраженной экспрессией Е-кадгерина в эпителиоцитах, а также с тенденцией ее снижения, вплоть до полной потери в поверхностных отделах эпителиального пласта, что свидетельствует об ослаблении и даже потере межклеточных контактов.
Исходно отмечается выраженная диффузная экспрессия E-catherin'a на клеточных мембранах, имеющая равномерное яркое распределение по всей толщине эпителиального пласта слизистой оболочки, что определено нами как выраженная мембранная реакция, демонстрирующая плотные межклеточные контакты.
После фармакотерапии при ИГХ исследовании с антителами против СД34 в подслизистом слое четко выявлена равномерная пролиферация эндотелия по всей окружности артериол и венул с наличием плотных межэндотелиальных контактов. Определена качественная иммуноэкспрессия клона LN10 СД3 в единичных дискретно расположенных реактивных Т-лимфоцитах на фоне отсутствия воспалительных инфильтратов (рис. 5-7).
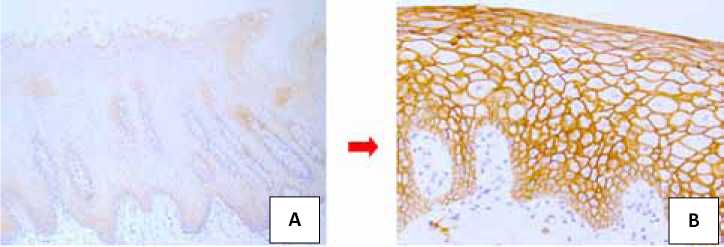
Рисунок 5. ИГХ реакция с антителами к Е-катгерину в исходной слизистой оболочке полости рта (А) и после фармакотерапии (Б). Увеличение: х 200
Figure 5. Immunohistochemical reaction with antibodies to E-cadherin in the initial mucosa of the oral cavity (A) and after pharmacotherapy (B). Magn.: x 200
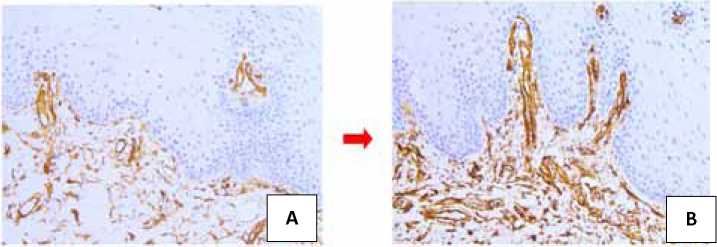
Рисунок 6. ИГХ реакция с антителами к CD34 в исходной слизистой оболочке полости рта (А) и после фармакотерапии (Б). Увеличение: х 200
Figure 6. Immunohistochemical reaction with CD34-antibodies in the intact mucosa of the oral cavity (A) and after pharmacotherapy (B). Magn.: x 200
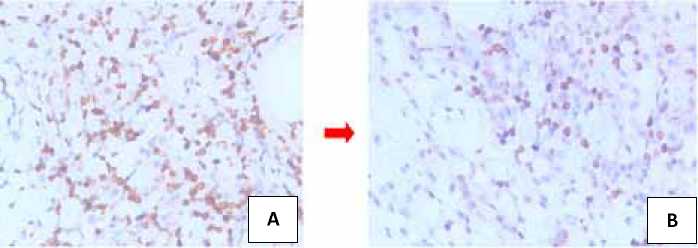
Рисунок 7. ИГХ реакция с антителами к CD3 в исходной слизистой оболочке полости рта (А) и после фармакотерапии (Б). Увеличение: х400
Figure 7. Immunohistochemical reaction with CD3-antibodies in the initial mucosa of the oral cavity (A) and after pharmacotherapy (B). Magn.: x400
Обсуждение
На протяжении многих лет реконструкция сужений и облитераций уретры остается сложной урологической проблемой. И если вопрос с лечением коротких СУ практически решен за счет эндоскопических вмешательств и резекционной хирургии, то лечение протяженных стриктур уретры, число которых растет год от года, особенно в развитых странах, остается крайне трудной хирургией [2][3][7][11].
«Золотым стандартом» хирургического лечения таких состояний в настоящее время являются аугментационная и заместительная уретропластики. В настоящее время лучшей из донорских тканей признано использование фрагментов слизистой оболочки полости рта различных локализаций [8][9][10][12].
В исследованиях было показано, что слизистая оболочка рта хорошо «приживляется» в зонах аугментации уретры и на протяжении длительного времени сохраняет свою исходную морфологическую структуру [9][18][20].
Рецидивы сужений мочеиспускательного канала, обусловленные как контрактурами самого трансплантата, сужениями в анастомотических зонах аугментации, образование свищей и др., в качестве причины имеют фиброз на уровне подслизистого слоя трансплантата и уретры и вакуолярную дегенерация самого трансплантата, что ранее было изучено, при этом предполагается, что в основе данного вида осложнений могут лежать различные исходные морфологические характеристики слизистой оболочки полости рта [13][19][20].
Поставив перед собой задачу изучить данный вопрос, нами была гистологически изучена исходная структура слизистой оболочки полости рта и её трансформация после 7-и дневного орошения полости рта больными антисептиком «Листерин».
Изучение нами исходной гистоструктуры буккальной слизистой показало, что участки с воспалительными инфильтратами на уровне субэпителиального слоя с элементами десквамации эпителиоцитов выявляются у каждого третьего пациента, что, по нашему мнению, следует считать неблагоприятным фоном при последующем использовании ее в качестве трансплантата.
После недельной фармакотерапии полости рта антисептиком «Листерин» гистологические и иммуногистохимические исследования слизистой оболочки показали выраженное увеличение и усиление межклеточных контактов в ее эпителиальном компоненте, характеризующееся выраженной экспрессией Е-кадгерина во всей толщине эпителиального пласта. Кроме того, произошла «самоорганизация» подслизистой основы за счет снижения отёка, усиления межклеточных и фокальных адгезионных контактов, что прослеживается в увеличении и четкой визуализации компонентов сосудистого русла с наличием большого количества сосудистых почек, что может быть расценено как положительный фактор для приживления трансплантата.
Заключение
У пациентов с протяжёнными СУ, где как метод лечения выбрана аугментационная уретропластика с использованием буккального трансплантата, целесообразно перед операцией в течение 7 дней осуществлять орошение полости рта антисептиком «Листерин», что позволяет купировать повреждения покровного эпителия и воспалительную инфильтрацию в подслизистой основе с улучшением её васкуляризации, что потенциально способно минимизировать риски неудачного приживления аутотрансплантата.
1. Постановления Совета Ассоциации общественных объединений «Стоматологическая ассоциация России» от 22 апреля 2014 года, г. Москва.
Список литературы
1. Stein DM, Thum DJ, Barbagli G, Kulkarni S, Sansalone S, Pardeshi A, Gonzalez CM. A geographic analysis of male urethral stricture aetiology and location. BJU Int. 2013;112(6):830-834. DOI: 10.1111/j.1464-410X.2012.11600.x
2. синельников Л.М., протощак В.В., Шестаев А.Ю., Кар-пущенко Е.Г., Янцев А.А. стриктура уретры: современное состояние проблемы (обзор литературы) Экспериментальная и клиническая урология. 2016;(2):80-87. eLIBRARY ID: 29899545
3. Коган М.И., Митусов В.В., Аметов Р.Э. Эффективность хирургического лечения протяжённых и многофокусных стриктур уретры у мужчин (Клинико-статистический анализ). Вестник урологии. 2013;(1):46-53. DOI: 10.21886/2308-6424-2013-0-1-46-53
4. Browne BM, Vanni Aj. Use of alternative Techniques and Grafts in Urethroplasty. Urol Clin North Am. 2017;44(1):127-140. DOI: 10.1016/j.ucl.2016.08.003
5. Horiguchi A. Substitution urethroplasty using oral mucosa graft for male anterior urethral stricture disease: current topics and reviews. Int J Urol. 2017;24(7):493-503. DOI: 10.1111/iju.13356
6. Levy ME, Elliott SP. Graft Use in Bulbar Urethroplasty. Urol Clin North Am. 2017;44(1):39-47. DOI: 10.1016/j.ucl.2016.08.009
7. Hillary CJ, Osman NI, Chapple CR. Current trends in urethral stricture management. Asian J Urol. 2014;1(1):46-54. DOI: 10.1016/j.ajur.2015.04.005
8. Barbagli G, Balo S, Montorsi F, Sansalone S, Lazzeri M. History and evolution of the use of oral mucosa for urethral reconstruction. Asian J Urol. 2017;4(2):96-101. DOI: 10.1016/j.ajur.2016.05.006
9. Коган М.И., Дементьева И.Ю., Митусов В.В., Глухов В.П., Красулин В.В., Сизякин Д.В., Ильяш А.В. Гистопатологическая оценка эволюции трансплантатов слизистой оболочки ротовой полости, используемых для аугментационной уретропластики. Урология. 2018;(5):64-68. DOI: 10.18565/urology.2018.5.64-68
10. Pathak HR, Jain TP, Bhujbal SA, Meshram KR, Gadekar C, Parab S. Does site of buccal mucosa graft for bulbar urethra stricture affect outcome? A comparative analysis of ventral, dorso-lateral and dorsal buccal mucosa graft augmentation urethroplasty. Turk J Urol. 2017;43(3):350-354. DOI: 10.5152/tud.2017.30771
11. Коган М.И., Глухов В.П., Митусов В.В., Красулин В.В., Ильяш А.В. Сравнительный анализ одно-и двухэтапной аугментационной дорсальной INLAY-пластики буккаль-ным графтом протяжённых стриктур спонгиозной уретры. Урология. 2018;(1):84-91. DOI: dx.doi.org/10.18565/urology.2018.1.84-90
12. Поляков Н.В., Кешишев Н.Г., Казаченко А.В., Трофимчук А.Д., Чернышев И.В., Даренков С.П., Аполихин О.И. Оценка эффективности методов буккальной уретропластики при стриктурах мочеиспускательного канала у мужчин. (Обзор литературы). Экспериментальная и клиническая урология. 2019;(4):99-106. DOI: 10.29188/2222-8543-2019-11-4-106-113
13. Robine E, Rigaud J, Luyckx F, Le Clerc QC, Madec FX, Bouchot O, Branchereau J. Analyse des taux de succes des uretroplas-ties pour stenoses de l'uretre bulbaire chez I'homme adulte : revue systematique de la litterature [Analysis of success rates of uretroplasty for adult male bulbar urethral stricture: A systematic review]. Prog Urol. 2017;27(2):49-57. DOI: 10.1016/j.purol.2016.12.003
14. Liu JS, Dong C, Gonzalez CM. Risk Factors and Timing of Early Stricture Recurrence After Urethroplasty. Urology. 2016;95:202-207. DOI: 10.1016/j.urology.2016.04.033
15. Javali TD, Katti A, NagarajHK. Management of recurrent anterior urethral strictures following buccal mucosal grafturethroplasty: A single center experience. Urol Ann. 2016;8(1):31-35. DOI: 10.4103/0974-7796.162217
16. Spilotros M, Sihra N, Malde S, Pakzad MH, Hamid R, Ockrim JL, Greenwell TJ. Buccal mucosal graft urethroplasty in men-risk factors for recurrence and complications: a third referral centre experience in anterior urethroplasty using buccal mucosal graft. Transl Androl Urol. 2017;6(3):510-516. DOI: 10.21037/tau.2017.03.69
17. Selim M, Salem S, Elsherif E, Badawy A, Elshazely M, Gawish M. Outcome of staged buccal mucosal graft for repair of long segment anterior urethral stricture. BMC Urol. 2019;19(1):38. DOI: 10.1186/s12894-019-0466-4
18. Soave A, Steurer S, Dahlem R, Rink M, Reiss P, Fisch M, Engel O. Histopathological characteristics of buccal mucosa transplants in humans after engraftment to the urethra: a prospective study. J Urol. 2014;192(6):1725-1729. DOI: 10.1016/j.juro.2014.06.089
19. Cavalcanti AG, Restrepo CF, Simoes M, Costa WS, Sampaio FJB, de Souza DB. What Is the Best Way to Prepare A Buccal Mucosa Graft for Urethroplasty? A Histology-Based Preliminary Report. Urol Int. 2018;100(4):397-401. DOI: 10.1159/000488805
20. Bhattar R, Yadav SS, Tomar V. Histopathological changes in oral mucosa in cases of failed augmented urethroplasty. Turk J Urol. 2019;45(3):206-211. DOI: 10.5152/tud.2019.67435
21. Alsarhan M, Alnofaie H, Ateeq R, Almahdy A. The Effect of Chlorhexidine and Listerine® Mouthwashes on the Tensile Strength of Selected Absorbable Sutures: An In Vitro Study. BiomedRes Int. 2018:8531706. DOI: 10.1155/2018/8531706
Об авторах
В. В. МитусовРоссия
Валерий Викторович Митусов - доктор медицинских наук, доцент; профессор кафедры урологии и репродуктивного здоровья человека (с курсом детской урологии-андрологии).
344022, Ростов-на-Дону, пер. Нахичеванский, д. 29
Конфликт интересов: нет
О. В. Воронова
Россия
Ольга Владимировна Воронова - ассистент кафедры оперативной хирургии, клинической анатомии и патологической анатомии.
344022, Ростов-на-Дону, пер. Нахичеванский, д. 29
Конфликт интересов: нет
М. И. Коган
Россия
Михаил Иосифович Коган - Заслуженный деятель науки РФ, доктор медицинских наук, профессор; заведующий кафедрой урологии и репродуктивного здоровья человека (с курсом детской урологии-андрологии).
344022, Ростов-на-Дону, пер. Нахичеванский, д. 29
Конфликт интересов: нет
З. А. Мирзаев
Россия
Заур Айдинович Мирзаев - аспирант кафедры урологии и репродуктивного здоровья человека (с курсом детской урологии-андрологии).
344022, Ростов-на-Дону, пер. Нахичеванский, д. 29
Конфликт интересов: нет
В. П. Глухов
Россия
Владимир Павлович Глухов - кандидат медицинских наук, доцент; доцент кафедры урологии и репродуктивного здоровья человека (с курсом детской урологии-андрологии).
344022, Ростов-на-Дону, пер. Нахичеванский, д. 29
Конфликт интересов: нет
Б. Г. Амирбеков
Россия
Бейкес Ганифаевич Амирбеков - кандидат медицинских наук; врач-уролог консультативно-поликлинического отделения Департамента по амбулаторно-поликлинической и параклинической работе.
344022, Ростов-на-Дону, пер. Нахичеванский, д. 29
Конфликт интересов: нет
Рецензия
Для цитирования:
Митусов В.В., Воронова О.В., Коган М.И., Мирзаев З.А., Глухов В.П., Амирбеков Б.Г. Существует ли целесообразность фармакотерапевтической подготовки слизистой полости рта к аугментационной уретропластике? Вестник урологии. 2020;8(3):38-46. https://doi.org/10.21886/2308-6424-2020-8-3-38-46
For citation:
Mitusov V.V., Voronova O.V., Kogan M.I., Mirzaev Z.A., Glukhov V.P., Amirbekov B.G. Is there a feasibility of pharmacotherapeutic preparation of the oral mucosa for augmentation urethroplasty? Urology Herald. 2020;8(3):38-46. (In Russ.) https://doi.org/10.21886/2308-6424-2020-8-3-38-46













































