Перейти к:
Результаты лечения гиперактивного мочевого пузыря после оперативных вмешательств по поводу гиперплазии предстательной железы в реальной клинической практике
https://doi.org/10.21886/2308-6424-2025-13-3-19-29
Аннотация
Введение. Различные методы оперативного лечения гиперплазии предстательной железы (ГПЖ) с высокой эффективностью ликвидируют симптомы опорожнения, улучшая качество мочеиспускания. Однако часто удовлетворённость лечением пациентов снижается за счёт сохранения симптомов накопления после оперативного лечения.
Цель исследования. Определить оптимальные подходы к терапии симптомов накопления у пациентов, перенёсших оперативное лечение ГПЖ с учётом распространённости симптомов и гиперактивности детрузора (ГД).
Материалы и методы. В исследование включены 94 пациента в возрасте 53 – 79 лет, оперированных по поводу ГПЖ, и с наличием симптомов накопления через 1 – 3 месяца после операции (балл IPSS-накопления ≥ 3). Пациентам выполняли комплексное уродинамическое исследование. В случае наличия симптомов накопления без подтверждённой ГД проведена поведенческая терапия (группа 1, n = 70). При выявлении ГД и наличии симптомов накопления без ургентного недержания мочи использовали медикаментозную терапию солифенацином 5 мг ежедневно (группа 2, n = 13), в случае выявления терминальной ГД, ургентного недержания мочи, применяли комбинированную терапию солифенацином 5 мг + мирабегрон 50 мг (группа 3, n = 11).
Результаты. Характеристики пациентов в предоперационном периоде не показали статистически значимых различий между группами в отношении возраста, уродинамических показателей и симптомов нижних мочевыводящих путей (СНМП), по данным опросника IPSS. На момент старта терапии медиана симптомов накопления составила 4, 8, 9 баллов в группах 1, 2, 3 соответственно. В группах как поведенческой, так и медикаментозной терапии определено достоверно значимое снижение выраженности симптомов накопления с течением времени (p < 0,001). Через 12 недель в группе 1 медиана симптомов накопления составила 3 балла, в группе 2 — 4 балла, в группе 3 — 6 баллов. На фоне проведения терапии в группе 3 ургентное недержание мочи ликвидировано. К 12 месяцам после оперативного лечения и приёма дополнительной терапии симптомы накопления, количество эпизодов ноктурии приближаются к равным значениям во всех группах (p > 0,05). Пациенты из групп медикаментозной терапии показали высокую приверженность терапии, не отмечено значимых побочных эффектов, требующих отмены продолжения приёма лекарственных препаратов.
Заключение. Применение медикаментозной терапии М-холиноблокаторами и / или β3-адреномиметиками в послеоперационном периоде при подтверждении ГД способствует уменьшению симптомов ургентности и увеличивает степень удовлетворённости пациентов лечением. При отсутствии ГД или IPSS-накопления ≤ 6 поведенческая терапия является хорошей альтернативой медикаментозной терапии.
Для цитирования:
Богданов Д.А., Юсуфов А.Г., Гуспанов Р.И., Котов С.В. Результаты лечения гиперактивного мочевого пузыря после оперативных вмешательств по поводу гиперплазии предстательной железы в реальной клинической практике. Вестник урологии. 2025;13(3):19-29. https://doi.org/10.21886/2308-6424-2025-13-3-19-29
For citation:
Bogdanov D.A., Yusufov A.G., Guspanov R.I., Kotov S.V. Overactive bladder following surgical intervention for benign prostatic hyperplasia: treatment outcomes in routine clinical practice. Urology Herald. 2025;13(3):19-29. (In Russ.) https://doi.org/10.21886/2308-6424-2025-13-3-19-29
Введение
Гиперплазия предстательной железы (ГПЖ) — заболевание, которое не теряет актуальности во всём мире и остаётся одним из самых распространённых доброкачественных заболеваний у мужчин среднего и пожилого возрастов. На гистологическом уровне ГПЖ встречается у 50% мужчин 51 – 60 лет, с возрастом доля пациентов увеличивается: 70% в возрасте 61 – 70 лет, 80% в возрасте 71 – 80 лет, достигая более 90% у мужчин старше 80 лет [1].
Мужчины могут испытывать различные проблемы с мочеиспусканием, к ним относятся слабая струя, учащённое мочеиспускание, ноктурия, чувство неполного опорожнения, прерывистость струи, ургентность. Когда консервативная терапия оказывается неэффективной или возникают какие-либо осложнения ГПЖ (острая задержка мочи, камень мочевого пузыря и другие), пациентам предлагается оперативное лечение. Все классические оперативные вмешательства, такие как открытая аденомэктомия, трансуретральные резекции и энуклеации, в том числе лапароскопические и робот-ассистированные техники, в целом сравнимы между собой по функциональной эффективности в виде улучшения максимальной скорости мочеиспускания, ликвидации инфравезикальной обструкции, несмотря на некоторые особенности, присущие той или иной методике [2][3].
В большинстве случаев симптомы опорожнения устраняются практически сразу после оперативного лечения, но симптомы накопления могут сохраняться длительное время. Часть пациентов беспокоит недержание мочи, у другой части пациентов наиболее беспокоящими симптомами после операции являются ургентность, учащённое мочеиспускание днём или ноктурия.
Гиперактивность детрузора (ГД) способствует сохранению симптомов накопления и снижает качество жизни больного и удовлетворённость от проведённой операции как пациента, так и оперирующего хирурга. В связи с этим нередко приходится применять дополнительное медикаментозное лечение для устранения симптомов накопления даже через несколько месяцев после операции.
Целью исследования ставится выявление распространённости сохранения накопительных симптомов и гиперактивности детрузора, а также сравнение вариантов терапии симптомов накопления после оперативного лечения ГПЖ в клинической практике.
Материалы и методы
За 2021 – 2024 годы проведено оперативное лечение 398 пациентов с ГПЖ. Всем пациентам проводили стандартное предоперационное обследование, включающее сбор жалоб и анамнеза, для объективизации жалоб использовали валидированный опросник IPSS-QoL. К стандартным инструментальным исследованиям относили УЗИ почек, мочевого пузыря с определением остаточной мочи, ТРУЗИ предстательной железы, урофлоуметрию. Также с целью определения индекса инфравезикальной обструкции и выявления ГД 192 пациентам выполнено уродинамическое исследование: цистометрия наполнения и «давление-поток». ГД при предоперационном обследовании была выявлена у 159 (82,8%) пациентов.
В послеоперационном периоде пациентам проводили контрольное обследование через 1, 3, 6, 12 месяцев. Оценку нарушений мочеиспускания производили посредством урофлоуметрии, УЗ-контроля остаточной мочи и валидированного опросника IPSS-QoL, используя при этом разделение баллов IPSS на симптомы накопления (IPSS-storage) и симптомы опорожнения (IPSS-voiding) — это простой метод для дифференциальной диагностики причины симптомов нижних мочевыводящих путей (СНМП) [4].
Среди 398 пациентов, оперированных по поводу ГПЖ, через 1 – 3 месяца при контрольном визите 280 пациентов (70,4%) предъявляли жалобы на сохранение симптомов накопления, что подтверждалось данными опросника IPSS (балл IPSS-storage ≥ 3). Методом рандомизации и при условии выполнения уродинамического исследования до оперативного лечения 123 пациентам предложено выполнение уродинамического исследования и включение в исследование. От выполнения исследования отказались 29 пациентов, они были исключены.
В итоге в текущее исследование включены 94 пациента в возрасте 53 – 79 лет, оперированных по поводу ГПЖ методами трансуретральной резекции, энуклеации простаты и лапароскопической аденомэктомии.
Критерии включения: пациенты, оперированные по поводу ГПЖ, у которых сохраняются симптомы накопления после хирургического лечения (балл IPSS-storage ≥ 3).
Критерии невключения: пациенты с отсутствием СНМП, по данным опросника IPSS после оперативного лечения; пациенты с выявленным инцидентальным раком предстательной железы.
Критерии исключения: пациенты, которые отказались от проведения уродинамического исследования в случае сохранения симптомов; пациенты, принимающие антихолинэргические препараты.
В случае сохранения симптомов накопления без уродинамически подтверждённой ГД пациентам медикаментозное лечение не применяли, рекомендовали поведенческую терапию (группа 1; n = 70). При выявлении ГД по данным КУДИ и сохранении симптомов накопления без ургентного недержания мочи («сухой» ГАМП) пациентам назначали медикаментозную терапию: солифенацин 5 мг ежедневно (группа 2; n = 13), а в случае выявления терминальной ГД, ургентного недержания мочи («мокрый» ГАМП), назначали комбинированную терапию солифенацин 5 мг + мирабегрон 50 мг (группа 3; n = 11). Дизайн исследования приведён на рисунке 1.
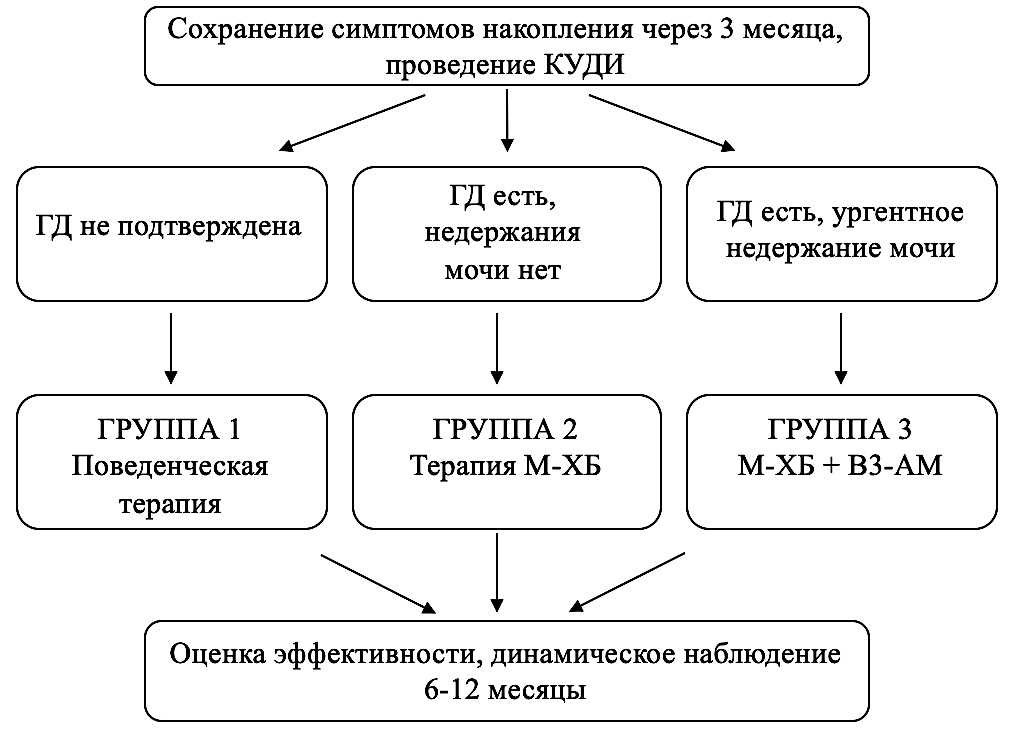
Рисунок 1. Дизайн исследования
Figure 1. Research design
Терапию проводили в течение 12 недель с последующим контрольным визитом на 6-м и 12-м месяцах после оперативного лечения.
Статистический анализ. Статистическую обработку данных осуществляли с использованием программного обеспечения программы StatTech v. 4.8.0 (ООО «Статтех», Россия). Для количественных данных, имеющих нормальное распределение, использовали среднее (М) и стандартное отклонение (SD), в тексте представлены в виде — М ± SD. Если количественные данные не подчинялись закону нормального распределения, для их описания применяли медиану (Ме) и 25-й / 75-й квартили (Q1; Q3), в тексте представлены в виде — Me [Q1; Q3]; 95%-й доверительный интервал (95% ДИ), для качественных данных — частоты (%). Для проверки статистических гипотез о виде распределения были применены критерии Shapiro-Wilk. Для сравнения непараметрических данных применяли Kruskal-Wallis test (для нескольких групп), сравнение двух независимых групп по качественным признакам производили с использованием критерия хи-квадрат Pearson (χ²). Для оценки дискриминационной способности количественных признаков при прогнозировании определённого исхода применяли метод анализа ROC-кривых. Разделяющее значение количественного признака в точке cut-off определяли по наивысшему значению Youden’s index. Различия считали достоверными при p < 0,05.
Результаты
Характеристики пациентов в предоперационном периоде не показали статистически значимых отличий между группами в отношении возраста, уродинамических показателей и СНМП по данным опросника IPSS. В группах 2 и 3 в сравнении с группой 1 объём простаты был больше, была более выражена степень симптомов накопления, однако статистически разница не подтверждена (p = 0,526 и p = 0,297 соответственно) (табл.). Также не выявлено отличий в распространённости сахарного диабета (p = 0,344; χ²).
Таблица. Предоперационные характеристики пациентов
Table. Preoperative characteristics of patients
Параметры Characteristics | Группа 1 Group 1 | Группа 2 Group 2 | Группа 3 Group 3 | P |
Возраст (M + SD), лет Age (M + SD), yrs | 67,3 ± 6,4 | 68,5 ± 6,4 | 65,3 ± 5,0 | 0,460 |
Объём ПЖ (Me [ Q1; Q3]), см³ Prostate volume (Me [ Q1; Q3]), cm³ | 81,1 [ 62,5; 112,5] | 94,4 [ 70,0; 108,0] | 101,7 [ 74,3; 119,6] | 0,526 |
Q max (Me [ Q1; Q3]), мл/с Q max (Me [ Q1; Q3]), ml/s | 6,8 [ 4,7; 9,1] | 8,5 [ 7,9; 9,8] | 7,1 [ 5,1; 8,7] | 0,115 |
Общий IPSS (M + SD), баллы Total IPSS (M + SD), score | 21,6 ± 6,6 | 20,5 ± 7,3 | 21,4 ± 6,3 | 0,879 |
IPSS-опорожнение (M + SD), баллы IPSS-voiding (M + SD), score | 12,8 ± 4,4 | 11,5 ± 4,3 | 13,6 ± 3,9 | 0,529 |
IPSS-накопление (Me [ Q1; Q3]), баллы IPSS-storage (Me [ Q1; Q3]), score | 9,0 [ 7,0; 11,0] | 10,0 [ 7,5; 11,25] | 11,0 [ 10,0; 11,0] | 0,297 |
Индекс ИВО (Me [ Q1; Q3]), баллы BOO index (Me [ Q1; Q3]), score | 67,5 [ 54,0; 90,0] | 64,0 [ 54,0; 92,0] | 70,0 [ 56,5; 100,0] | 0,900 |
Примечания: 1) M — среднее; SD — стандартное отклонение; Ме — медиана; Q1 — 25% перцентиль; Q3 — 75% перцентиль. 2) ПЖ — предстательная железа; Q max — максимальная скорость мочеиспускания; IPSS — Международная система суммарной оценки заболеваний предстательной железы в баллах; ИВО — инфравезикальная обструкция
Notes: 1) M — mean; SD — standard deviation; Ме — median; Q1 — 25% percentile; Q3 — 75% percentile. 2) IPSS — International Prostate Symptom Score; Q max — maximal urinary flow rate; BOO — bladder outlet obstruction
Временное недержание мочи после удаления уретрального катетера было выявлено в 46 случаях, а именно у всех пациентов групп 2 и 3 (суммарно 24 пациента); из группы 1 временное недержание было зафиксировано у 22 пациентов. В большинстве случаев недержание было обусловлено ургентностью или смешанной природой и прекратилось в течение 1 месяца (кроме пациентов группы 3). Отмечено, что у пациентов, страдающих сахарным диабетом, при выполнении уродинамического исследования наличие сахарного диабета не оказывало влияния на частоту определения послеоперационной ГД и недержания мочи (p = 1,000; p = 0,365).
Среди 94 пациентов, включённых в исследование, ГД до операции выявлена у 78 (83%) пациентов. По данным контрольного уродинамического исследования, ГД сохранялась у 20 (21,3%) пациентов, а у 4 пациентов ГД возникла de novo.
Несмотря на факт наличия симптомов накопления после операции, мы получили хорошие функциональные результаты оперативного лечения в виде изменения максимальной скорости потока мочи (Q max), объёма остаточной мочи и уменьшения симптомов опорожнения, по данным IPSS (p < 0,001).
На рисунке 2 представлены результаты Q max после удаления уретрального катетера и при контрольных визитах. Среди каждой из групп отчётливо видна положительная динамика качества мочеиспускания (p < 0,001). В целом между группами в одной точке наблюдения показатели не различаются, хотя на 3-м и 6-м месяцах наблюдения среднее значение Q max в группе 1 статистически достоверно лучше, чем в группах 2 и 3 (p = 0,019; p = 0,015; соответственно). На графике хорошо отражено, что сама динамика изменения показателя скорости мочеиспускания внутри каждой из групп разная (p = 0,016). Если в группе без дополнительных назначений к 3-му месяцу Q max практически выходит на плато и удерживается на одном уровне на 6-м и 12-м месяцах наблюдения, то в группах 2 и 3 наблюдается положительная динамика относительно предыдущего визита.
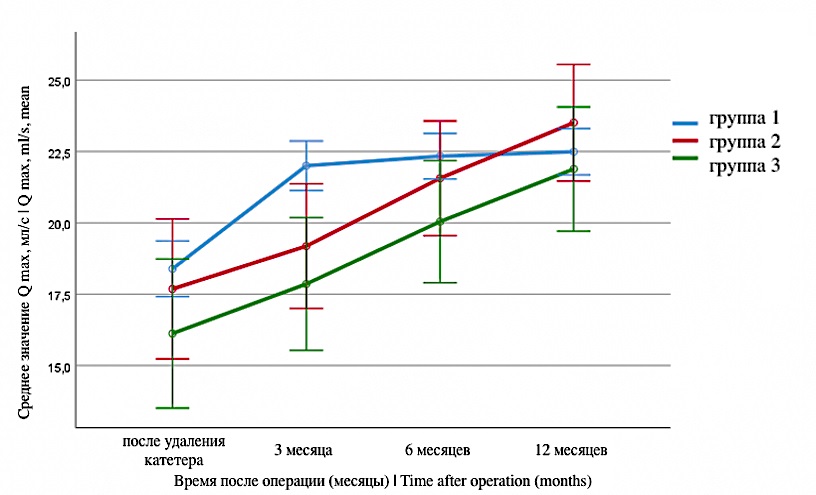
Рисунок 2. Динамика изменения Q max после операции
Figure 2. Dynamics of the Q max change after surgery
Если рассматривать симптомы опорожнения (рис. 3), то оперативное лечение с высокой степенью эффективности их устраняет в ближайшее время после проведённой операции (p < 0,001). В течение наблюдения нет абсолютно никаких достоверных различий в симптомах опорожнения между группами как в отношении динамики изменения симптомов (p = 0,839), так и в каждой временной точке наблюдения (p = 0,411).
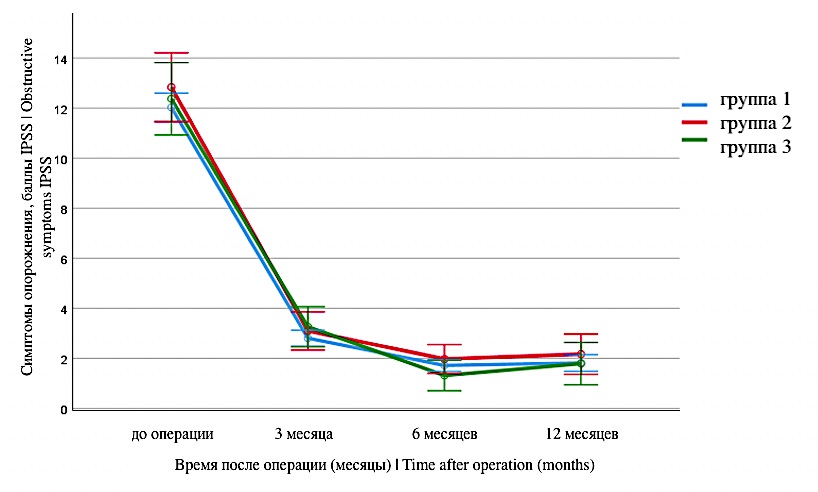
Рисунок 3. Динамика симптомов опорожнения после операции
Figure 3. Dynamics of voiding symptoms after surgery
Динамика изменения симптомов накопления отражена на рисунке 4. Показано, что в группе 1 симптомы накопления значительно уменьшилась к 3-му месяцу наблюдения после оперативного лечения. Пациенты, у которых выявлена ГД после оперативного лечения, к 3-му месяцу имеют минимальную положительную динамику, крутое снижение симптоматики в данных группах отмечается только после назначения медикаментозной терапии (p < 0,001). При этом в группе как поведенческой, так и медикаментозной терапии определяется достоверно значимое улучшение симптомов накопления с течением времени (p < 0,001). Не вызывает сомнений, что между группами в отдельных точках наблюдения результаты достоверно различаются (p < 0,001). Через 12 недель приёма медикаментозной терапии в группе 3 у всех пациентов «мокрый» ГАМП ликвидирован (рис. 4).
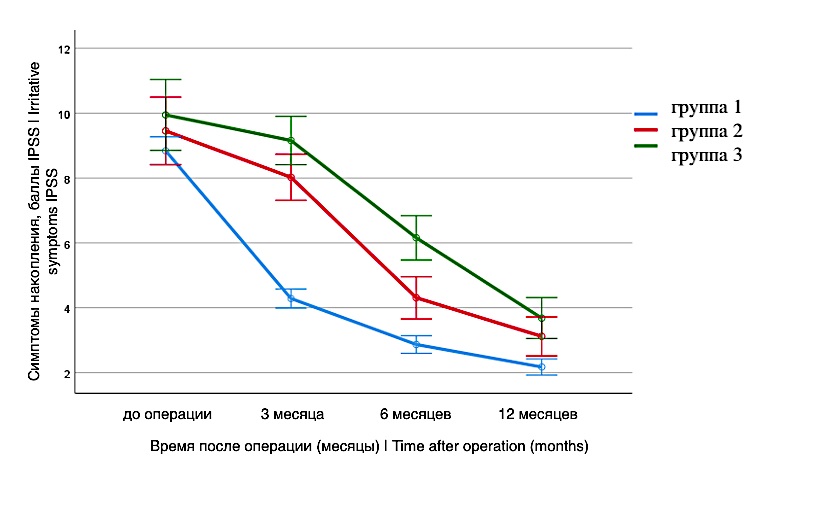
Рисунок 4. Динамика симптомов накопления после операции
Figure 4. Dynamics of storage symptoms after surgery
Пороговое значение симптомов накопления после операции в точке cut-off, которому соответствовало наивысшее значение Youden’s index, составило 7,0 баллов. Наличие ГД прогнозировали при значении симптомов накопления через 1 месяц выше данной величины или равном ей. Чувствительность и специфичность полученной прогностической модели составили 82,6% и 88,7% соответственно (рис. 5).
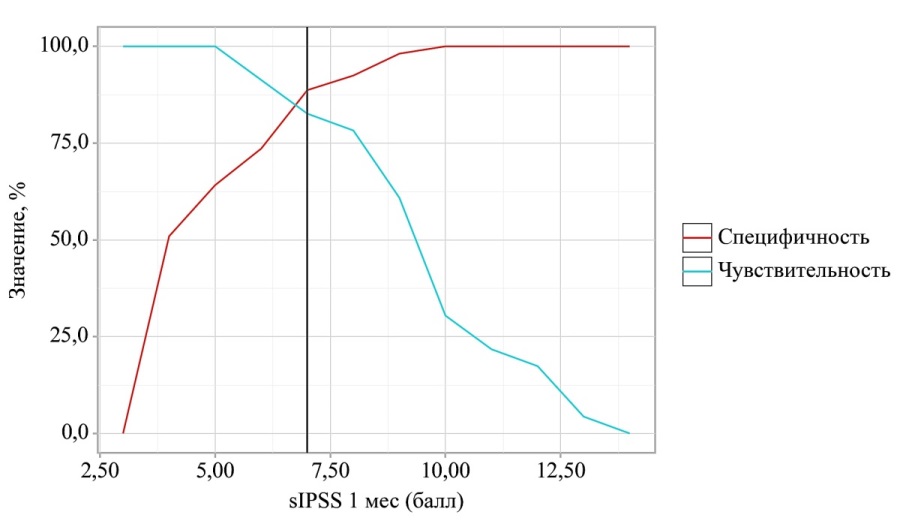
Рисунок 5. Анализ чувствительности и специфичности модели в зависимости от пороговых значений оценок вероятности детрузорной гиперактивности после операции
Figure 5. Analysis of the sensitivity and specificity of the model depending on threshold probability scores for detrusor overactivity after surgery
На рисунке 6 отражено изменение количества ночных мочеиспусканий (ноктурии). Динамика ноктурии, а также значения в точке старта терапии в зависимости от группы статистически достоверно различаются (p < 0,001; p = 0,002 соответственно). К 12 месяцам после оперативного лечения и приёма дополнительной терапии частота эпизодов ноктурии приближается к равным значениям в группах пациентов (p > 0,05).
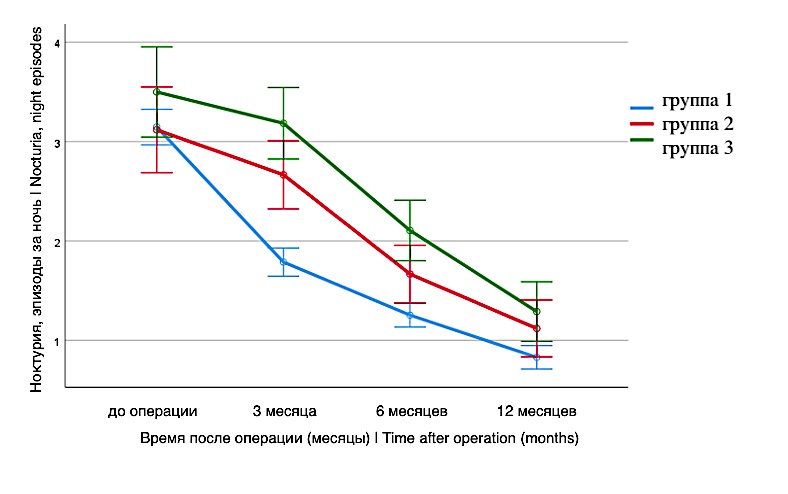
Рисунок 6. Динамика ноктурии после операции
Figure 6. Dynamics of nocturia after surgery
Уровень остаточной мочи был сопоставим между группами (p = 0,548) и не отличался во всех точках наблюдения (p = 0,224) — рисунок 7.
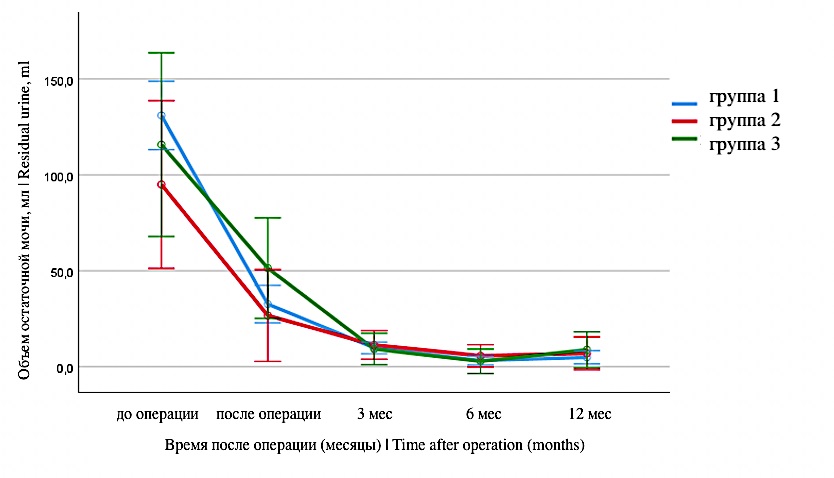
Рисунок 7. Динамика изменения уровня остаточной мочи после операции
Figure 7. Dynamics of post-void residual volume after surgery
Пациенты из групп медикаментозной терапии показали высокую приверженность терапии, не отмечено значимых побочных эффектов, требующих отмены приёма лекарственных препаратов. В одном случае среди пациентов группы 2 и в двух случаях в группе 3 пациенты предъявляли жалобы на умеренную сухость во рту. Медикаментозная терапия не ухудшала функциональные результаты.
Обсуждение
Несмотря на неоспоримую эффективность и ликвидацию обструктивной симптоматики, пациенты после оперативного лечения по поводу ГПЖ долгое время могут испытывать расстройства мочеиспускания, в основном в виде симптомов накопления [5][6].
В проспективном мультицентровом исследовании D. Castellani et al. (2022) отмечают, что восстановление после трансуретральной хирургии может занимать около 12 месяцев. Симптомы накопления, по данным IPSS, снижались на 72,8% за 1 месяц, а через год после операции — уже на 94,8%. Ургентное недержание наблюдали у 26,5 % мужчин через 1 месяц, у 15,4% — через 3 месяца и у 4,3 % — через 6 месяцев [7].
В нашем исследовании отмечена подобная динамика. У пациентов без подтверждённой ГД после оперативного лечения в первые месяцы сохраняются симптомы накопления, но в отличие от пациентов с ГД имеет место положительная динамика уже к 3-му месяцу после операции.
Иначе выглядит симптоматика у пациентов с ГД после операции. К 3 месяцам после оперативного лечения симптомы ургентности у пациентов с ГД выражены сильнее, чем у пациентов без таковой, что и обусловливает назначение медикаментозной терапии, направленной на купирование симптомов.
По данным S.J. Kim et al. (2023), 18,6% прооперированных пациентов требовало назначения медикаментозной терапии после операции, что примерно соотносится с нашими данными (25,5%). Гиперактивный мочевой пузырь, терминальная ГД и ургентные позывы были идентифицированы как возможные прогностические факторы для использования медикаментозной терапии после трансуретральной энуклеации [8].
В ещё более раннем исследовании J. Jeong et al. (2015) показали, что доля пациентов, которые начинают терапию после оперативного лечения, резко возрастает. Среди 110 пациентов, включённых в исследование, 52,7% имели ГД. Если до операции всего 17 пациентов принимали М-холиноблокаторы по поводу симптомов накопления, то после оперативного лечения необходимость в дополнительной терапии требовалась 49 пациентам на 3-м месяце наблюдения и 39 пациентам на 6-м месяце наблюдения. Доля пациентов с ГАМП преобладала (48,3% против 21,2%) [9]. Это говорит о том, что, ликвидировав инфравезикальную обструкцию, мы не можем сказать, что однозначно устранили беспокойства пациента относительно его мочеиспускания и повысили качество его жизни. С пациентами необходимо проговаривать возможные варианты восстановительного периода и его длительности после операции, а также высокий риск медикаментозной терапии после оперативного лечения.
С целью снижения симптомов накопления в послеоперационном периоде в российском исследовании С.Н. Волков и соавт. (2024) сравнили различные методики выполнения лапароскопической транскапсулярной аденомэктомии, дополненной уретроцистоанастомозом. Авторы отмечают, что данная модификация имеет преимущества в отношении симптомов накопления в послеоперационном периоде в сравнении с классической аденомэктомией и трансуретральной энуклеацией гиперплазии больших размеров. Средний балл ирритативного компонента IPSS был значимо ниже в группе выполнения уретроцистоанастомоза в сравнении со стандартной лапароскопической аденомэктомией и трансуретральной гольмиевой лазерной энуклеацией простаты (p = 0,032 и р = 0,001 соответственно). Наблюдаемая тенденция сохранялась и к 6-му месяцу после операции [10].
А.Г. Мартов и соавт. (2019) проводили исследование по назначению солифенацина после трансуретральной резекции предстательной железы и показали, что комбинированная терапия тамсулозин 0,4 мг + солифенацин 5 мг улучшает симптомы накопления начиная с 1-го месяца после операции, при этом не влияя на Q max и количество остаточной мочи, период наблюдения составил 3 месяца [11].
На основании полученных результатов мы предлагаем следующий алгоритм ведения пациентов после оперативного вмешательства. При условии сохранения симптомов накопления и недержания мочи через 3 месяца после операции можно с большой уверенностью говорить о сохранении ГД («мокрый» ГАМП), таким пациентам мы рекомендуем проводить комбинированную терапию М-холиноблокаторами и β3-адреномиметиками. В случае отсутствия недержания мочи при сохраняющихся симптомах накопления рекомендуется выполнить уродинамическое исследование и при подтверждении ГД назначать стартовую терапию М-холиноблокаторами, согласно клиническим рекомендациям. При невозможности выполнения КУДИ и / или симптомах IPSS-storage ≥ 7, с большой вероятностью можно предполагать наличие ГД и также проводить медикаментозную терапию М-холиноблокаторами.
При отсутствии фазовых волн гиперактивности или показателе IPSS storage < 7, можно ограничиться поведенческой терапией.
Применение медикаментозной терапии как в монорежиме, так и в комбинированном варианте может считаться безопасным и, как показывают результаты нашего исследования, приводит к значимому улучшению симптомов накопления у пациентов с сохраняющейся ГД после операции.
Заключение
Согласно результатам нашего исследования, расстройства мочеиспускания после оперативного лечения ГПЖ встречаются нередко. Основным предрасполагающим фактором является ГД вследствие длительной инфравезикальной обструкции. Несмотря на устранение обструктивного компонента, симптомы накопления значимо снижают качество жизни. Применение дополнительной медикаментозной терапии М-холиноблокаторами и / или β3-адреномиметиками в послеоперационном периоде способствует уменьшению симптомов ургентности и увеличивает степень удовлетворённости пациентов лечением.
Список литературы
1. Berry SJ, Coffey DS, Walsh PC, Ewing LL. The development of human benign prostatic hyperplasia with age. J Urol. 1984;132(3):474-479. DOI: 10.1016/s0022-5347(17)49698-4
2. Wang YB, Yan SY, Xu XF, Huang X, Luo LS, Deng YQ, Li XH, Huang Q, Wang YY, Huang J, Jin YH, Zeng XT. Comparison on the Efficacy and Safety of Different Surgical Treatments for Benign Prostatic Hyperplasia With Volume >60 mL: A Systematic Review and Bayesian Network Meta-Analysis of Randomized Controlled Trials. Am J Mens Health. 2021;15(6):15579883211067086. DOI: 10.1177/15579883211067086
3. Chen F, Chen Y, Zou Y, Wang Y, Wu X, Chen M. Comparison of holmium laser enucleation and transurethral resection of prostate in benign prostatic hyperplasia: a systematic review and meta-analysis. J Int Med Res. 2023;51(8):3000605231190763. DOI: 10.1177/03000605231190763
4. Liao CH, Chung SD, Kuo HC. Diagnostic value of International Prostate Symptom Score voiding-to-storage subscore ratio in male lower urinary tract symptoms. Int J Clin Pract. 2011;65(5):552-558. DOI: 10.1111/j.1742-1241.2011.02638.x
5. Котов С.В., Перов Р.А., Жестков И.А., Новиков А.А., Неменов А.А. Оценка функциональных результатов и послеоперационных осложнений гольмиевой лазерной энуклеации предстательной железы крупных размеров. Вестник урологии. 2024;12(2):33-42. DOI: 10.21886/2308-6424-2024-12-2-33-42
6. Панферов А.С., Котов С.В., Юсуфов А.Г., Елагин В.В., Бекреев Е.А., Бадаква Г.В., Семенов А.П. Лапароскопическая трансвезикальная аденомэктомия при крупных и гигантских размерах предстательной железы. Экспериментальная и клиническая урология. 2022;15(1):102-110. DOI: 10.29188/2222-8543-2022-15-1-102-110
7. Castellani D, Di Rosa M, Saredi G, Pacchetti A, Banchero R, Ambrosini F, Meroni P, Guano G, Boltri M, Bucci S, Simonetti E, Maestroni UV, Ferretti S, Terrone C, Dellabella M. Change in Postoperative Storage Symptoms and De Novo Urge Incontinence After Thulium:YAG Laser Enucleation of the Prostate: Results from a Prospective Multicenter Study. J Endourol. 2022;36(9):1223-1230. DOI: 10.1089/end.2022.0118
8. Kim SJ, Park SG, Pak S, Kwon O, Lee YG, Cho ST. Predictive factors for postoperative medication therapy for overactive bladder symptoms after holmium laser enucleation of prostate. Int J Urol. 2023;30(11):1036-1043. DOI: 10.1111/iju.15260
9. Jeong J, Lee HS, Cho WJ, Jung W, You HW, Kim TH, Sung HH, Lee KS. Effect of Detrusor Overactivity on Functional Outcomes After Holmium Laser Enucleation of the Prostate in Patients With Benign Prostatic Obstruction. Urology. 2015;86(1):133-138. DOI: 10.1016/j.urology.2015.03.033
10. Волков С.Н., Пушкарь Д.Ю., Колонтарев К.Б., Степанченко В.С., Терещенко В.И., Джаримок А.Р., Шевякина А.Е., Дауров М.А. Выраженность симптомов нижних мочевых путей в послеоперационном периоде как фактор выбора подхода к хирургическому лечению гиперплазии простаты больших размеров: гольмиевая энуклеация предстательной железы и лапароскопическая позадилонная аденомэктомия. Вестник урологии. 2024;12(2):5-14. DOI: 10.21886/2308-6424-2024-12-2-5-14
11. Мартов А.Г., Турин Д.Е., Ергаков Д.В., Андронов А.С., Камалов А.А. Выбор медикаментозной терапии у пациентов после биполярной трансуретральной резекции предстательной железы в зависимости от ее исходных размеров. Экспериментальная и клиническая урология. 2019;11(2):70-79. DOI: 10.29188/2222-8543-2019-11-2-70-78
Об авторах
Д. А. БогдановРоссия
Даниил Андреевич Богданов
Москва
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
А. Г. Юсуфов
Россия
Ренат Иватуллаевич Гуспанов — канд. мед. Наук.
Москва
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
Р. И. Гуспанов
Россия
Анвар Гаджиевич Юсуфов — канд. мед. наук.
Москва
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
С. В. Котов
Россия
Сергей Владиславович Котов — д-р мед. наук, профессор.
Москва
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
Рецензия
Для цитирования:
Богданов Д.А., Юсуфов А.Г., Гуспанов Р.И., Котов С.В. Результаты лечения гиперактивного мочевого пузыря после оперативных вмешательств по поводу гиперплазии предстательной железы в реальной клинической практике. Вестник урологии. 2025;13(3):19-29. https://doi.org/10.21886/2308-6424-2025-13-3-19-29
For citation:
Bogdanov D.A., Yusufov A.G., Guspanov R.I., Kotov S.V. Overactive bladder following surgical intervention for benign prostatic hyperplasia: treatment outcomes in routine clinical practice. Urology Herald. 2025;13(3):19-29. (In Russ.) https://doi.org/10.21886/2308-6424-2025-13-3-19-29
JATS XML













































