Перейти к:
Ревизия искусственного мочевого сфинктера у мужчин: многолетний опыт одиночного центра
https://doi.org/10.21886/2308-6424-2025-13-1-56-62
Аннотация
Введение. Основным методом оперативного лечения мужчин со стрессовым недержанием мочи средней и тяжёлой степени является установка искусственного мочевого сфинктера (ИМС). Несмотря на эффективность, имплантация сопряжена с развитием осложнений, в ряде случаев требующих ревизий и удаления всего устройства или его компонентов.
Цель исследования. Оценить результаты установки ИМС в отношении безопасности и необходимости повторных вмешательств при длительном наблюдении.
Материалы и методы. С 2004 по 2023 годы ИМС имплантирован 62 пациентам со стрессовым недержанием мочи тяжёлой степени. Осложнения учитывались согласно модифицированной классификации хирургических осложнений Clavien-Dindo. Производился учёт ревизий, сопровождающихся заменой компонентов или всего ИМС при отсутствии признаков инфекции, и ревизий, сопровождающихся удалением компонентов и всего ИМС в случае инфекции.
Результаты. Средний возраст пациента на момент имплантации составил 67,4 ± 8 лет. При медиане времени наблюдения 73,5 [14,8 – 118,3] месяца у 22 (35,5%) пациентов отмечены осложнения, выполнены 33 ревизии. Медиана времени до осложнения, требующего замены ИМС или его компонентов, составила 60 [50 – 94] месяцев. Медиана времени до осложнения, требующего удаления ИМС или его компонентов, составила 31 [8 – 83] месяц. Выявлено статистически значимое влияние сахарного диабета на замену компонентов ИМС (ОШ 4,9, p < 0,05).
Заключение. Установка ИМС связана с развитием осложнений, требующих ревизии, доля их составляет около трети всех вмешательств на ИМС. Ревизии позволяют восстановить работу ИМС и улучшить качество жизни пациентов. С учётом несовершенства применения общехирургической классификации осложнений у мужчин, перенёсших оперативное лечение недержания мочи, требуется пересмотр учёта и классификации осложнений этого вида вмешательств.
Ключевые слова
Для цитирования:
Томилов А.А., Велиев Е.И., Голубцова Е.Н., Багателия З.А. Ревизия искусственного мочевого сфинктера у мужчин: многолетний опыт одиночного центра. Вестник урологии. 2025;13(1):56-62. https://doi.org/10.21886/2308-6424-2025-13-1-56-62
For citation:
Tomilov A.A., Veliev E.I., Golubtsova E.N., Bagatelia Z.A. Revision of the artificial urinary sphincter in men: a long-term experience from a single centre. Urology Herald. 2025;13(1):56-62. (In Russ.) https://doi.org/10.21886/2308-6424-2025-13-1-56-62
Введение
Установка искусственного мочевого сфинктера ИМС — наиболее часто выполняемое и наиболее изученное оперативное вмешательство, направленное на устранение стрессового недержания мочи у мужчин [1-4]. Ежегодное число имплантаций исчисляется тысячами [5]. Современные клинические рекомендации предлагают рассматривать установку ИМС преимущественно пациентам с недержанием мочи средней и тяжёлой степени [2]. Несмотря на высокую эффективность при длительном наблюдении [3][6][4], имплантация сопряжена с развитием осложнений, в ряде случаев требующих ревизий и удаления всего устройства или его компонентов [5-7]. Настоящее исследование посвящено изучению ревизий ИМС при долгосрочном наблюдении.
Цель исследования: оценить результаты установки ИМС в отношении безопасности и необходимости повторных вмешательств при длительном наблюдении.
Материалы и методы
В исследование включены результаты лечения и наблюдения 62 пациентов, которым с 2004 по 2023 годы произведена установка ИМС AMS 800 («American Medical Systems Inc.», Minnetonka, MN, USA) в городской клинической больнице им. С.П. Боткина (г. Москва). У пациентов производили тщательный сбор анамнеза, устанавливали причину и сроки НМ, отмечали ранее проводимые попытки хирургической коррекции, наличие предшествующей лучевой терапии и других факторов риска. Потери мочи оценивали с помощью дневника мочеиспускания. Перед установкой или ревизией ИМС у каждого пациента было взято информированное согласие.
Имплантация включала следующие основные этапы: мобилизацию луковичного отдела уретры промежностным или пеноскротальным доступом, измерение окружности уретры и установку манжеты соответствующего диаметра, формирование ложа резервуара, его установку и наполнение, формирование ложа помпы в мошонке, а также герметичное соединение всех компонентов с помощью коннекторных трубок. ИМС интраоперационно был деактивирован. Мочевой пузырь дренирован уретральным катетером, который удаляли в первый послеоперационный день. Активацию ИМС производили через 4 – 6 недель.
Учёт осложнений проводили с применением модифицированной классификации хирургических осложнений Clavien-Dindo. Производили учёт ревизий, сопровождающихся заменой компонентов или всего ИМС при отсутствии признаков инфекции и ревизий, сопровождающихся удалением компонентов и всего ИМС в случае инфекции. В последнем случае в последующем могла быть проведена ревизия с повторной установкой удалённого ранее компонента или всего ИМС. Оценивали влияние на исходы следующих предоперационных факторов: сахарный диабет, лучевая терапия, стриктура уретры, ранее проведённое вмешательство по поводу недержания мочи.
Статистический анализ. Ведение базы данных пациентов производили с помощью программы Microsoft Office Excel 365 (Microsoft Corp., Redmond, WA, USA), статистическую обработку с помощью программы Statistica v 12.0 (Statsoft Inc., Tulsa, OK, USA). Нормальность распределения выявляли с помощью метода Shapiro-Wilk. Описательная статистика представлена в зависимости от типа распределения: средних (М), стандартного отклонения (± SD), медиан (Ме), межквартильного размаха [LQ – UQ]. Для исследования влияния факторов риска использовали модель пропорциональных рисков Cox. Анализ выживаемости ИМС проводили с использованием метода Kaplan-Meier. Различия считали достоверными при p < 0,05.
Результаты
Средний возраст пациента на момент имплантации составил 67,4 ± 8 лет. Причинами стрессового недержания мочи тяжёлой степени были последствия радикальной простатэктомии (61,3%), трансуретральной резекции предстательной железы (21%), чреспузырной аденомэктомии (8,1%) и других вмешательств (9,7%). Медиана времени после вмешательства, послужившего причиной недержания мочи до установки ИМС составила 24 [ 13 – 36] месяца. Кроме того, у 48,4% пациентов недержание мочи сочеталось со стриктурой уретры, потребовавшей оперативного вмешательства перед установкой ИМС, а 16,1% пациентов до установки ИМС перенесли другие вмешательства по поводу недержания мочи.
У 22 (35,5%) пациентов отмечены 28 осложнений. 19 пациентам (30,6% от всех первичных имплантаций) выполнены ревизии, 11 из них повторные, всего выполнены 33 ревизии. Доля инфекционных осложнений составила 46,4%, доля неинфекционных осложнений составила 53,6%.
Характер и число осложнений, которые были причинами ревизии ИМС, представлены в таблице в соответствии с классификацией хирургических осложнений Clavien-Dindo.
Медиана времени до развития осложнения, требующего ревизии, составила 58 [ 18 – 94] месяцев. Медиана времени до осложнения, требующего замены ИМС или его компонентов, составила 60 [ 50 – 94] месяцев.
Кривая выживаемости без замены ИМС и его компонентов представлена на рисунке 1. Медиана времени до осложнения, требующего удаления ИМС или его компонентов, составила 31 [ 8 – 83] месяц. Кривая выживаемости без удаления ИМС и его компонентов представлена на рисунке 2.
При анализе факторов риска с помощью регрессионного анализа было выявлено статистически значимое сильное влияние сахарного диабета на замену компонентов ИМС (ОШ = 4,9; p < 0,05).
Таблица. Осложнения установки ИМС, которые привели к ревизии
Table. Complications of AUS implantation resulting in revision
Осложнения — лечебные мероприятия | Complications — repairs | Количество, n (%) * | Total, n (%) * | |
Clavien-Dindo IIIa | Эрозия уретры — удаление манжеты или ИМС Urethral erosion — AUS cuff removal | 10 (16,1) |
Дефицит жидкости — ревизия с восполнением объема Fluid deficit — revision with volume restoration | 9 (14,5) | |
Ятрогенное повреждение резервуара — замена Iatrogenic reservoir damage — Replacement | 1 (1,6) | |
Механическая поломка — замена части/всей системы Mechanical failure — Part / whole AUS replacement | 3 (4,8) | |
Примечание. * — % от общего числа имплантаций Note. * — % of the overall number of implantations | ||
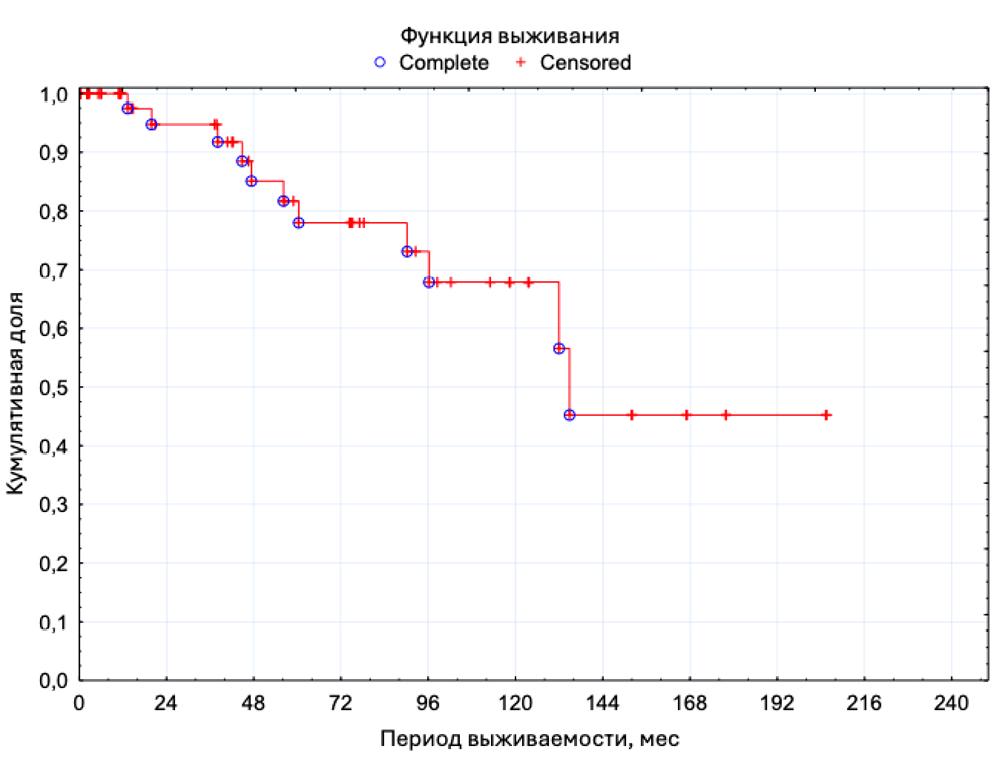
Рисунок 1. Кривая выживаемости ИМС без замены его компонентов
Figure 1. Kaplan-Meier curve of the AUS without replacement of its components
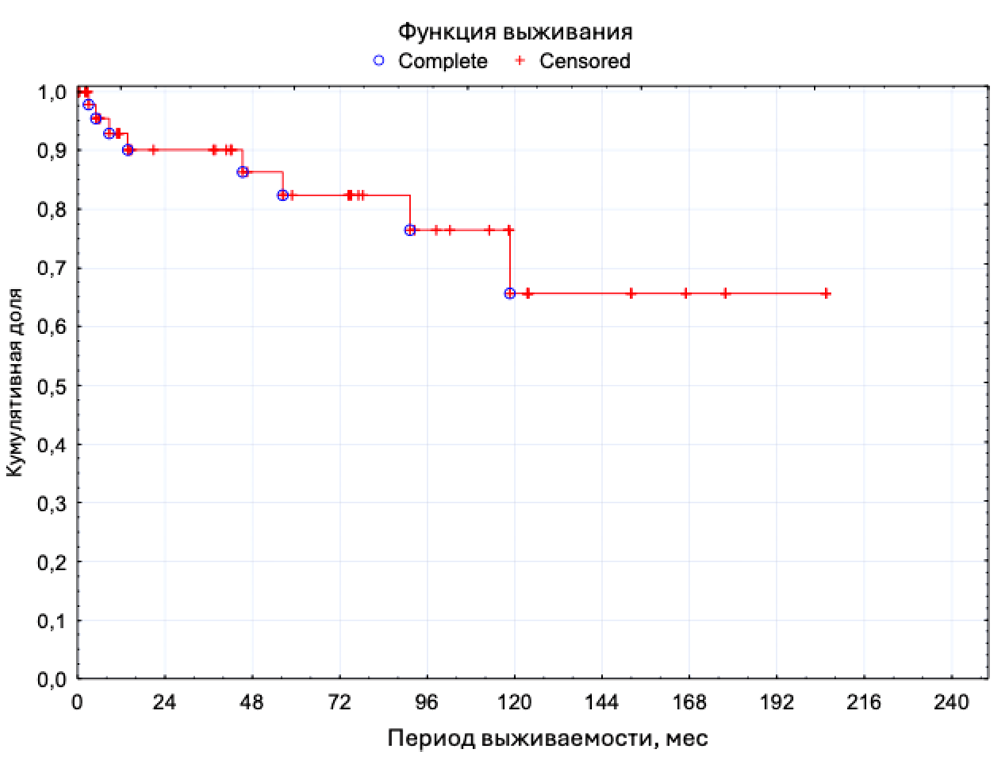
Рисунок 2. Кривая выживаемости ИМС без его удаления
Figure 2. Kaplan-Meier curve of the AUS without removal
Обсуждение
Концепция ИМС, реализуемая в большинстве современных устройств, предложена F. Scott et al. (1974) более полувека назад и заключается в сдавлении мочеиспускательного канала манжетой, состоящей из эластичного полимера [8]. На успех установки и развитие возможных осложнений оказывают влияние факторы, зависящие как от пациента (состояние уретры, инфекция, сопутствующие заболевания и др.), так и от хирурга (опыт, асептика и др.) и самого устройства (механическая поломка, утечка жидкости и др.) [9]. Одним из наиболее частых и наиболее сложных осложнений является эрозия уретры в месте стояния манжеты [10]. Очевидно, что недостаточное сдавление мочеиспускательного канала манжетой может привести к неэффективности операции, в то время как чрезмерное — к эрозии уретры. При этом наличие имплантированного искусственного материала повышает риски инфекционных осложнений [7][11 – 13].
В больших сериях и при длительном наблюдении показано, что около трети вмешательств с ИМС — это его ревизии [14]. С увеличением срока наблюдения растёт и доля пациентов, подвергнутых повторным вмешательствам. В исследовании B. Linder et al. (2015) через 1, 5, 10 и 15 лет после установки доля пациентов, которым не выполнялись повторные вмешательства, составила 90%, 74%, 57% и 41% соответственно [15]. В работе P. Leon et al. (2015) через 5, 10, 15 и 20 лет доля пациентов, которым не выполнялась ревизия, и вовсе составила 59%, 28%, 15% и 5% соответственно [6]. В другом исследовании 263 пациента с медианой наблюдения 61 месяц медиана времени до ревизии составила 10,8 года [16]. В нашем исследовании среди 95 вмешательств по поводу ИМС 62 были первичными установками, а 33 — ревизиями, таким образом, доля повторных вмешательств составила 35%.
В случае развития осложнений, требующих ревизии ИМС, большинство пациентов вне зависимости от возраста готово подвергаться повторным вмешательствам с надеждой на восстановление работы устройства. Связано это со значительным влиянием расстройств мочеиспускания на качество жизни пациентов. При этом факт проведения ревизии не оказывает негативного влияния на эффективность ИМС, а пациенты продолжают быть удовлетворены имплантацией [1]. В нашем исследовании среди 19 пациентов, подвергнутых повторным вмешательствам, восстановить работу устройства и качество жизни удалось у 11 (58%) пациентов.
С клинической точки зрения, в отношении тактики ведения мужчин с осложнениями оперативного лечения недержания мочи следует различать ревизии неинфицированного ИМС и ревизии с целью удаления ИМС или его компонентов по поводу инфекции, поскольку в первом случае ревизия предполагает одноэтапное восстановление работоспособности устройства, в то время как в последнем случае предполагается многоэтапное лечение, включающее удаление устройства или его части, борьбу с инфекцией и повторную установку ИМС или его компонентов. В исследованной нами группе пациентов доля ревизий, связанных с инфекционными осложнениями, составила 19%, а доля вмешательств по поводу неинфекционных осложнений составила 16% от числа всех вмешательств на ИМС. При этом повторные вмешательства у пациентов по поводу неинфекционных осложнений позволяли восстановить работу устройства в 86% случаев, в то время как при вмешательствах в отношении осложнений, связанных с инфекцией, восстановить работу устройства удалось лишь в 27% случаев. Причинами существенно худших результатов у последней группы пациентов являются наличие полирезистентной микрофлоры и выраженные изменения мочеиспускательного канала. Различия в медиане развития неинфекционных (60 месяцев) и инфекционных (31 месяц) осложнений свидетельствуют не только об изменении числа, но и характера осложнений и причин ревизий ИМС с увеличением периода наблюдения.
В этой связи стоит отметить несовершенство общепринятой классификации хирургических осложнений Clavien-Dindo в отношении пациентов с недержанием мочи, которая не отражает существенных различий при регистрируемых осложнениях. Например, к осложнению IIIa (вмешательство без общей анестезии) могут быть отнесены такие различные осложнения, как острая задержка мочеиспускания, требующая цистостомии, замена помпы при механической поломке и удаление ИМС при перипротезной инфекции [17]. Учёт и классификацию осложнений у таких пациентов целесообразно проводить с учётом наличия или отсутствия признаков инфекции и необходимости ревизии.
Ограничения исследования. Стоит отметить несколько ограничений проведённой работы. Исследование носило ретроспективный характер и было проведено в одном центре.
Заключение
Установка ИМС связана с развитием осложнений, требующих ревизии, доля их составляет около трети всех вмешательств на ИМС. Ревизии позволяют восстановить работу ИМС, при этом пациенты готовы подвергаться повторным вмешательствам с целью улучшения качества жизни. С учётом несовершенства общехирургической классификации осложнений у мужчин, перенёсших оперативное лечение недержания мочи, требуется пересмотр учёта и классификации осложнений этого вида вмешательств.
Ключевые моменты:
1) установка ИМС связана с развитием осложнений и необходимостью ревизий (до трети вмешательств при длительном наблюдении);
2) наличие сахарного диабета влияет на частоту необходимости замены компонентов ИМС;
3) требуется разработка классификации осложнений оперативного лечения недержания мочи.
Список литературы
1. Viers BR, Linder BJ, Rivera ME, Rangel LJ, Ziegelmann MJ, Elliott DS. Long-Term Quality of Life and Functional Outcomes among Primary and Secondary Artificial Urinary Sphincter Implantations in Men with Stress Urinary Incontinence. J Urol. 2016;196(3):838-843. DOI: 10.1016/j.juro.2016.03.076
2. EAU Guidelines. Edn. presented at the EAU Annual Congress Milan; 2023.
3. Abrams P, Cardoso L, Wagg A, Wein A, eds. Incontinence (7th ed.). Bristol, UK: International Continence Society; 2023. ISBN: 978-0-9569607-4-0
4. Велиев Е.И., Томилов А.А., Голубцова Е.Н. Долгосрочные результаты эффективности и безопасности имплантации искусственного мочевого сфинктера AMS 800ТМ. Вестник урологии. 2021;9(1):14-21. DOI: 10.21886/2308-6424-2021-9-1-14-21
5. Plata M, Zuluaga L, Santander J, Salazar M, Castaño JC, BenavidesMartÍnez JA, Garzón DL, Schlesinger R, Serrano B, Echeverry M, Silva JM, Varela D, Carvajal A, Azuero J. Performance of the artificial urinary sphincter implantation in men with urinary incontinence: Results from a contemporary long-term real-world nationwide analysis. Neurourol Urodyn. 2022;41(7):1573-1581. DOI: 10.1002/nau.25002
6. Léon P, Chartier-Kastler E, Rouprêt M, Ambrogi V, Mozer P, Phé V. Longterm functional outcomes after artificial urinary sphincter implantation in men with stress urinary incontinence. BJU Int. 2015;115(6):951-957. DOI: 10.1111/bju.12848
7. Велиев Е.И., Томилов А.А. Современные возможности диагностики и лечения недержания мочи у мужчин. М.: АО «Видаль Рус»; 2020.
8. Scott FB, Bradley WE, Timm GW. Treatment of urinary incontinence by an implantable prosthetic urinary sphincter. J Urol. 1974;112(1):75-80. DOI: 10.1016/s0022-5347(17)59647-0
9. Brant WO, Martins FE. Artificial urinary sphincter. Transl Androl Urol. 2017;6(4):682-694. DOI: 10.21037/tau.2017.07.31
10. Томилов А.А., Велиев Е.И., Голубцова Е.Н. Клинический случай первичной транскорпоральной имплантации манжеты искусственного мочевого сфинктера. Онкоурология. 2024;20(1):134-139. DOI: 10.17650/1726-9776-2024-20-1-134-139
11. Natali AN, Fontanella CG, Todros S, Pavan PG, Carmignato S, Zanini F, Carniel EL. Conformation and mechanics of the polymeric cuff of artificial urinary sphincter. Math Biosci Eng. 2020;17(4):3894-3908. DOI: 10.3934/mbe.2020216
12. Magera JS Jr, Elliott DS. Artificial urinary sphincter infection: causative organisms in a contemporary series. J Urol. 2008;180(6):2475-2478. DOI: 10.1016/j.juro.2008.08.021
13. Martins FE, Kulkarni SB, Köhler TS, eds. Textbook of Male Genitourethral Reconstruction. Springer Cham; 2020. DOI: 10.1007/978-3-030-21447-0
14. Agarwal DK, Linder BJ, Elliott DS. Artificial urinary sphincter urethral erosions: Temporal patterns, management, and incidence of preventable erosions. Indian J Urol. 2017;33(1):26-29. DOI: 10.4103/0970-1591.195758
15. Linder BJ, Rivera ME, Ziegelmann MJ, Elliott DS. Long-term Outcomes Following Artificial Urinary Sphincter Placement: An Analysis of 1082 Cases at Mayo Clinic. Urology. 2015;86(3):602-607. DOI: 10.1016/j.urology.2015.05.029
16. Schillebeeckx C, Deruyver Y, Beels E, De Ridder D, Van der Aa F. Longterm functional outcomes and patient satisfaction of artificial urinary sphincter implantation for male non-neurogenic incontinence: a retrospective study of 30-year experience in a tertiary centre. ICS 2021 Online. Melburn; 2021. (Accessed on 06.11.2023). URL: https://www.ics.org/2021/abstract/4
17. Dindo D, Demartines N, Clavien PA. Classification of surgical complications: a new proposal with evaluation in a cohort of 6336 patients and results of a survey. Ann Surg. 2004;240(2):205-213. DOI: 10.1097/01.sla.0000133083.54934.ae
Об авторах
А. А. ТомиловРоссия
Андрей Александрович Томилов — канд. мед. наук
Москва
Е. И. Велиев
Россия
Евгений Ибадович Велиев — д-р мед. наук; профессор
Москва
Е. Н. Голубцова
Россия
Елена Николаевна Голубцова — канд. мед. наук
Москва
З. А. Багателия
Россия
Зураб Антонович Багателия — д-р мед. наук, профессор
Москва
Рецензия
Для цитирования:
Томилов А.А., Велиев Е.И., Голубцова Е.Н., Багателия З.А. Ревизия искусственного мочевого сфинктера у мужчин: многолетний опыт одиночного центра. Вестник урологии. 2025;13(1):56-62. https://doi.org/10.21886/2308-6424-2025-13-1-56-62
For citation:
Tomilov A.A., Veliev E.I., Golubtsova E.N., Bagatelia Z.A. Revision of the artificial urinary sphincter in men: a long-term experience from a single centre. Urology Herald. 2025;13(1):56-62. (In Russ.) https://doi.org/10.21886/2308-6424-2025-13-1-56-62













































