Перейти к:
Оценка эффективности пептидного регулятора Везустен в лечении синдрома гиперактивного мочевого пузыря
https://doi.org/10.21886/2308-6424-2024-12-4-50-56
Аннотация
Введение. Гиперактивный мочевой пузырь (ГАМП) остаётся одним из самых трудноизлечимых заболеваний в нейроурологии. Ежегодно количество пациентов, обращающихся за помощью по поводу симптомов ГАМП, не уменьшается, в то время как патогенетического лечения до сих пор не разработано, что мотивирует исследователей пробовать новые подходы. Данное исследование посвящено оценке эффективности нового препарата Везустен у женщин с уродинамически подтверждённым ГАМП.
Цель исследования. Оценить эффективность пептидного регулятора Везустен у женщин с идиопатическим ГАМП в отношении снижения клинических и уродинамических проявлений детрузорной гиперактивности (ДГ).
Материалы и методы. В проспективное когортное исследование включены 20 женщин с диагнозом ГАМП и подтверждённой посредством комплексного уродинамического исследования ДГ. Пациентки посещали клинику 3 раза в неделю. Каждой выполнили 10 внутримышечных инъекций пептидного регулятора Везустен. По истечении месяца после последней инъекции женщины заполняли контрольный дневник мочеиспусканий, валидизированный опросник по оценке симптомов ГАМП Международного общества по континенции The Overactive Bladder Questionnaire (OAB-q) и проходили контрольное комплексное уродинамическое исследование (КУДИ).
Результаты. Нами были получены статистически значимые отличия по следующим показателям: количество дневных мочеиспусканий по дневнику мочеиспусканий сократилось с 14,0 [13,0; 16,3] до 11,0 [8,8; 12,0] раз (p < 0,001), субъективно пациенты стали реже отмечать эпизоды ургентного недержания (p = 0,004), при этом уродинамически увеличилась максимальная цистометрическая ёмкость с 267 [158; 332] до 320 [267; 433] мл. Субъективно пациентки отмечали улучшение согласно баллам опросника ГАМП (OAB-q): показатель снизился с 28 [22; 30] до 19 [14; 24] (p = 0,001), и снизилось количество эпизодов ноктурии с 4 до 2 (p < 0,001). Побочных эффектов от терапии не отмечалось ни у одной из пациенток.
Заключение. Данное исследование продемонстрировало статистически значимое улучшение субъективных симптомов ГАМП у женщин с ДГ, получивших курс лечения пептидным регулятором Везустен, однако для подтверждения эффективности требуются дальнейшие крупные плацебо-контролируемые исследования.
Ключевые слова
Для цитирования:
Ковалев Г.В., Лабетов И.А., Шакирова Р.Р., Шкарупа Д.Д. Оценка эффективности пептидного регулятора Везустен в лечении синдрома гиперактивного мочевого пузыря. Вестник урологии. 2024;12(4):50-56. https://doi.org/10.21886/2308-6424-2024-12-4-50-56
For citation:
Kovalev G.V., Labetov I.A., Shakirova R.R., Shkarupa D.D. The peptide regulator Vezusten in the management of overactive bladder syndrome: an efficacy evaluation. Urology Herald. 2024;12(4):50-56. (In Russ.) https://doi.org/10.21886/2308-6424-2024-12-4-50-56
Введение
Гиперактивный мочевой пузырь (ГАМП) — это симптомокомплекс, включающий в себя ургентность, учащённое мочеиспускание c потерей мочи или без, а также ноктурию [1][2]. Существует множество этиологических причин развития данного заболевания, и универсального патогенетического лечения для него не разработано [2]. Известно, что ГАМП оказывает существенное влияние на качество жизни и производительность труда [3]. Кроме того, на сегодняшний день доказано, что у людей, длительно страдающих от симптомов ГАМП, с большей долей вероятности развиваются тревожные и депрессивные состояния, что в конечном итоге приводит к социальной дезадаптации [3].
В современных клинических рекомендациях предлагается линейный путь коррекции данного заболевания, основанный на принципе «От менее инвазивных методов к более инвазивным» (поведенческая терапия, приём лекарственных препаратов, физиотерапевтическое лечение и минимально-инвазивные методики нейромодуляции или химической денервации и хирургическое лечение [4]). Тем не менее самым распространённым методом лечения ГАМП всё ещё остаётся медикаментозная терапия.
На сегодняшний день высокий уровень отказа пациентов от приёма конкурентных ингибиторов мускариновых рецепторов и B3-агонистов в связи с побочными эффектами и/или недостаточной эффективностью [5] и неоднозначные результаты рандомизированных контролируемых исследований (РКИ), сравнивающих исходы физиотерапевтического и хирургического лечения [6], подчёркивают актуальность поиска новых эффективных методов воздействия на нижние мочевые пути. В этом свете особую актуальность представляют новые методы медикаментозной коррекции ГАМП.
Одним из перспективных методов для изучения является использование регуляторных пептидов, в частности, в Российской Федерации зарегистрирован препарат Везустен [7 – 9]. Несмотря на многообещающие субъективные результаты у пациенток во время III фазы клинических исследований, влияние препарата на субъективные и объективные уродинамические параметры остаётся неисследованным [7].
Цель исследования: оценить эффективность пептидного регулятора Везустен у женщин с идиопатическим ГАМП в отношении снижения клинических и уродинамических проявлений детрузорной гиперактивности (ДГ).
Материалы и методы
Дизайн исследования. Проспективное когортное исследование, в которое мы включили 20 женщин с клиническими симптомами ГАМП и установленной по КУДИ детрузорной гиперактивностью. Исследование одобрено локальным этическим комитетом Клиники высоких медицинских технологий СПбГУ, протокол 01/24 от 18 января 2024 года. Все пациентки перед началом исследования заполнили информированное согласие на участие.
Диагноз подтверждался клинически, а также при наличии паттернов (фазовой или терминальной) детрузорной гиперактивности при проведении цистометрии наполнения. Наличие указанных паттернов было критерием включения в исследование. Критериями исключения стали повышенная чувствительность к действующему веществу и/или вспомогательному веществу в составе препарата, беременность или период грудного вскармливания, тяжёлые хронические сердечно-сосудистые заболевания или недавно перенесённые острые состояния (инфаркт миокарда, инсульт головного мозга и т. д.), опущение органов малого таза (I – III стадии по системе POP-Q), наличие острой инфекции мочевыводящих путей и наличие сопутствующей неврологической патологии (нейрогенный мочевой пузырь).
Протокол обследования. Обследование включало в себя подробный сбор анамнеза, заполнение дневников мочеиспусканий за 3 дня, заполнение стандартного опросника по оценке симптомов ГАМП. После оценки субъективных жалоб пациенткам было предложено пройти КУДИ, которое включало урофлоуметрию с определением объёма остаточной мочи, цистометрию наполнения и цистометрию опорожнения/исследование давление/поток). В случае, если пациентки принимали любые препараты, влияющие на функцию нижних мочевых путей (конкурентные ингибиторы мускариновых рецепторов, B3-агонисты), они должны были отменить приём за 2 недели до проведения КУДИ.
Протокол лечения. Женщины посещали клинику 3 раза в неделю на протяжении 4 недель (10 инъекций). Каждой из них при посещении выполняли внутримышечную инъекцию пептидного регулятора Везустен в дозировке 5 мг (1 флакон). Перед введением содержимое флакона растворяли в 2 мл воды для инъекций. По истечении одного месяца после последней инъекции терапии женщины заполняли валидизированные опросники и проходили контрольное КУДИ.
Оценка лечения. Субъективное снижение выраженности симптомов ГАМП, таких как учащённое мочеиспускание в дневное время, ноктурия и частота эпизодов ургентности, являлись первичной конечной точкой исследования. Первичная конечная точка эффективности была оценена с помощью дневника мочеиспусканий и стандартного опросника по оценке симптомов ГАМП Международного общества по континенции / The Overactive Bladder Questionnaire (OAB-q). Вторичной конечной точкой являлось улучшение уродинамических параметров, таких как максимальная цистометрическая ёмкость (МЦЕ), а также паттерны детрузорной гиперактивности (фазовой и терминальной). Вторичные конечные точки были оценены при помощи комплексного уродинамического исследования (КУДИ), состоящего из цистометрии наполнения и исследования давление/поток. Клинические симптомы и параметры уродинамики описаны в исследовании в соответствии со стандартизированной терминологией Международного общества континенции (International Continence Society) [10].
Статистический анализ. Все количественные данные описывались как среднее ± стандартное отклонение (для нормально распределённых признаков) либо медиана и межквартильный размах. Для оценки динамики результатов лечения использовали парный критерий Wilcoxon. При описании качественных данных использовали абсолютные значения (n) и проценты (%), для их анализа — критерий Pearson chi-square. В случае если не выполнялось допущение использования критерия (число ожидаемых значений в ячейке таблицы сопряжённости менее 5), применяли точный критерий Fisher. Отличия считали значимыми при p < 0,05. Все вычисления производили на языке R версии 4.1.3 (The R Foundation for Statistical Computing, Vienna, Austria).
Результаты
Исходные данные пациенток до лечения представлены в таблице.
Таблица. Сравнение основных параметров пациентов до и после терапии
Table. Comparison of basic patient`s parameters before and after treatment
Характеристика Characteristic | До лечения Before treatment (n = 20¹) | После лечения After treatment (n = 20¹) | P² |
Количество мочеиспусканий днём | Number of micturitions | 14,0 [ 3,0; 16,3] | 11,0 [ 8,8; 12,0] | < 0,001 |
Количество прокладок | Number of pads | 3,00 [ 2,00; 4,00] | 2,50 [ 2,00; 3,00] | 0,2 |
Эпизоды ургентного недержания | Urgent incontinence episodes | |||
2 | 0 (0%) | 3 (15%) | 0,004 |
3 | 4 (20%) | 3 (15%) | |
4 | 2 (10%) | 10 (50%) | |
5 | 9 (45%) | 2 (10%) | |
6 | 5 (25%) | 2 (10%) | |
МЦЕ | MCC | 267 [ 158; 332] | 320 [ 267; 433] | 0,026 |
Q max | 24 [ 20; 27] | 23 [ 19; 26] | 0,7 |
Q ave | 10,0 [ 6,8; 13,0] | 13,0 (9,0; 14,0) | 0,2 |
PVR | 10 [ 0; 20] | 0 [ 0; 13] | 0,2 |
Рdet Q max | 29 [ 24; 34] | 25 [ 20; 32] | 0,3 |
Фазовая ДГ | Phase DO | 14 (70%) | 12 (60%) | 0,5 |
Терминальная ДГ | Terminal DO | 10 (50%) | 6 (30%) | 0,2 |
Стресс-индуцированная ДГ | Stress-induced DO | 15 (75%) | 14 (70%) | 0,7 |
PdetMax | 42 [ 39; 48] | 35 [ 31; 43] | 0,029 |
Первое ощущение | First sensation | 72 [ 59; 104] | 112 [ 93; 117] | 0,033 |
Первый позыв | First desire | 125 [ 118; 155] | 137 [ 127; 165] | 0,4 |
Сильный позыв | Strong desire | 197 [ 159; 240] | 230 [ 126; 307] | 0,6 |
Баллы опросника ГАМП | OAB-q points | 28 [ 22; 30] | 19 [ 14; 24] | 0,001 |
Ноктурия | Nocturia | 4,00 [ 3,00; 4,00] | 2,00 [ 2,00; 3,00] | < 0,001 |
Примечания: 1) МЦЕ — максимальная цистометрическая ёмкость;
Q max — пиковая скорость мочеиспускания; Q ave — средняя скорость мочеиспускания;
PVR — объём остаточной мочи;
Pdet Qmax — давление детрузора во время пикового потока;
ДГ — детрузорная гиперактивность; ГАМП — гиперактивный мочевой пузырь
2) ¹ — медиана и межквартильное расстояние (Median [Q1; Q3]);
² — парный критерий Wilcoxon
Notes: 1) MCС — maximum cystometric capacity;
Q max — peak urinary flow rate; Q ave — mean urinary flow rate;
PVR — post-voiding residual volume;
Pdet Qmax — detrusor pressure during peak flow;
DO — detrusor overactivity; OAB — overactive bladder
2) ¹ — Median and interquartile range (Median [Q1; Q3]);
² — Wilcoxon paired sum rank test
Через 1 месяц после окончания терапии нами были получены статистически значимые отличия по следующим показателям: количество дневных мочеиспусканий по дневнику мочеиспусканий сократилось с 14,0 [ 13,0; 16,3] до 11,0 [ 8,8; 12] раз (p < 0,001), субъективно пациенты стали реже отмечать эпизоды ургентного недержания (p = 0,004), при этом уродинамически увеличилась медиана МЦЕ с 267 [ 158; 332] до 320 [ 267; 433] мл (рис.). Кроме того, наблюдалось статистически значимое снижение максимального давления детрузора в фазе накопления с 42 [ 39; 48] до 35 [ 31; 43], (p = 0,029). Прочие уродинамические параметры не изменились.
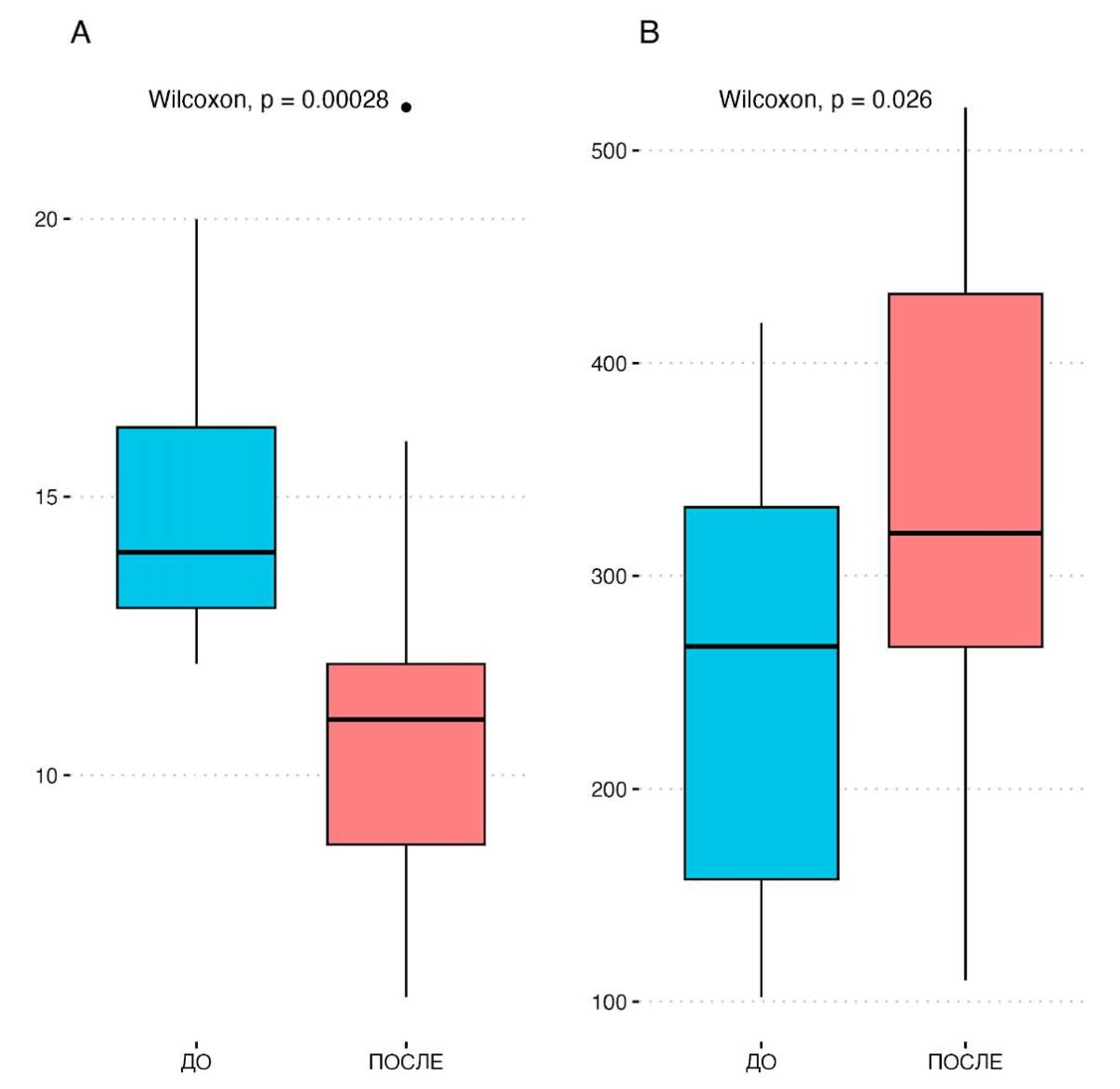
Рисунок. Динамика изменения показателей до и после терапии;
A — изменение количества мочеиспусканий (n) в сутки по дневнику;
B — изменение максимальной цистометрической ёмкости (мл) при КУДИ
Figure. Dynamics of changes in the parameters before and after therapy;
A — change in the number of daily urinations (n) according to the diary;
B — change in the maximum cystometric capacity (mL) according to urodynamic study
Субъективно пациентки отмечали улучшение согласно баллам опросника ГАМП (OAB): показатель снизился с 28 [ 22; 30] до 19 [ 14; 24] (p = 0,001), снизилось количество эпизодов ноктурии с 4 до 2 (p < 0,001). Побочных эффектов от терапии не отмечалось ни у одной из пациенток, за исключением незначительной болезненности (1 – 2 балла по ВАШ боли) в месте инъекции.
Обсуждение
Несмотря на достижения современной медицины, полное излечение от ГАМП остаётся нерешённой задачей. Определение новых точек патогенетического воздействия может расширить терапевтические возможности и повысить качество жизни пациентов.
В проведённом нами исследовании пептидный препарат Везустен приводил к уменьшению эпизодов ургентности, максимального давления детрузора в фазе накопления и увеличению максимальной цистометрической ёмкости мочевого пузыря у пациенток, что нашло отражение в снижении субъективных жалоб по параметрам опросников. Тем не менее, хотя нами и были выявлены положительные тенденции по снижению количества эпизодов подъёма детрузорного давления во время цистометрии наполнения, статистически значимого снижения данного показателя не было получено, что может говорить о необходимости дальнейших исследований с большей выборкой пациентов. С учётом этих находок потенциальное использование препарата может быть максимально эффективно у пациенток с симптомами ГАМП и снижением максимальной цистометрической емкости мочевого пузыря без признаков патологической детрузорной активности при КУДИ [11][12].
Описанный в литературе механизм действия регуляторных пептидов заключается в модулировании нейромышечного сигнала, выступая в качестве ко-медиаторов, выделяющихся из нервных окончаний вместе с классическими медиаторами [7]. Ранее проведённые исследования на экспериментальных животных показали, что Везустен способен нормализовать показатели сократительной способности детрузора на модели крыс с инфравезикальной обструкцией без увеличения остаточной мочи [7]. Несмотря на находки экспериментальных исследований in vitro, представленных в виде отчётов, и многообещающие результаты клинических испытаний II и III фазы, остаётся нераскрытым вопрос фармакокинетики препарата, определение которой является важной задачей для клинической фармакологии. В связи с этим рассмотрение оптимальных методов доставки препарата в ткани мочевого пузыря с минимизацией побочных эффектов и потенцированием эффективности может быть ценным для изучения в предстоящих клинических и фундаментальных исследованиях.
Ограничения исследования. Проведённое нами исследование имеет ряд ограничений. Одним из них является дизайн с отсутствием группы контроля, который не позволяет исключить плацебо-эффект. Кроме того, малый объём выборки и отсутствие периода отсроченного наблюдения может вносить дополнительные систематические ошибки. Однако это первое исследование препарата Везустен, оценивающее клинические симптомы совместно с уродинамическими параметрами пациентов с ГАМП в краткосрочном периоде. В дальнейшем интерес представляют сравнительные исследования комбинированного применения Везустена с конкурентными ингибиторами мускариновых рецепторов и/или BЗ-агонистами.
Заключение
Таким образом, препарат Везустен продемонстрировал эффективность и безопасность в купировании субъективных проявлений ГАМП у женщин с ДГ, а также проявил потенциал в отношении влияния на показатели КУДИ. Для уточнения спектра возможностей воздействия полипептидов мочевого пузыря на объективные уродинамические параметры требуются дальнейшие многоцентровые плацебо-контролируемые исследования с более крупной выборкой.
Список литературы
1. Abrams P, Cardozo L, Fall M, Griffiths D, Rosier P, Ulmsten U, Van Kerrebroeck P, Victor A, Wein A; Standardisation Sub-Committee of the International Continence Society. The standardisation of terminology in lower urinary tract function: report from the standardisation sub-committee of the International Continence Society. Urology. 2003;61(1):37-49. DOI: 10.1016/s0090-4295(02)02243-4
2. Peyronnet B, Mironska E, Chapple C, Cardozo L, Oelke M, Dmochowski R, Amarenco G, Gamé X, Kirby R, Van Der Aa F, Cornu JN. A Comprehensive Review of Overactive Bladder Pathophysiology: On the Way to Tailored Treatment. Eur Urol. 2019;75(6):988-1000. DOI: 10.1016/j.eururo.2019.02.038
3. Coyne KS, Sexton CC, Kopp ZS, Ebel-Bitoun C, Milsom I, Chapple C. The impact of overactive bladder on mental health, work productivity and health-related quality of life in the UK and Sweden: results from EpiLUTS. BJU Int. 2011;108(9):1459-1471. DOI: 10.1111/j.1464-410X.2010.10013.x
4. Hutchinson A, Nesbitt A, Joshi A, Clubb A, Perera M. Overactive bladder syndrome: Management and treatment options. Aust J Gen Pract. 2020;49(9):593-598. DOI: 10.31128/AJGP-11-19-5142
5. Chapple CR, Nazir J, Hakimi Z, Bowditch S, Fatoye F, Guelfucci F, Khemiri A, Siddiqui E, Wagg A. Persistence and Adherence with Mirabegron versus Antimuscarinic Agents in Patients with Overactive Bladder: A Retrospective Observational Study in UK Clinical Practice. Eur Urol. 2017;72(3):389-399. DOI: 10.1016/j.eururo.2017.01.037
6. Amundsen CL, Richter HE, Menefee SA, Komesu YM, Arya LA, Gregory WT, Myers DL, Zyczynski HM, Vasavada S, Nolen TL, Wallace D, Meikle SF. OnabotulinumtoxinA vs Sacral Neuromodulation on Refractory Urgency Urinary Incontinence in Women: A Randomized Clinical Trial. JAMA. 2016;316(13):1366-1374. DOI: 10.1001/jama.2016.14617
7. Пушкарь Д.Ю., Куприянов Ю.А., Гамидов С.И., Кривобородов Г.Г., Спивак Л.Г., Аль-Шукри С.Х., Лерман Д.М., Гомберг В.Г., Богдан Е.Н., Щукин В.Л., Чибиров К.Х., Гелашвили В.В., Гураль А.К., Кешишев Н.Г., Старосельская М.А., Бастрикова Н.А. Оценка безопасности и эффективности лекарственного препарата ВЕЗУСТЕН® у пациентов с гиперактивным мочевым пузырем. Урология. 2022;(3):42-51. DOI: 10.18565/urology.2022.3.42-51
8. Кузьмин И.В. Биорегулирующая терапия гиперактивного мочевого пузыря. Урология. 2024;(2):92-99. DOI: 10.18565/urology.2024.2.92-99
9. Галкина Н.Г., Галкин А.В. Оценка эффективности лекарственного препарата Везустен® у пациенток с гиперактивным мочевым пузырём и хроническим рецидивирующим циститом. Вестник урологии. 2024;12(3):36-45. DOI: 10.21886/2308-6424-2024-12-3-36-45
10. Wein AJ, Rovner ES. Definition and epidemiology of overactive bladder. Urology. 2002;60(5 Suppl 1):7-12; discussion 12. DOI: 10.1016/s0090-4295(02)01784-3
11. Guralnick ML, Grimsby G, Liss M, Szabo A, O'Connor RC. Objective differences between overactive bladder patients with and without urodynamically proven detrusor overactivity. Int Urogynecol J. 2010;21(3):325-329. DOI: 10.1007/s00192-009-1030-7
12. Haylen BT, Chetty N, Logan V, Schulz S, Verity L, Law M, Zhou J. Is sensory urgency part of the same spectrum of bladder dysfunction as detrusor overactivity? Int Urogynecol J Pelvic Floor Dysfunct. 2007;18(2):123-128. DOI: 10.1007/s00192-006-0165-z
Об авторах
Г. В. КовалевРоссия
Ковалев Глеб Валерьевич — канд. мед. наук.
Санкт-Петербург
Конфликт интересов:
Нет
И. А. Лабетов
Россия
Лабетов Иван Антонович.
Санкт-Петербург
Конфликт интересов:
Нет
Р. Р. Шакирова
Россия
Шакирова Резеда Радиславовна.
Санкт-Петербург
Конфликт интересов:
Нет
Д. Д. Шкарупа
Россия
Шкарупа Дмитрий Дмитриевич — д-р мед. наук.
Санкт-Петербург
Конфликт интересов:
Нет
Рецензия
Для цитирования:
Ковалев Г.В., Лабетов И.А., Шакирова Р.Р., Шкарупа Д.Д. Оценка эффективности пептидного регулятора Везустен в лечении синдрома гиперактивного мочевого пузыря. Вестник урологии. 2024;12(4):50-56. https://doi.org/10.21886/2308-6424-2024-12-4-50-56
For citation:
Kovalev G.V., Labetov I.A., Shakirova R.R., Shkarupa D.D. The peptide regulator Vezusten in the management of overactive bladder syndrome: an efficacy evaluation. Urology Herald. 2024;12(4):50-56. (In Russ.) https://doi.org/10.21886/2308-6424-2024-12-4-50-56
JATS XML













































