Перейти к:
Определение оптимальных точек экстракорпорального акустического воздействия ультразвуковым амплитудно-модулированным сигналом на мочеточниковый стент с целью профилактики его инкрустации в эксперименте
https://doi.org/10.21886/2308-6424-2021-9-3-70-78
Аннотация
Введение. Инкрустация и формирование биоплёнок на поверхности мочеточниковых стентов остаются самыми грозными осложнениями внутреннего дренирования верхних мочевыводящих путей. На сегодняшний день ведётся множество поисковых научных исследований по борьбе с данными осложнениями. Отсутствие решения данной проблемы неизбежно оставляет отпечаток на конечных результатах лечения и экономических потерях. Перспективным и мало освещённым остаётся вопрос использования физических методов воздействия на мочеточниковый стент, в частности применение экстракорпорального ультразвукового акустичесткого воздействия.
Цель исследования. Определить оптимальные точки экстракорпорального акустического воздействия низкочастотным ультразвуковым амплитудно-модулированным сигналом на установленный уретеральный стент в эксперименте.
Материалы и методы. Сконструирован оригинальный прибор, принципом работы которого является генерация амплитудно-модулированного ультразвукового сигнала в двух режимах – импульсном и постоянном. В качестве экспериментального животного в эксперименте участвовала половозрелая беспородная собака, которой посредством лапаротомии и цистотомии устанавливали мочеточниковый стент. Интраоперационно к кожному покрову животного прикладывали излучатель разработанного прибора по ранее обозначенным топографо-анатомическим ориентирам. Одновременно через лапаротомную рану к соответствующему уровню мочеточника прикладывали анализатор шума ультразвуковых волн, трёхкратно выполняя замеры показателей интенсивности ультразвука в двух режимах работы прибора.
Результаты. В импульсном режиме работы для верхней трети мочеточника наибольшая интенсивность ультразвуковой волны (123,67 dB) достигается по задней аксиллярной линии. Для средней трети мочеточника наилучшие показатели интенсивности ультразвука получены по задней аксиллярной линии (115 dB). Для нижней трети мочеточника наибольшая интенсивность ультразвука (113,67 dB) отмечена по средней аксиллярной линии. При работе инструментом в постоянном режиме наилучшие показатели интенсивности ультразвуковой волны в проекции верхней, средней и нижней третей мочеточника достигаются по задней аксиллярной линии, составляя 118,67 dB, 117 dB и 116,67 dB соответственно. При работе инструментом в постоянном режиме отмечен чрезмерный тепловой эффект, проявляющийся гиперемией и гипертермией кожного покрова животного, фасцикулярными сокращениям мышц, что потенциально может привести к термическому ожогу и непереносимости процедуры.
Заключение. Безопасным режимом работы прибора является импульсный. Оптимальным точками приложения излучателя инструмента являются для верхней трети и средней трети мочеточника – задняя подмышечная линия, для нижней трети – средняя подмышечная линия.
Для цитирования:
Цуканов А.Ю., Ахметов Д.С., Новиков А.А., Негров Д.А., Путинцева А.Р., Семикина С.П. Определение оптимальных точек экстракорпорального акустического воздействия ультразвуковым амплитудно-модулированным сигналом на мочеточниковый стент с целью профилактики его инкрустации в эксперименте. Вестник урологии. 2021;9(3):70-78. https://doi.org/10.21886/2308-6424-2021-9-3-70-78
For citation:
Tsukanov A.Yu., Akhmetov D.S., Novikov A.A., Negrov N.A., Putintseva A.R., Semikina S.P. Extracorporeal ultrasound exposure by the low-frequency acoustic amplitude-modulated signal on a ureteral stent for preventing its incrustation: experimental determination of optimal application points. Urology Herald. 2021;9(3):70-78. (In Russ.) https://doi.org/10.21886/2308-6424-2021-9-3-70-78
Введение
Мочеточниковые стенты рутинно используются в урологической практике для обеспечения адекватного пассажа мочи при обструкции верхних мочевыводящих путей в различных клинических ситуациях [1][2].
Наличие инородного тела в просвете мочеточника неизбежно сопряжено с осложнениями, связанными с самим фактором его присутствия. Безусловно осложнения могут проявляться от клинически малозначимых до жизнеугрожающих, но в любом случае неразрывно связаны с такими феноменами, как инкрустация и формирование биоплёнок [3][4]. Предыдущие исследования показали, что до 70% удалённых стентов содержат на своей поверхности бактерии [5], образующие биоплёнки, устойчивые к большому ряду антибиотиков. Выраженная инкрустация может привести к серьёзным последствиям вплоть до угрожающего жизни уросепсиса. В мировой периодической печати регулярно появляются работы, посвящённые борьбе с этими осложнениями.
Несмотря на многочисленные инновации и улучшения в дизайне и материалах стента, поиск решения данной проблемы остаётся актуальным и на сегодняшний день. Наибольшей биоинертностью обладают полимерные материалы, самыми распространёнными из которых являются полиуретан, силикон с их многочисленными модификациями [6]. Ведётся множество поисковых научных работ по созданию биоинертных покрытий, наносимых на поверхность полимерных стентов, будь то покрытия из серебра, гепарина, триклозана и др. [7][8][9][10][11]. Перспективным направлением является создание биодеградируемых материалов. Однако невозможность контроля скорости разложения этих материалов ограничивает оптимальные сроки дренирования [12]. Несмотря на использование разнообразных материалов с различными физическими характеристиками, ни один из них не устойчив к осаждению кристаллов и микроорганизмов, что наглядно иллюстрирует сложность механизмов этих процессов [13].
Отсутствие решения данной проблемы сказывается на результатах лечения, ограничивая тем самым оптимальные сроки дренирования. Несостоятельность дренажа в конечном итоге приводит к необходимости частой его замены.
Помимо разработки новых материалов и покрытий, малоосвещённым, но перспективным вариантом решения является использование физических методов воздействия на мочеточниковый стент. Исследования посвящённые ультразвуковой очистке мочевых дренажей, продемонстрированы на катетерах Фолея в единичных публикациях [14][15][16]. Предложенные варианты данного типа воздействия реализуются контактно, что в значительной мере сдерживает их клиническое применение, в частности в случае внутреннего дренирования верхних мочевыводящих путей. Создание способа неинвазивного воздействия представляется перспективным и требует дальнейшего изучения.
Цель исследования: определить оптимальные точки экстракорпорального акустического воздействия низкочастотным ультразвуковым амплитудно-модулированным сигналом на установленный уретеральный стент в эксперименте.
Материалы и методы
Коллективом авторов был рассчитан, спроектирован и изготовлен ультразвуковой инструмент, основным принципом работы которого является генерация амплитудно-модулированного ультразвукового сигнала, рабочая часть которого выполнена в виде плоского диска диаметром 30 мм из титанового сплава ВТ3-1. Излучатель конструктивно размещен в корпусе типа «пистолет». Физические характеристики ультразвукового воздействия: Am – 10 мкм, f – 20 кГц, мощность –30 Вт [17].
В качестве экспериментального животного использована половозрелая беспородная собака (самка) весом 20,3 кг в возрасте 3 – 4-х лет, соматически здоровая, без признаков травматических повреждений.
Данный эксперимент является фрагментом работы по изучению эффективности низкочастотного амплитудно-модулированного ультразвука для профилактики инкрустации мочеточникового стента, получившей одобрение локального этического комитета ОмГМУ (протокол № 107 от 02.10.2018 года). Животное содержали в отдельном помещении в металлической клетке в условиях регулируемого искусственного освещения, температура воздуха составляла в среднем 25°С, собака получала полнорационный корм и питьевую фильтрованную воду без ограничений. Условия содержания животного и порядок работы с ним строго соответствовали положениям, принятыми Европейской конвенцией по защите позвоночных животных, используемых для исследовательских и иных научных целей, Федерацией европейских ассоциаций по науке о лабораторных животных, Международным советом по науке о лабораторных животных, законодательству Российской Федерации
Животное выдержало карантин в течение пяти суток, а также было предварительно обследовано на наличие инфекции мочевыводящих путей (ОАМ, бак посев мочи). На фоне премедикации (сульфат атропина 0,1 мг/кг, подкожно) и общей анестезии (Propofol 1%, 10 мг/кг, в/в; Zoletil 100, 8 мг/кг, в/в) кожный покров животного подвергали предварительному бритью, троекратно обработав раствором спиртового антисептика. Далее выполнили нижнесрединную лапаротомию. По передней стенке мочевого пузыря производили разрез длиной 3 см. В устье левого мочеточника вводили струну-проводник до полостной системы левой почки. По струнепроводнику в устье левого мочеточника установили мочеточниковый полиуретановый стент 5 CH длиной 20 см, пальпаторно осуществляя контроль удовлетворительного стояния стента в просвете мочеточника и лоханке левой почки. Ушивали мочевой пузырь непрерывным двурядным швом.
Оценку параметров ультразвуковой волны непосредственно на уровне мочеточника проводили следующим образом: на поверхности кожного покрова животного условно обозначали топографические ориентиры (передняя (ПП), средняя (СП) и задняя (ЗП) подмышечные линии). Излучатель после предварительного нанесения акустического геля прикладывали к кожному покрову в точках прямоугольной проекции верхней (В/3), средней (С/3) и нижней (Н/3) третей мочеточника по каждой из трех вышеуказанных линий (рис. 1).
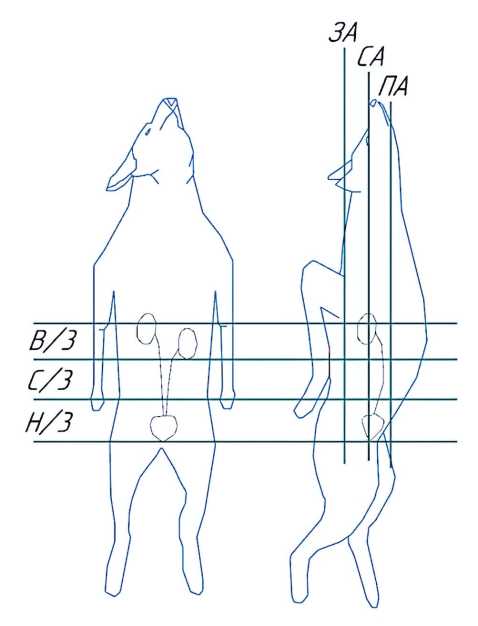
Рисунок 1. Условные топографические ориентиры проекции мочеточника
Figure 1. Ureter's conditional topographic landmarks
Через лапаротомную рану к соответствующему уровню мочеточника располагали анализатор шума ультразвуковых волн «АССИСТЕНТ» S/U30 приборостроительной компании ООО «НТМЗащита». Из каждой точки воздействие ультразвуком осуществляли трижды с интервалом в 1 минуту, фиксируя уровень шума (рис. 2).
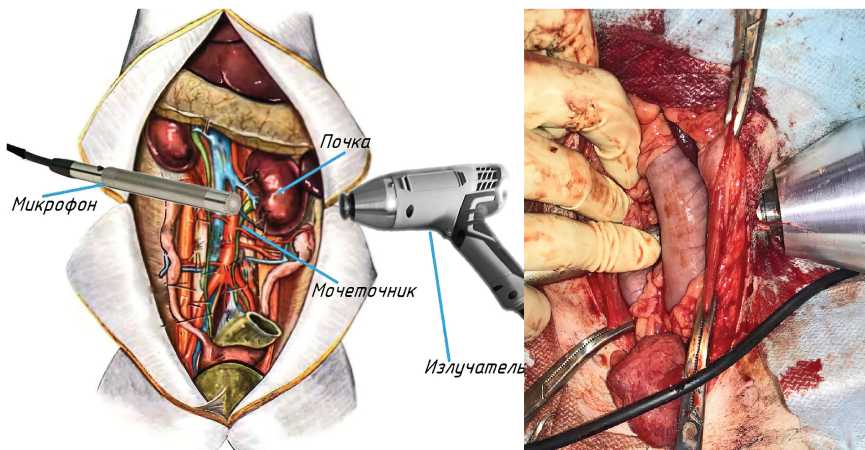
Рисунок 2. Схема эксперимента
Figure 2. Experiment scheme
После завершения замеров брюшную полость промывали физиологическим раствором, рану ушивали послойно. Обрабатывали кожные швы раствором бриллиантовой зелени.
Звуковая волна, распространяющаяся с поверхности тела животного, проходит через несколько слоёв тканей, разнородных по своей плотности и ультразвуковой проводимости (кожа и её придатки, подкожно-жировой слой, мышцы, фасции, полые и паренхиматозные органы и т.д.). Проходя через границу раздела сред, ультразвуковая волна изменяет свою интенсивность, т.к. часть энергии ультразвуковой волны проходит в нижележащий слой, а часть отражается в противоположном направлении (рис. 3.)
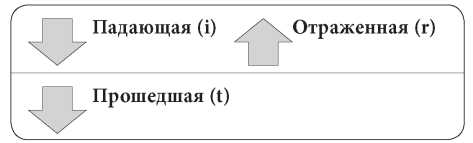
Рисунок 3. Схема прохождения и отражения звуковой волны на границе раздела сред
Figure 3. Scheme of sonotransmission at the interface between media
Исходя из анатомо-физиологических особенностей на каждом из трёх уровней мочеточника (В/3, С/3, Н/3), по каждой из трёх условных топографических линий (ПП, СП, ЗП) на пути ультразвуковой волны расположены органы и ткани, приведённые в таблице 1.
Таблица 1. Органы и ткани, расположенные на пути прохождения ультразвуковой волны
Table 1. Organs and tissues located along the path of sonotransmission

Примечание: В/3 – верхняя треть мочеточника; С/3– средняя треть мочеточника; Н/3 – нижняя треть мочеточника; ПП – передняя подмышечная линия; СП – средняя подмышечная линия; ЗП – задняя подмышечная линия.
Note: U/3 – the ureteral upper third; M/3 – the ureteral middle third; L/3 – the ureteral lower third; AA – the anterior axillary line; MA – the middle axillary line; PA – the posterior axillary line.
Разработанный ультразвуковой прибор имеет два режима работы – импульсный и постоянный, – что отражается на количестве и способе передачи энергии, передаваемой мягким тканям.
С помощью анализатора шума измерена интенсивность ультразвуковых волн, достигающих мочеточника в ранее обозначенных топографоанатомических ориентирах, раздельно для импульсного и постоянного режимов работы.
Результаты
За эталонную среду распространения ультразвуковых волн в эксперименте принята дистиллированная вода. Опытным путём определена интенсивность волн, генерируемых разработанным ультразвуковым инструментом в импульсном и постоянном режимах. Получены следующие значения: Iимп в воде = 120 dB, Iпост в воде = 134 dB.
Измеренные параметры прохождения ультразвуковой волны через биологические среды представлены в таблицах 2 – 3.
Таблица 2. Интенсивность ультразвуковой волны при работе прибора в импульсном режиме
Table 2. Pulsed mode ultrasonic wave intensity
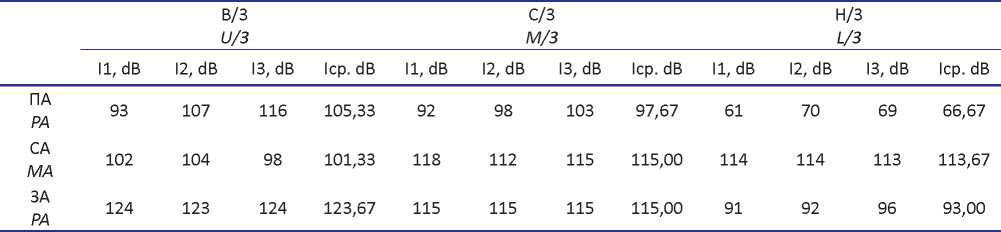
Примечание: В/3 – верхняя треть мочеточника; С/3– средняя треть мочеточника; Н/3 – нижняя треть мочеточника; ПП – передняя подмышечная линия; СП – средняя подмышечная линия; ЗП – задняя подмышечная линия.
Note: U/3 – the ureteral upper third; M/3 – the ureteral middle third; L/3 – the ureteral lower third; AA – the anterior axillary line; MA – the middle axillary line; PA – the posterior axillary line.
Таблица 3. Интенсивность ультразвуковой волны при работе прибора в постоянном режиме
Table 3. Permanent mode ultrasonic wave intensity
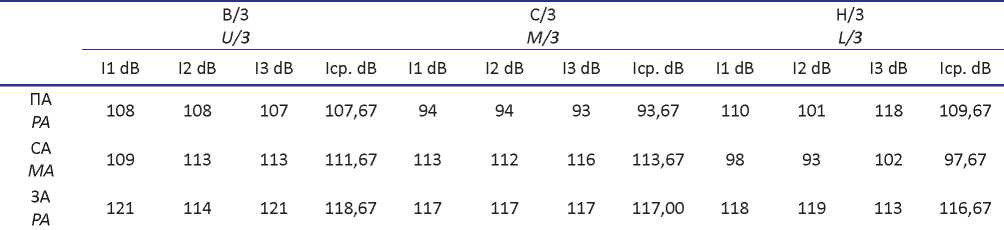
Примечание: В/3 – верхняя треть мочеточника; С/3– средняя треть мочеточника; Н/3 – нижняя треть мочеточника; ПП – передняя подмышечная линия; СП – средняя подмышечная линия; ЗП – задняя подмышечная линия.
Note: U/3 – the ureteral upper third; M/3 – the ureteral middle third; L/3 – the ureteral lower third; AA – the anterior axillary line; MA – the middle axillary line; PA – the posterior axillary line.
В импульсном режиме работы для верхней трети мочеточника наибольшая интенсивность ультразвуковой волны (123,67 dB) достигается по задней аксиллярной линии.
Для средней трети мочеточника наилучшие показатели интенсивности ультразвука получены как по средней, так и задней аксиллярным линиям (115 dB), однако при выполнении трёхкратных замеров наиболее стабильные показатели достигнуты по задней аксиллярной линии.
Для нижней трети мочеточника наибольшая интенсивность ультразвука (113,67 dB) отмечена по средней аксиллярной линии.
При работе инструментом в постоянном режиме наилучшие показатели интенсивности ультразвуковой волны в проекции верхней, средней и нижней третей мочеточника достигаются по задней аксиллярной линии, составляя 118,67 dB, 117 dB и 116,67 dB соответственно (табл. 3).
Однако при работе инструментом в постоянном режиме ввиду большего количества энергии, передаваемого излучателем, отмечен чрезмерный тепловой эффект, который приводил к гипертермии и гиперемии кожного покрова животного, фасцикулярным сокращениям мышц, что потенциально может привести к термическому ожогу и непереносимости процедуры при экстраполяции результатов данного эксперимента на организм человека. При работе в импульсном режиме данных явлений не отмечено.
Обсуждение
Высокий потенциал, заложенный в использовании ультразвуковой энергии для предотвращения образования биоплёнок и отложения солевых депозитов на поверхности мочевых дренажей, продемонстрирован лишь в немногочисленных исследованиях, большая часть которых посвящена катетерам Фолея, и реализованных на экспериментальных моделях катетеризированного мочевого пузыря путём контактного воздействия [14][15][16]. Контактное воздействие на мочеточниковый стент значительно ограничивает применение данной технологии, тем самым определяя перспективность создания неинвазивного метода воздействия на дренаж. Однако при исследовании применение ультразвука для очистки мочеточникового стента в неинвазивном аспекте возникает неизбежная необходимость изучения влияния разнородных биологических сред на распространение ультразвуковых колебаний и связанные с этим потери эффективности излучения. Механизм ультразвуковой очистки поверхности дренажа обусловлен воздействием ударной волны, возникающей в результате кавитации пузырьков жидкости, которые проникают в щели и поры между загрязнениями и поверхностью стента.
Интенсивность звука – средняя по времени энергия, переносимая звуковой волной через единичную площадку, перпендикулярную к направлению распространения волны, в единицу времени. Поскольку в данной работе рассмотрен метод неинвазивного воздействия, прохождение ультразвуковых колебаний через границы раздела биологических сред сопровождается снижением интенсивности ультразвуковой волны, достигающей до мочеточникового стента. Полученные в результате эксперимента данные позволили определить интенсивность ультразвуковой волны на глубине установленного мочеточникового стента. Исходя из этих данных выделены оптимальные точки, для осуществления неинвазивного акустического ультразвукового воздействия с минимальной потерей интенсивности.
Полученные результаты можно соотнести с таблицей 1 и сделать вывод о том, что наилучшие параметры интенсивности достигаются в тех анатомо-топографических точках, где на пути ультразвуковой волны встречается меньшее количество границ раздела сред и отсутствуют полые органы и костные структуры.
Заключение
Применение экстракорпорального акустического воздействия ультразвуковым амплитудномодулированным сигналом для санации мочеточниковых стентов является возможным. Безопасным режимом работы прибора является импульсный. Оптимальными точками приложения излучателя инструмента с минимальными потерями интенсивности ультразвуковой волны в экспериментальной модели являются для верхней трети и средней трети мочеточника – задняя подмышечная линия, для нижней трети – средняя подмышечная линия. Необходимы дальнейшие исследования по изучению эффективности и безопасности данного неинвазивного ультразвукового воздействия.
Список литературы
1. Ordonez M, Hwang EC, Borofsky M, Bakker CJ, Gandhi S, Dahm P. Ureteral stent versus no ureteral stent for ureteroscopy in the management of renal and ureteral calculi. Cochrane Database Syst Rev. 2019;2(2):CD012703. DOI: 10.1002/14651858.CD012703.pub2
2. Трусов П.В., Гусев А.А. Лечение камней почек: стандарты и инновации. Вестник урологии. 2019;7(2):93-111. DOI: 10.21886/2308-6424-2019-7-2-93-111
3. Zumstein V, Betschart P, Albrich WC, Buhmann MT, Ren Q, Schmid HP, Abt D. Biofilm formation on ureteral stents – Incidence, clinical impact, and prevention. Swiss Med Wkly. 2017;147:w14408. DOI: 10.4414/smw.2017.14408
4. Pengfei S, Yutao L, Jie Y, Wuran W, Yi D, Hao Z, Jia W. The results of ureteral stenting after ureteroscopic lithotripsy for ureteral calculi: a systematic review and meta-analysis. J Urol. 2011;186(5):1904-9. DOI: 10.1016/j.juro.2011.06.066
5. El-Azizi M, Rao S, Kanchanapoom T, Khardori N. In vitro activity of vancomycin, quinupristin/dalfopristin, and linezolid against intact and disrupted biofilms of staphylococci. Ann Clin Microbiol Antimicrob. 2005;4:2. DOI: 10.1186/1476-0711-4-2
6. Liatsikos E, Kallidonis P, Stolzenburg JU, Karnabatidis D. Ureteral stents: past, present and future. Expert Rev Med Devices. 2009;6(3):313-24. DOI: 10.1586/erd.09.5
7. Коган М.И., Мойсюк Я.Г., Шкодкин С.В., Сайдулаев Д.А., Идашкин Ю.Б. Эффективность использования стентов с наноструктурным покрытием при трансплантации почки (предварительные результаты). Урология. 2015;1:58-6. eLIBRARY ID: 23608466
8. Cauda F, Cauda V, Fiori C, Onida B, Garrone E. Heparin coating on ureteral Double J stents prevents encrustations: an in vivo case study. J Endourol. 2008;22(3):465-72. DOI: 10.1089/end.2007.0218
9. Cadieux PA, Chew BH, Knudsen BE, Dejong K, Rowe E, Reid G, Denstedt JD. Triclosan loaded ureteral stents decrease proteus mirabilis 296 infection in a rabbit urinary tract infection model. J Urol. 2006;175(6):2331-5. DOI: 10.1016/S0022-5347(06)00252-7
10. Gultekinoglu M, Kurum B, Karahan S, Kart D, Sagiroglu M, Ertaş N, Haluk Ozen A, Ulubayram K. Polyethyleneimine brushes effectively inhibit encrustation on polyurethane ureteral stents both in dynamic bioreactor and in vivo. Mater Sci Eng C Mater Biol Appl. 2017;71:1166-74. DOI: 10.1016/j.msec.2016.11.125
11. John T, Rajpurkar A, Smith G, Fairfax M, Triest J. Antibiotic pretreatment of hydrogel ureteral stent. J Endourol. 2007;21(10):1211-6. DOI: 10.1089/end.2007.9904
12. Wang L, Yang G, Xie H, Chen F. Prospects for the research and application of biodegradable ureteral stents: from bench to bedside. J Biomater Sci Polym Ed. 2018;29(14):1657-66. DOI: 10.1080/09205063.2018.1498184
13. Tunney MM, Jones DS, Gorman SP. Biofilm and biofilmrelated encrustation of urinary tract devices. Methods Enzymol. 1999;310:558-66. DOI: 10.1016/s0076-6879(99)10043-0
14. Hazan Z, Zumeris J, Jacob H, Raskin H, Kratysh G, Vishnia M, Dror N, Barliya T, Mandel M, Lavie G. Effective prevention of microbial biofilm formation on medical devices by low-energy surface acoustic waves. Antimicrob Agents Chemother. 2006;50(12):4144-52. DOI: 10.1128/AAC.00418-06
15. Kopel M, Degtyar E, Banin E. Surface acoustic waves increase the susceptibility of Pseudomonas aeruginosa biofilms to antibiotic treatment. Biofouling. 2011;27(7):701-10. DOI: 10.1080/08927014.2011.597051
16. Dror N, Mandel M, Hazan Z, Lavie G. Advances in microbial biofilm prevention on indwelling medical devices with emphasis on usage of acoustic energy. Sensors (Basel). 2009;9(4):2538-54. DOI: 10.3390/s90402538
17. Патент РФ на изобретение № 2703472/17.10.2019. Бюл. №29. Новиков А. А., Цуканов А. Ю., Ахметов Д. С. Способ неинвазивной санации мочеточниковых стентов. Доступно по: https://edrid.ru/en/rid/219.017.d836.html Ссылка активна на 20.08.2021
Об авторах
А. Ю. ЦукановРоссия
Антон Юрьевич Цуканов – докт. мед. наук, профессор; заведующий кафедрой хирургических болезней и урологии
644099, г. Омск, ул. Ленина, д. 12
тел.: + 7 (913) 967-36-76
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
Д. С. Ахметов
Россия
Данияр Сарсенбаевич Ахметов – аспирант кафедры хирургических болезней и урологии
644099, г. Омск, ул. Ленина, д. 12
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
А. А. Новиков
Россия
Алексей Алексеевич Новиков – докт. тех. наук, профессор кафедры машиностроение и материаловедение
644050, г. Омск, пр. Мира, д. 11
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
Д. А. Негров
Россия
Дмитрий Анатольевич Негров – канд. тех. наук, доцент кафедры машиностроение и материаловедение
644050, г. Омск, пр. Мира, д. 11
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
А. Р. Путинцева
Россия
Александра Рустамовна Путинцева – аспирант кафедры машиностроение и материаловедение
644050, г. Омск, пр. Мира, д. 11
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
С. П. Семикина
Россия
София Павловна Семикина – клинический ординатор кафедры хирургических болезней и урологии
644099, г. Омск, ул. Ленина, д. 12
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
Рецензия
Для цитирования:
Цуканов А.Ю., Ахметов Д.С., Новиков А.А., Негров Д.А., Путинцева А.Р., Семикина С.П. Определение оптимальных точек экстракорпорального акустического воздействия ультразвуковым амплитудно-модулированным сигналом на мочеточниковый стент с целью профилактики его инкрустации в эксперименте. Вестник урологии. 2021;9(3):70-78. https://doi.org/10.21886/2308-6424-2021-9-3-70-78
For citation:
Tsukanov A.Yu., Akhmetov D.S., Novikov A.A., Negrov N.A., Putintseva A.R., Semikina S.P. Extracorporeal ultrasound exposure by the low-frequency acoustic amplitude-modulated signal on a ureteral stent for preventing its incrustation: experimental determination of optimal application points. Urology Herald. 2021;9(3):70-78. (In Russ.) https://doi.org/10.21886/2308-6424-2021-9-3-70-78













































