Перейти к:
Минимально-инвазивная органосохраняющая хирургия рака почки: нефронсберегающий алгоритм
https://doi.org/10.21886/2308-6424-2026-14-1-118-130
Аннотация
Введение. Резекция почки — золотой стандарт лечения локального рака почки. Для дальнейшего улучшения результатов органосохраняющей хирургии пациентов с локальным раком почки назрела необходимость смены стратегии лечения. Лечение должно быть основано на оптимизации методики резекции почки с целью сохранения максимального количества функциональных единиц почки — нефронов.
Цель исследования. Разработка алгоритма роботассистированной нефронсберегающей резекции почки с оценкой первоначальных клинических результатов.
Материалы и методы. В работе изложены принципы нефронсберегающей хирургии и подробно описан последовательный алгоритм выполнения резекции почки. Рассмотрены особенности выполнения методики в зависимости от сложности оперативного пособия. Проанализированы результаты первых 100 операций по нефронсберегающей методике в период с 2020 по 2021 год на базе ММНКЦ им. С.П. Боткина: 70 лапароскопических и 30 робот-ассистированных резекций почки в рамках проспективного когортного исследования с учётом функциональных результатов через год после операции.
Результаты. Большинство пациентов перед операцией имело стадию сT1а — 70 пациентов, стадию сT1b — 14 пациентов, стадию сТ2 — 4 пациента. Кистозная опухоль обнаружена у 12 пациентов. Частота применения тепловой ишемии составила 14% при среднем времени 9 минут и ни в одном случае не превышала 25 минут. Частота отрицательного хирургического края — 97%. Вероятность достижения «трифекты» составила 89%, а «пентафекты» — 55%.
Заключение. Применение принципов нефронсберегающей хирургии позволяет улучшить функциональные результаты органосохраняющей хирургии. Представленный подробный алгоритм выполнения резекции почки может быть полезен при старте программы минимально-инвазивной резекции почки.
Ключевые слова
Для цитирования:
Серёгин А.А., Шустицкий Н.А., Серёгин А.В., Колонтарев К.Б., Говоров А.В., Раснер П.И., Тарасов Р.А., Нифталыев А.Э., Золотарёва К.П., Пушкарь Д.Ю., Лоран О.Б. Минимально-инвазивная органосохраняющая хирургия рака почки: нефронсберегающий алгоритм. Вестник урологии. 2026;14(1):118-130. https://doi.org/10.21886/2308-6424-2026-14-1-118-130
For citation:
Seregin A.A., Shustitskiy N.A., Seregin A.V., Kolontarev K.B., Govorov A.V., Rasner P.I., Tarasov R.A., Niftaliyev A.E., Zolotareva K.P., Pushkar D.Yu., Loran O.B. Nephron-sparing algorithm for minimally invasive partial nephrectomy. Urology Herald. 2026;14(1):118-130. (In Russ.) https://doi.org/10.21886/2308-6424-2026-14-1-118-130
Введение
Резекция почки — операция, направленная на удаление части почки с патологическим образованием. Многочисленными исследованиями было показано, что органосохраняющие операции (резекция почки) не только не уступают, но и превосходят классическую радикальную нефрэктомию в отношении продолжительности и качества жизни при лечении рака почки [1 – 3]. Таким образом, резекция почки вытеснила радикальную нефрэктомию в качестве золотого стандарта лечения локального рака почки [4 – 5].
Для дальнейшего улучшения результатов органосохраняющей хирургии пациентов с локальным раком почки назрела необходимость изменения стратегии лечения. Лечение должно быть основано на оптимизации как самой методики резекции почки с целью сохранения максимального количества функциональных единиц почки — нефронов, так и во внедрении принципов нефронсберегающей хирургии, разработанных нами на основе результатов анализа пред- и интраоперационных факторов, влияющих на функцию почки.
Нами определены следующие принципы нефронсберегающей хирургии:
- Хирург, выполняющий нефрон-сберегающую операцию, должен пройти специализированное обучение.
- Резекция почки должна выполняться согласно чёткому стандартному операционному протоколу.
- Хирургу следует изучить трёхмерную анатомию почки, пораженной опухолью.
- Необходимо предварительно выделить почечную артерию и, при возможности, ветви артерии, питающие опухоль.
- Минимизировать объём удаляемой здоровой паренхимы. При чётко определяемой псевдокапсуле возможна энуклеация.
- На любом этапе оперативного вмешательства необходима чёткая визуализация зоны резекции.
- Предпочтение следует отдавать резекции почки без ишемии.
- При необходимости ишемии следует использовать селективную ишемию, её время не должно превышать 20 минут.
- При ушивании зоны резекции следует применять прецизионную коагуляцию или гемостатические швы, а также герметизирующие ЧЛС швы без наложения второго ряда швов, сближающего края паренхимы.
- Доступ вторичен. При любом сомнении в соблюдении онкологических принципов следует выполнить резекцию с конверсией в открытую операцию.
Целью данной работы явилась демонстрация предложенного нами алгоритма лапароскопической и робот-ассистированной нефронсберегающей резекции почки с оценкой первоначальных клинических результатов.
Материалы и методы
Проанализированы результаты резекции почки у первых 100 пациентов, которые были оперированы с 2020 по 2021 год на базе ММНКЦ им. С. П. Боткина по нефронсберегающей методике: 70 лапароскопических и 30 робот-ассистированных резекций почки при раке почки в рамках проспективного когортного исследования с доступными на момент исследования данными функциональных результатов через год после операции. Критериями невключения являлись ранее перенесённая резекция почки, более одной удаленной опухоли во время резекции почки, резекция единственной почки. Операции выполняли согласно действующим стандартам помощи пациентам с локальным раком почки и действующим клиническим рекомендациям. Для комплексной оценки анатомической сложности резекции почки с опухолью новообразования классифицированы согласно нефрометрической шкале R.E.N.A.L.
Ниже приведён алгоритм нефрон-сберегающей операции, используемый в условиях ежедневной клинической практики в нашей клинике.
На диагностическом этапе опытный хирург (более 50 самостоятельных резекций), прошедший обучение по специализированной программе, самостоятельно анализирует данные компьютерной томографии с контрастированием в программе, позволяющей демонстрировать изображение в трёх плоскостях и строить трёхмерную реконструкцию. Основные цели анализа: 1) выявить опухоль; 2) провести дифференциальный диагноз с кистой почки или ангиомиолипомой; 3) изучить кровоснабжение почки и опухоли, выявить артериальные ветви, питающие опухоль; 4) оценить расположение опухоли по отношению к чашечно-лоханочной системе; 5) классифицировать анатомическую сложность резекции опухоли по специализированной шкале (шкала R.E.N.A.L.) (рис. 1).

Рисунок 1. Компьютерная томография опухоли правой почки. A — аксиальный срез; B — фронтальный срез; C — трёхмерная реконструкция на основании плотности тканей; D — сегментированная трёхмерная модель
Figure 1. CT scan of a right renal tumour. A — axial slice; B — coronal slice; C — three-dimensional reconstruction based on tissue density; D — segmented 3D model
Основываясь на полученных результатах анализа, хирург выбирает хирургический доступ. При несложных и умеренно сложных для резекции опухолях (R.E.N.A.L. 4 – 9) хорошие результаты демонстрирует лапароскопическая методика. Робот-ассистированный доступ является методом выбора при резекции опухолей средней и высокой степеней сложности (R.E.N.A.L. 7 – 12).
Основной вариабельной составляющей плана операции является оценка возможности диссекции артериальной ветви, кровоснабжающей опухоль в случае её выявления при компьютерной томографии. В последующем оперативное пособие производится согласно стандартному операционному протоколу (табл. 1).
Таблица 1. Стандартный операционный протокол лапароскопической резекции почки
Table 1. Standard operative procedure of laparoscopic nephron-sparing partial nephrectomy
Этапы | Stages | Действия | Actions |
Подготовка Preparation | 1. Установка уретрального катетера | Urinary catheter placement 2. Положение на боку c фиксацией в двух местах, верхняя рука отведена краниально | Side position for kidney surgery. Body is fixed with 2 straps. The upper hand is on the stand moved ahead away from the instruments 3. Назогастральный зонд (анестезиолог) | The nasogastric tube is inserted by the anesthesia team 4. КТ данные в операционной | CT data in the operating room 5. Контроль наличия инструментов согласно списку | Instrument list check |
Доступ в брюшную полость Peritoneal cavity access | 1. Игла Veress / открытый доступ по методике Hasson через пупок (или латеральнее у тучного больного) — интраперитонеальное давление 15 мм рт. ст.| Veress needle or open access by Hasson technique through the umbilicus (or laterally in obese patient). Intra abdominal pressure is kept at 15 mm Hg 2. Установка первого троакара 12 мм c защитой для оптики (Endo-tip, Storz) | First trocar placement should be with defence system (Endo-tip, Storz). 3. Снижение давления до 12 мм рт. ст. | Pressure decreses to 12 mm Hg 4. Установка дополнительных троакаров (1 – 12 мм, 1 – 5 мм) | Accessory trocar placement (1 – 12 mm, 1 – 5 mm) |
Доступ к почечной ножке Access to renal pedicle | 1. Мобилизация толстого кишечника | Colon mobilisation 2. Визуализация мочеточника | Ureter identification 3. Мобилизация почечной ножки | Renal pedicle mobilisation 4. Мобилизация ветви почечной артерии, питающей опухоль | Mobilization of tumour-feeding renal artery branch |
Резекция Resection | 1. Мобилизация почки, выделение опухоли | Kidney mobilization. Identification of the tumor 2. Установка под необходимым углом дополнительного троакара для резекции | Placement of accessory trocar under needed degree for kidney resection 3. Интраперитонеальное размещение нитей, салфеток, мешка | Intraperitoneal placement of sutures with needles, napkins and evacuation bag 4. Анестезиолог (контроль релаксации), нестерильная сестра — в операционную | Anesthetist checks for relaxation, call for unsterile nurse to the operating room 5. * Наложение превентивных швов | Preventive suture placement * Селективная ишемия (УЗИ-контроль зоны ишемии, при неэффективности пережатие основной артерии) | Selective ischemia (with Doppler control. If ineffective and bleeds — clamp the main artery) * Пережатие основной артерии (Контроль времени пережатия) | Main renal artery closing with endoscopic bulldog clamps and vocalize the time of closing * Без ишемии | No ischemia 6. Резекция или энуклеация опухоли почки, с последовательной коагуляцией сосудов, при ухудшении видимости — пережатие почечной ножки, при улучшении — раннее снятие зажима | Tumor enucleation with stepwise control of vessels by coagulation. If bad visualization — clamp the renal artery, when the bleeding is controlled — remove the clamp (early unclamping) 7. После удаления опухоль сразу же помещается в мешок | The tumour is placed in a retrieval bag immediately after excision. 8. Контроль на вскрытие чашечек | Check for calices opening 9. При сомнении в гемостазе наложение первой линии шва нитью V-lok 3-0 на игле 5/8 на ложе удалённого фрагмента почки с кровоточащими сосудами | If there is any doubt regarding haemostasis, a first layer of suture is placed with 3-0 V-Loc on a 5/8 needle across the resection bed, incorporating the bleeding vessels. 10. При кровотечении наложение второго ряда швов на паренхиму с использованием прокладки Surgi-Cell Fibrillar 3 – 5 см | If still blleds place a second layer of sutures on renal parenchima with Surgi-cell Fibrillar bolster of 3 to 5 cm length |
Контроль Control | 1. Подсчёт инородных тел. Удаление иголок с нитями, салфеток, макропрепарата | Foreign bodies count. Removal of the specimen, needles and napkins 2. Ревизия брюшной полости, удаление троакаров под оптическим контролем | Peritoneal revision, trocar removing under optical control |
Завершение операции Completion of the procedure | 1. Ушивание портов более 12 мм (викрил 2/0, игла 5/8, 26 мм) | Closure of ports larger than 12 mm with Vicryl 2-0 on a 5/8, 26 mm needle 2. Швы на кожу | Skin sutures 3. Стерильные наклейки | Sterile strips 4. Протокол операции с указанием вида и времени ишемии, методики резекции и обработки / вида ушивания ложа | An operative report should include the type and duration of ischaemia, the resection technique, and the method and pattern of renal defect closure. |
Примечание * — альтернативные варианты выполнения операции
Notes * — alternative surgery techniques
Анализ стандартного операционного протокола показывает, что подготовительный этап и доступ не имеют принципиального значения для сохранения функциональной способности почек и могут отличаться в разных клиниках.
Одна из первых особенностей предложенного нами протокола заключается в обязательном выделении почечной ножки. Мы считаем данный манёвр необходимым даже при резекции небольших опухолей, при которых часто определяется отсутствие выраженной псевдокапсулы и, следовательно, невозможность выполнения энуклеации. В этом случае в ходе резекции существует вероятность кровотечения, затрудняющего четкую визуализацию границ резекции, что противоречит нефрон-сберегающим принципам, так как может привести к неконтролируемому наложению швов, травме значительного количества здоровой паренхимы и положительному хирургическому краю. Особенностью выделения почечной ножки при робот-ассистированной резекции почки является необходимость проведения под почечную артерию гибкой резиновой держалки, что значительно ускоряет этап осуществления временной окклюзии почечной артерии при кровотечении.
Определение основных почечных сосудов даёт возможность выделения субсегментарной (3 – 4 уровня) ветви почечной артерии, питающей опухоль (рис. 2). Следует подчеркнуть необходимость интраоперационного ультразвукового доплеровского контроля для подтверждения полноты окклюзии и исключения ишемии здоровой паренхимы почки.

Рисунок 2. Ветви почечной артерии: А — ветвь артерии, питающая верхний полюс почки, В — ветвь артерии, питающая опухоль, С — ветвь артерии, питающая нижний полюс почки
Figure 2. Renal artery branches: A – arterial branch supplying the upper pole of the kidney; B — arterial branch supplying the tumour; C — arterial branch supplying the lower pole of the kidney
Следующий этап операции заключается в обнаружении опухоли, что может оказаться довольно сложным при её эндофитном расположении. В этой ситуации интраоперационное ультразвуковое исследование позволяет определить расположение, глубину и диаметр опухоли и, кроме того, исключить мультифокальность (рис. 3).

Рисунок 3. Интраоперационная ультрасонограмма опухоли
Figure 3. Intraoperative ultrasound tumour image
Фасция Gerot вскрывается на некотором расстоянии от опухоли, при этом собственная капсула почки обнажается до краёв опухоли. На данном этапе операции при лапароскопии оценивают углы расположения троакаров и при необходимости устанавливают дополнительный троакар для резекции и последующего ушивания зоны резекции. При неприемлемых углах доступа почка должна быть полностью мобилизована и ротирована, например, для доступа к опухолям, располагающимся по заднемедиальной поверхности верхнего полюса. В этом случае целесообразно применение интраперитонеального размещения салфеток, которые позволяют удержать почку в нужном положении и, абсорбируя кровь, обеспечивают лучший обзор операционного поля. Кроме того, с целью минимизации времени тепловой ишемии мы помещаем внутрь заранее заготовленные нити V-Loc 3-0 на игле 5/8 и полигликолид N-0 с закреплённой на конце нити клипсой Hem-o-loc XL, «развешивая» их на передней брюшной стенке для удобного одномоментного захвата иглодержателем (рис. 4). В этот же временной период анестезиологи должны проконтролировать глубину анестезии и миорелаксации. В операционной должна присутствовать нестерильная медсестра или медицинский техник.
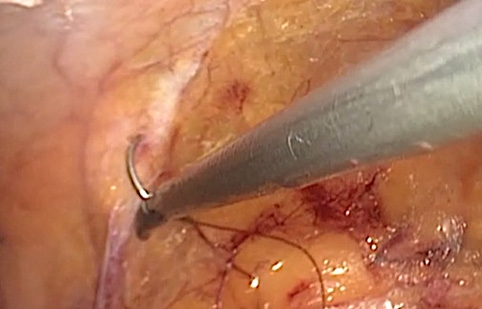
Рисунок 4. Предварительная фиксация иглы с нитью на передней брюшной стенке позволяет сэкономить важное время при ушивании зоны резекции
Figure 4. Pre-positioning the needle with suture on the anterior abdominal wall helps to save crucial time during closure of the resection bed.
Резекция и ушивание зоны резекции. Перед резекцией следует сделать разметку электродом-крючком и вскрыть собственную капсулу почки вокруг опухоли, используя высокую мощность коагулятора, что позволяет предупредить капсульное кровотечение. Также этот этап возможно осуществить с применением современных электро- или ультразвуковых скальпелей — LigaSure (Covidien), Thunderbeat (Olympus), Harmonic (Ethicon) и других (рис. 5).
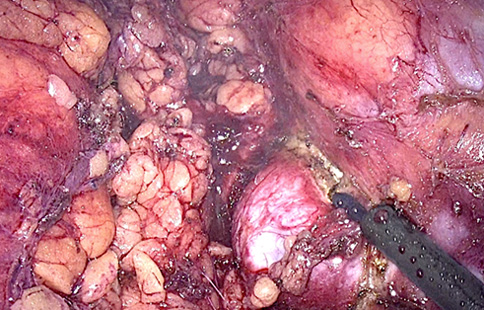
Риcунок 5. Разметка зоны резекции с помощью монополярного электрода-крючка. Мощность 80 Вт позволяет остановить кровотечение из капсулы
Figure 5. Monopolar hook electrode is used to mark the margins of partial nephrectomy. 80 Watt power adequately stops capsular bleeding
Дальнейшая последовательность резекции зависит от размеров опухоли, типа её кровоснабжения и наличия у неё псевдокапсулы. Как правило, опухоли более 2 см имеют хорошо выраженную псевдокапсулу, определяемую при компьютерной томографии. В данных обстоятельствах энуклеация опухоли начинается вдоль псевдокапсулы с помощью биполярного зажима, используемого в автобиполярном режиме мощностью 70 Вт, и отсоса. Биполярный зажим позволяет коагулировать сосуды диаметром до 4 – 5 мм. Диссекция осуществляется постепенно, последовательно коагулируя и пересекая один сосуд за другим. Сосуды диаметром 5 мм и более могут быть раздельно клипированы и пересечены (рис. 6).


Рисунок 6. Робот-ассистированная резекция почки: А — пересечена артерия, питающая опухоль; В — выделена опухолевая вена
Figure 6. Robotic-assisted partial nephrectomy: А — Tumour-feeding artery is cut; В — Tumor vein is mobilized
Часто в ходе энуклеации в самой глубине раны обнаруживается основной питающий сосуд, который не представляется возможным клипировать, поэтому целесообразно провести энуклеацию в пределах псевдокапсулы и только затем отсечь опухоль от ложа. Выявленный сосуд захватывается зажимом, коагулируется, клипируется, либо (при неэффективности указанных методик) прошивается швом нитью V-loc на игле 5/8 (рис. 7).
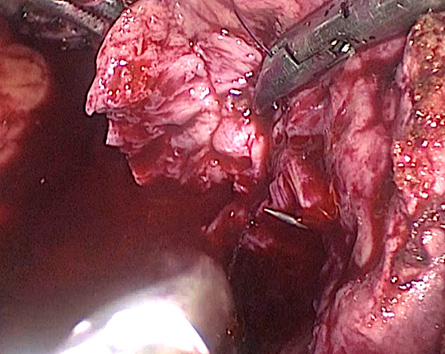
Риcунок 7. Наложение первого глубокого шва на ложе опухоли нитью V-loc 3-0 на игле 5/8
Figure 7. Placement of the first deep suture across the tumour bed using 3-0 V-Loc on a 5/8 needle
Следует отметить, что стабильность видеоизображения, масштабирование диапазона движений и фильтрация тремора при робот-ассистированной операции являются несомненными преимуществами и позволяют выполнять данную методику практически при опухолях любой степени сложности.
При резекции малых (< 2 см), преимущественно экзофитных, опухолей мы не выделяем почечную ножку, не выполняем энуклеацию, а накладываем 1 – 2 превентивных шва вокруг опухоли и осуществляем резекцию холодными ножницами. Применение клипс Hem-o-lok позволяет подтянуть нити при недостаточной компрессии после удаления опухоли. Мелкие сосуды коагулируем.
При невозможности чётко идентифицировать край резекции вследствие недостаточного гемостаза во время энуклеации приходится прибегать к пережатию почечной артерии или (предпочтительнее) её ветви, кровоснабжающей опухоль. Для пережатия почечных сосудов применяются эндоскопические зажимы мини-бульдоги с привязанной на них толстой нитью для безопасности и быстрого их обнаружения в брюшной полости. Особенностью использования мини-бульдогов может быть неполная окклюзия сосудов у пациентов с атеросклерозом.
В условиях тепловой ишемии резекцию выполняли «холодными» ножницами с целью макcимального сохранения объёма функционирующей почки (рис. 8).

Рисунок 8. Резекция почки «холодными» ножницами при пережатой артерии обеспечивает лучшую визуализацию границы резекции
Figure 8. Resection of the kidney with cold scissors under arterial clamping provides superior visualisation of the resection margin
По завершении резекции опухоль помещали в мешок для эвакуации и осуществляли окончательный гемостаз.
При неполноценном текущем гемостазе в ходе энуклеации либо в условиях ишемии основным методом достижения тщательного гемостаза при резекции почки является реноррафия. В соответствии с нефронсберегающими принципами нашей обычной практикой при опухоли более 3 см со значимым эндофитным компонентом является наложение непрерывного однорядного шва нитью V-loc 3-0 на игле 5/8 на ложе опухоли (рис. 7). При этом на конце нити закрепляется клипса Hem-o-lok, далее выполняется вкол через собственную капсулу почки в основание зоны резекции, где сосуды и вскрытые чашечки тщательно ушиваются. Свойств нити по удержанию тканей достаточно, чтобы не выводить её при каждом стежке на капсулу почки. По завершении этого внутреннего шва снимается зажим с почечной ножки и контролируется гемостаз (рис. 9).

Риcунок 9. Контроль гемостаза после завершения внутреннего шва
Figure 9. Hemostasis control after first layer completion
При необходимости на кровоточащие сосуды накладываются дополнительные внутренние гемостатические швы. Если и в этом случае гемостаз недостаточен, то вынужденно применяется второй ряд швов, накладываемый на паренхиму с целью сдавления ею кровоточащих сосудов. После тампонирования ложа опухоли прокладкой Surgi-Cell Fibrillar (Ethicon) длиной 3 – 5 см на паренхиму накладывается непрерывный шов синтетической рассасывающей нитью на большой (40 – 50 мм) игле 1/2 с фиксацией каждого выкола серединной клипсы Hem-o-lok, позволяющей при необходимости подтянуть нить и достичь большей компрессии (рис. 10). В конце шва нить закрепляется в замке клипсы, что не позволяет ей распускаться. По завершении гемостаза производится контроль его эффективности на сниженном внутрибрюшном давлении, удаляются иголки с нитями, салфетки и макропрепарат. Вне брюшной полости производится разрез опухоли и оценивается целостность псевдокапсулы. Выполняется окончательная ревизия брюшной полости, через один из 5 мм портов устанавливается пластинчатый дренаж к зоне операции и троакары удаляются под оптическим контролем.

Рисунок 10. Зона резекции после наложения второго ряда швов. Нить V-loc 2-0, игла 44 мм, 1/2. Каждый стежок непрерывного шва фиксируется клипсой Hem-o-loc
Figure 10. Resection bed after placement of the second layer of sutures. Closure is performed with 2-0 V-Loc on a 44-mm, 1/2-circle needle, with each bite of the running suture secured using a Hem-o-lok clip
Результаты
Медиана возраста пациентов составила 63 (21 – 86) года. Количество мужчин — 58, женщин — 42. Средний индекс массы тела — 26,8 (20 – 43) кг/м². У 19% пациентов имела место хроническая болезнь почек перед операцией — 3‑й и выше стадии. Индекс Charlson составил в среднем 4,0 и не различался, как и все другие показатели, у пациентов вне зависимости от типа операции, которой они подверглись.
Большинство пациентов перед операцией имели стадию сT1а — 70 пациентов, стадию сT1b — 14 пациентов, стадию сТ2 — 4 пациента. Кистозная опухоль обнаружена у 12 пациентов.
В правой почке опухоль была выявлена в 54 случаях, в левой — в 46 случаях. Медиана диаметра опухоли в наибольшем измерении составила 3,6 ± 1,6 см. В среднем сегменте опухоль располагалась у 29 больных, в нижнем полюсе — у 39, у 32 пациентов имело место расположение в верхнем полюсе. Опухоль обнаруживали по передней поверхности в 45% случаев, по задней поверхности — в 55% случаев. У 16 пациентов имело место преимущественно внутриорганное расположение опухоли, в 31 наблюдении опухоль выступала за контур почки менее чем на 50%, в 53 случаях отмечен преимущественно экзофитный рост новообразования. В большинстве случаев опухоль располагалась на значительном расстоянии от чашечно-лоханочной системы и синуса (в 62 случаях ≥ 7 мм), в 16 — на расстоянии от 4 до 7мм, у 22 пациентов опухоль примыкала к синусу (< 4 мм).
Сопутствующие заболевания, способные неблагоприятно влиять на почечную функцию, диагностированы в 75,3% случаев. Наиболее частыми заболеваниями явились артериальная гипертензия (58,8%), другие сердечно-сосудистые заболевания (24,7%) и сахарный диабет (11,7%).
Средняя сумма баллов по шкале R.E.N.A.L составила 7,5 балла. Следует отметить, что в нашем исследовании всего 45% больных имели лёгкую сложность резекции, а в 55% случаев сложность резекции была умеренной или высокой.
Лапароскопические и робот-ассистированные резекции почки с применением нефронсберегающих принципов были выполнены без конверсии у всех пациентов. У 97 пациентов был констатирован отрицательный хирургический край. Пережатие почечной ножки потребовалось 14 пациентам при среднем времени тепловой ишемии 9 минут. Ни у одного больного время ишемии не превышало 25 минут. Средний объём кровопотери 80 (10 – 350) мл (T1a — 50 мл, T1b — 160 мл, T2 — 120 мл, кистозная опухоль — 100 мл). Средняя длительность операции — 95 (65 – 165) минут.
Гистологическое исследование после операции у 76 пациентов выявило светлоклеточный рак почки, у 4 пациентов — папиллярный рак 2-го типа, у 8 — хромофобный и у 12 пациентов выявлена онкоцитома. Высокодифференцированная опухоль (G1) обнаружена у 65 пациентов, умеренно-дифференцированная (G2) — у 18 и низкодифференцированная опухоль (G3) выявлена у 5 больных.
Скорость клубочковой фильтрации более чем на 10% после операции снизилась у 28 пациентов. У 22 больных был отмечен рост стадии ХБП (из них у 6 СКФ уменьшилась менее чем на 10%).
Осложнения 1-й – 2‑й степени по шкале у Clavien-Dindo были зарегистрированы у 8 пациентов. Интра- и послеоперационных осложнений Clavien-Dindo 3 и выше отмечено не было.
«Трифекта» достигнута у 89 пациентов, «Пентафекта» — у 55 пациентов. Среднее время наблюдения составило 30 месяцев (24 – 36).
Обсуждение
Результаты резекции почки зависят от ряда факторов, которые можно разделить на неизменные и модифицируемые.
Соматический статус пациента и морфометрические характеристики опухоли являются основными неизменными предикторами достижения функционального результата резекции почки. Эффективность сохранения функции почки снижается при операциях c трудно расположенными опухолями, у пациентов с изначальным снижением функции почек или с факторами риска, повышающими вероятность ухудшения функции почек в дальнейшем.
Указанные параметры являются немодифицируемыми, и в этом аспекте следует обратить внимание на те интраоперационные параметры и технические особенности выполнения операции, на которые возможно повлиять [6].
Функциональные результаты резекции почки зависят от совокупности взаимовлияющих интраоперационных факторов, к которым относят применение, тип и продолжительность ишемии, объём сохранённой непоражённой паренхимы почки. По нашему мнению, эти параметры являются взаимосвязанными, и рассматривать их по отдельности нецелесообразно. При сложных и длительных резекциях почки, при центрально расположенных внутрисинусных опухолях обычно требуется и продолжительная ишемия. Очевидно, что и объём паренхимы в таких ситуациях сохранить труднее, и он, скорее всего, будет меньше после операции. С другой стороны, при небольших, периферически расположенных опухолях будут минимальными как время ишемии, так и объём удалённой паренхимы [7].
Несмотря на то, что большинством авторов порог в 25 минут признан не приводящим к существенному снижению функции оперированной почки в отдалённом периоде, существуют исследования, свидетельствующие о том, что даже непродолжительная ишемия может приводить к необратимым изменениям паренхимы почки [8]. Это особенно достоверно продемонстрировано в исследованиях на единственной почке и в исследованиях с объективной оценкой функции с применением радионуклидных методов [9 – 10].
Предложенные принципы нефрон-сберегающей хирургии направлены на максимальное сохранение функции почки за счёт минимизации травмы здоровой паренхимы и времени тепловой ишемии. Они основаны как на наших исследованиях, так и на исследованиях наших коллег.
В частности, была доказана лучшая сохранность функции почки при использовании селективной ишемии ветви почечной артерии, питающей опухоль, по сравнению с тотальной ишемией [11 – 12].
В ряде работ неоднократно подчеркивалась важность анализа данных компьютерной томографии с оценкой сложности по нефрометрическим шкалам и построения трёхмерных моделей почек с опухолями при планировании органосохраняющего лечения [13 – 15].
Существует множество исследований, посвящённых различным аспектам гемостаза и техническим особенностям резекции при раке почки [16 – 18]. Доказана онкологическая безопасность энуклеации и её преимущество в сравнении с резекцией в отношении сохранения функции почки [16][19]
Были продемонстрированы хорошие результаты лапароскопической резекции при опухолях почки в стадии T1b – T2 [20 – 22].
Обосновано применение коагуляции в сравнении с двурядным швом паренхимы почки при реконструкции ложа удалённой опухоли почки [23 – 26].
Применение превентивных швов и использование лапароскопических систем трёхмерного видения ультравысокого разрешения также являются предпочтительными подходами для сохранения функции почки после её резекции [27 – 30].
Таким образом, мы объединили все достижения современной отечественной урологии и разработали алгоритм не органо-, а нефронсберегающей резекции почки.
Представленный анализ первичных клинических результатов демонстрирует преимущество такого подхода. Вероятность достижения «пентафекты» увеличилась с 28% в исторической группе до 55% в настоящем исследовании [6].
Заключение
Развитие эндоскопических технологий, внедрение робот-ассистированной хирургии и совершенствование методики выполнения резекции почки привело к изменению парадигмы в лечении локального рака почки. Применение принципов нефронсберегающей хирургии позволяет улучшить функциональные результаты органосохраняющей хирургии рака почки. Представленный подробный алгоритм выполнения резекции почки лег в основу клинических протоколов минимально-инвазивной резекции почки.
Список литературы
1. Gill IS, Matin SF, Desai MM, Kaouk JH, Steinberg A, Mascha E, Thornton J, Sherief MH, Strzempkowski B, Novick AC. Comparative analysis of laparoscopic versus open partial nephrectomy for renal tumors in 200 patients. J Urol. 2003;170(1):64-68. DOI: 10.1097/01.ju.0000072272.02322.ff
2. Cozar JM, Tallada M. Open partial nephrectomy in renal cancer: a feasible gold standard technique in all hospitals. Adv Urol. 2008;2008:916463. DOI: 10.1155/2008/916463
3. Матвеев В.Б., Матвеев Б.П., Волкова М.И., Перлин Д.В., Фигурин К.М. Роль органосохраняющего хирургического лечения рака почки на современном этапе. Онкоурология. 2007;3(2):5-11.
4. Ljungberg B, Albiges L, Abu-Ghanem Y, Bedke J, Capitanio U, Dabestani S, Fernández-Pello S, Giles RH, Hofmann F, Hora M, Klatte T, Kuusk T, Lam TB, Marconi L, Powles T, Tahbaz R, Volpe A, Bex A. European Association of Urology Guidelines on Renal Cell Carcinoma: The 2022 Update. Eur Urol. 2022;82(4):399-410. DOI: 10.1016/j.eururo.2022.03.006
5. Campbell S, Uzzo RG, Allaf ME, Bass EB, Cadeddu JA, Chang A, Clark PE, Davis BJ, Derweesh IH, Giambarresi L, Gervais DA, Hu SL, Lane BR, Leibovich BC, Pierorazio PM. Renal Mass and Localized Renal Cancer: AUA Guideline. J Urol. 2017;198(3):520-529. DOI: 10.1016/j.juro.2017.04.100
6. Серегин А.А., Серегин А.В., Колонтарев К.Б., Шустицкий Н.A., Чехонацкий И.A., Лоран O.Б. Предоперационные факторы, влияющие на достижение «трифекты» и «пентафекты» при резекции почки с опухолью. Урология. 2023;(5):57-62.
7. Antonelli A, Cindolo L, Sandri M, Veccia A, Annino F, Bertagna F, Carini M, Celia A, D’Orta C, De Concilio B, Furlan M, Giommoni V, Ingrosso , Mari A, Nucciotti R, Olianti C, Porreca A, Primiceri G, Schips L, Sessa F, Bove P, Simeone C, Minervini A; AGILE Group (Italian Group for Advanced Laparo-Endoscopic Surgery). Is off-clamp robot-assisted partial nephrectomy beneficial for renal function? Data from the CLOCK trial. BJU Int. 2022;129(2):217-224. DOI: 10.1111/bju.15503
8. Lane BR, Campbell SC, Gill IS. 10-year oncologic outcomes after laparoscopic and open partial nephrectomy. J Urol. 2013;190(1):44-49. DOI: 10.1016/j.juro.2012.12.102
9. Gill IS, Kavoussi LR, Lane BR, Blute ML, Babineau D, Colombo JR Jr, Frank I, Permpongkosol S, Weight CJ, Kaouk JH, Kattan MW, Novick AC. Comparison of 1,800 laparoscopic and open partial nephrectomies for single renal tumors. J Urol. 2007;178(1):41-46. DOI: 10.1016/j.juro.2007.03.038
10. Индароков Т.Р., Серегин А.В., Лоран О.Б., Шустицкий Н.А., Симанков И.В., Бессолова О.В., Яндиев А.М. Оценка почечной функции после резекции по поводу рака. Consilium Medicum. 2017;19(7):23-27
11. Перлин Д.В., Александров И.В., Зипунников В.П., Каргин К.А. Лапароскопическая резекция почки с применением локальной ишемии. Урология. 2013;(4):69-73.
12. Перлин Д.В., Сапожников А.Д., Зипунников В.П., Лялюев А.М., Шевченко О.Н. Органосохраняющие лапароскопические операции при раке почки с использованием посегментной ишемии. Эндоскопическая хирургия. 2014;20(6):9 13.
13. Сирота Е.С., Рапопорт Л.М., Гридин В.Н., Цариченко Д.Г., Кузнецов И.А., Сирота А.Е., Аляев Ю.Г. Анализ кривой обучения хирургов в зависимости от сложности нефрометрической оценки при выполнении лапароскопической резекции почки у пациентов с локализованными образованиями паренхимы почки. Урология. 2020;(6):11-18.
14. Проскура А.В., Аляев Ю.Г., Борисов В.В., Бутнару Д.В., Рапопорт Л.М., Сирота Е.С., Суворов А.Ю., Фиев Д.Н., Шпоть Е.В., Безруков Е.А., Еникеев М.Э., Акопян Г.Н., Королев Д.О., Воробьев A.А., Черненький М.М., Черненький И.М., Исмаилов Х.М., Шомукимова З.С. Оценка функционального состояния почек до и после резекции по поводу односторонней опухоли с помощью математической обработки данных компьютерной томографии с контрастированием. Андрология и генитальная хирургия. 2023;24(3):66-74.
15. Аляев Ю.Г., Сирота Е.С., Рапопорт Л.М., Безруков Е.А., Суханов Р.Б., Цариченко Д.Г. Сравнение значимости шкал нефрометрической оценки RENAL, PADUA, С-index для прогноза сложности лапароскопической резекции почки. Онкоурология. 2018;14(1):36-46.
16. Шпоть Е.В., Мамедкасимов Н.А., Аляев Ю.Г., Рапопорт Л.М., Проскура А.В., Машин Г.А. Сравнительный анализ результатов лапароскопической и ретроперитонеоскопической резекции почки в зависимости от вида временного и окончательного гемостаза. Урология. 2018;(6):95-100
17. Глыбочко П.В., Аляев Ю.Г., Пшихачев А.М., Шпоть Е.В., Сорокин Н.И., Дымов А.М., Акопян Г.Н., Чиненов Д.В., Снурницына О.В. Возможности эндовидеохирургических технологий при ипсилатеральном сочетании опухоли и камня почки. Урология. 2016;(3):70-75.
18. Аляев Ю.Г., Безруков Е.А., Сирота Е.С., Шпоть Е.В., Проскура А.В. Методы гемостаза при проведении лапароскопической резекции почки. Урология. 2014;(4):90-95.
19. Мамедкасимов Н.А., Шпоть Е.В., Аляев Ю.Г., Рапопорт Л.М., Сорокин Н.И. Органосохраняющие операции по поводу опухоли почки в условиях нулевой ишемии. Нужно ли нам 3D-моделирование? Урология. 2019;(1):56-62.
20. Котов С.В., Гуспанов Р.И., Юсуфов А.Г., Неменов А.А., Манцов А.А. Влияние adherent perinephric fat на результаты органосохраняющего лечения почечно-клеточного рака. Вестник урологии. 2023;11(2):47-55.
21. Кочкин А.Д., Кнутов А.В., Севрюков Ф.А. Лапароскопическая резекция почки при опухолях R.E.N.A.L.10 и больше. Урология. 2020;(6):93-98.
22. Котов С.В., Неменов А.А., Юсуфов А.Г., Гуспанов Р.И., Пульбере С.А., Простомолотов А.О. Сравнение периоперационных и ранних функциональных результатов лапароскопической резекции почки с опухолью при стадии cT1aN0M0 и cT1b-T2aN0M0. Онкоурология. 2021;17(4):38-46.
23. Носов А.К., Лушина П.А., Петров С.Б. Лапароскопическая резекция почки без ишемии и без наложения гемостатического шва на зону резекции у пациентов с раком почки. Урологические ведомости. 2016;6(S):76-77.
24. Попов С.В., Зайцев Э.В., Петрова Ю.А., Гусейнов Р.Г., Топузов Т.М. Оценка различных методов гемостаза при выполнении лапароскопической резекции почки. Урология. 2013;(3):61-67.
25. Петров С.Б., Шпиленя Е.С., Шкарупа Д.Д. Функциональные результаты резекции почки при новообразованиях. Вестник хирургии им. И.И. Грекова. 2009;168(4):85-87.
26. Носов А.К., Мамижев Э.М., Щекутеев Н.А., Семейко Д.П., Лушина П.А., Румянцева Д.И., Беркут М.В. Способы хирургического гемостаза и герметизации при лапароскопической резекции почки. Онкоурология. 2022;18(3):27-34.
27. Серегин А.А., Серегин А.В., Колонтарев К.Б., Серегин И.В., Махмадалиев А.И., Лоран О.Б. Превентивный шов при лапароскопической резекции почки без ишемии. Описание методики ГКБ им. С.П. Боткина. Онкоурология. 2022;18(3):35-40.
28. Серегин А.В., Шустицкий Н.А., Индароков Т.Р., Морозов А.Д., Бессолова О.В. Резекция почки с превентивным швом при почечноклеточном раке. Анналы хирургии. 2016;21(4):235-239.
29. Серегин А.А., Серегин И.В., Махмадалиев А.И. 3D-лапароскопия при резекции почки: первый опыт применения и предварительные результаты. Медицинский вестник МВД. 2022;121(6):34.
30. Серегин А.В., Лоран О.Б., Серегин А.А., Шустицкий Н.А., Серегин И.В., Бессолова О.В., Индароков Т.Р. Возможности и особенности выполнения органосохраняющих операций без ишемии при локализованном раке почки. Вестник урологии. 2023;11(2):188-202.
Об авторах
А. А. СерёгинРоссия
Александр Александрович Серёгин — д-р мед. наук
Москва
Конфликт интересов:
Статья прошла принятую в журнале процедуру рецензирования независимыми экспертами. Об иных конфликтах интересов авторы не заявляли
Н. А. Шустицкий
Россия
Николай Александрович Шустицкий — канд. мед. наук
Москва
Конфликт интересов:
Статья прошла принятую в журнале процедуру рецензирования независимыми экспертами. Об иных конфликтах интересов авторы не заявляли
А. В. Серёгин
Россия
Александр Васильевич Серёгин — д-р мед. наук, профессор
Москва
Конфликт интересов:
Статья прошла принятую в журнале процедуру рецензирования независимыми экспертами. Об иных конфликтах интересов авторы не заявляли
К. Б. Колонтарев
Россия
Константин Борисович Колонтарев — д-р мед. наук, профессор
Москва
Конфликт интересов:
Статья прошла принятую в журнале процедуру рецензирования независимыми экспертами. Об иных конфликтах интересов авторы не заявляли
А. В. Говоров
Россия
Александр Викторович Говоров — д-р мед. наук, профессор
Москва
Конфликт интересов:
Статья прошла принятую в журнале процедуру рецензирования независимыми экспертами. Об иных конфликтах интересов авторы не заявляли
П. И. Раснер
Россия
Павел Ильич Раснер — д-р мед. наук, профессор
Москва
Конфликт интересов:
Статья прошла принятую в журнале процедуру рецензирования независимыми экспертами. Об иных конфликтах интересов авторы не заявляли
Р. А. Тарасов
Россия
Родион Александрович Тарасов
Москва
Конфликт интересов:
Статья прошла принятую в журнале процедуру рецензирования независимыми экспертами. Об иных конфликтах интересов авторы не заявляли
А. Э. Нифталыев
Россия
Ага Эльбурус оглы Нифталыев
Москва
Конфликт интересов:
Статья прошла принятую в журнале процедуру рецензирования независимыми экспертами. Об иных конфликтах интересов авторы не заявляли
К. П. Золотарёва
Россия
Карина Павловна Золотарёва
Москва
Конфликт интересов:
Статья прошла принятую в журнале процедуру рецензирования независимыми экспертами. Об иных конфликтах интересов авторы не заявляли
Д. Ю. Пушкарь
Россия
Дмитрий Юрьевич Пушкарь — д-р мед. наук, профессор, акад. РАН
Москва
Конфликт интересов:
Автор статьи Дмитрий Юрьевич Пушкарь является членом редакционной коллегии журнала «Вестник урологии». Статья прошла принятую в журнале процедуру рецензирования независимыми экспертами
О. Б. Лоран
Россия
Олег Борисович Лоран —д-р мед. наук, профессор, акад. РАН, заслуженный деятель науки РФ
Москва
Конфликт интересов:
Автор статьи Олег Борисович Лоран является членом редакционной коллегии журнала «Вестник урологии». Статья прошла принятую в журнале процедуру рецензирования независимыми экспертами. Об иных конфликтах интересов авторы не заявляли
Рецензия
Для цитирования:
Серёгин А.А., Шустицкий Н.А., Серёгин А.В., Колонтарев К.Б., Говоров А.В., Раснер П.И., Тарасов Р.А., Нифталыев А.Э., Золотарёва К.П., Пушкарь Д.Ю., Лоран О.Б. Минимально-инвазивная органосохраняющая хирургия рака почки: нефронсберегающий алгоритм. Вестник урологии. 2026;14(1):118-130. https://doi.org/10.21886/2308-6424-2026-14-1-118-130
For citation:
Seregin A.A., Shustitskiy N.A., Seregin A.V., Kolontarev K.B., Govorov A.V., Rasner P.I., Tarasov R.A., Niftaliyev A.E., Zolotareva K.P., Pushkar D.Yu., Loran O.B. Nephron-sparing algorithm for minimally invasive partial nephrectomy. Urology Herald. 2026;14(1):118-130. (In Russ.) https://doi.org/10.21886/2308-6424-2026-14-1-118-130
JATS XML