Перейти к:
Сравнение циторедуктивной резекции почки и циторедуктивной нефрэктомии у пациентов с метастатическим почечноклеточным раком
https://doi.org/10.21886/2308-6424-2026-14-1-60-70
Аннотация
Введение. Циторедуктивная нефрэктомия (ЦНЭ) является стандартом комплексного лечения при метастатическом почечно-клеточном раке (мПКР) благоприятного прогноза. Циторедуктивная резекция почки (ЦРП) при мПКР выполняется нечасто.
Цель исследования. Сравнить эффективность ЦРП и ЦРН в реальной клинической практике.
Материалы и методы. В ретроспективное исследование были включены 102 пациента с мПКР, в том числе 32 пациента, которым была выполнена ЦРП, и 70 больных после ЦНЭ. Исходы заболевания включали смертность от всех причин, 30-дневную смертность и 90-дневную смертность и были стратифицированы по типу циторедуктивной операции (ЦРП против ЦНЭ). Клинические данные из медицинских карт были получены и проанализированы ретроспективно, всем пациентам было проведено клинико-лабораторное, патоморфологическое исследование. Первичной конечной точкой исследования являлась общая выживаемость (ОВ) пациентов, перенесших ЦРП или ЦНЭ. Вторичные результаты включали продолжительность пребывания в стационаре и повторную госпитализацию пациентов. Показатели выживаемости пациентов оценивали с помощью статистического метода анализа времени жизни (Survival Analysis) с расчётом описательных характеристик времени жизни в форме таблицы жизни и построения кривых Kaplan-Meier.
Результаты. У пациентов в группе ЦРП в отличие от группы ЦНЭ реже встречались светлоклеточный вариант ПКР (84,4% / 97,1% соответственно), низкодиференцированные опухоли (21,9% / 41,4% соответственно), синхронные метастазы (21,9% / 40% соответственно) и множественные метастазы (59,4% / 78,6% соответственно). Категория сТ1 значительно чаще выявлена у больных в группе ЦРП — 84,4% / 15,8%. Больные группы ЦРП чаще относились к группе благоприятного прогноза по IMDC (34,4% / 25,7%). У больных группы ЦРП реже встречались метастазы в лёгких (53,1% / 80%) и лимфатических узлах (6,2% / 22,8%), реже проводилась системная терапия ингибиторами контрольных точек (ИКТ) (3,1% / 18,6%). У пациентов группы ЦРП реже выполнялась лучевая терапия (6,2% / 18,6%). Показатели трёх- и пятилетней ОВ у больных групп ЦРП и ЦНЭ составили 62,9% и 68,1%, 40,5% и 56,3% соответственно (р = 0,08).
Заключение. На данный момент не определена тактика проведения циторедуктивной резекции почки при мПКР. Общая выживаемость выше у больных в группе ЦНЭ, несмотря на более благоприятные функциональные показатели у пациентов в группе ЦРП. Необходимы дальнейшие исследования, чтобы определить, какие пациенты лучше всего подходят для данного паллиативного метода лечения с целью улучшения персонализированной терапии и повышения показателей выживаемости.
Ключевые слова
Для цитирования:
Семенов Д.В., Орлова Р.В., Широкорад В.И., Кострицкий С.В. Сравнение циторедуктивной резекции почки и циторедуктивной нефрэктомии у пациентов с метастатическим почечноклеточным раком. Вестник урологии. 2026;14(1):60-70. https://doi.org/10.21886/2308-6424-2026-14-1-60-70
For citation:
Semyonov D.V., Orlova R.V., Shirokorad V.I., Kostritsky S.V. Cytoreductive partial nephrectomy versus cytoreductive nephrectomy in metastatic renal cell carcinoma. Urology Herald. 2026;14(1):60-70. (In Russ.) https://doi.org/10.21886/2308-6424-2026-14-1-60-70
Введение
В настоящее время на долю почечно-клеточного рака (ПКР) приходится около 5% всех новых случаев рака у мужчин и 3% у женщин во всём мире, заболевание также входит в первую десятку наиболее распространённых новообразований в США [1]. В последние годы количество ПКР увеличивается, поскольку обнаруживается случайно при плановом УЗ-исследовании брюшной полости. Хотя большинство опухолей выявляются на ранних стадиях развития и локализуются в почке, до 17% впервые выявленных опухолей являются метастатическими. По данным ВОЗ, от ПКР в мире ежегодно умирают более 140 000 человек, данная патология является 3‑й по частоте смертности от рака [2]. При этом двух- и пятилетняя общая выживаемость (ОВ) составляет 29,3% и 15,5% соответственно [3].
Пациентам, которые считаются оптимальными кандидатами для циторедуктивной нефрэктомии (ЦНЭ), может быть проведена немедленная или отсроченная операция и системная терапия для достижения наилучших показателей ОВ [4]. Согласно рекомендациям, таргетная терапия (включая ТКИ — тирозинкиназные ингибиторы) предназначается для системного лечения мПКР, при этом ЦНЭ была важным компонентом терапии на поздних стадиях заболевания [5 – 7]. Решение о циторедукции зависит от множества переменных, включая группы прогноза по IMDC, сопутствующие заболевания, статус ECOG и гистологические подтипы опухоли [5][8]. На современном этапе ЦНЭ выполняется больным мПКР благоприятного прогноза [9], однако в редких случаях для циторедукции используется циторедуктивная резекция почки (ЦРП).
Текущие руководства не рекомендуют и не обсуждают ЦРП у пациентов с мПКР [10]. Несмотря на то, что общие показатели выживаемости больных мПКР остаются низкими, предыдущие исследования продемонстрировали увеличение частоты проведения ЦРП [11]. Роль ЦРП в литературе остаётся неоднозначной, некоторые исследования носят исторический характер или ограничены по размеру выборки, а проспективных рандомизированных контролируемых исследований нет. Тем не менее ранние исследования показали, что ЦРП даёт схожие онкологические результаты в сравнении с ЦНЭ у пациентов мПКР [10][12 – 14].
С учётом изменения последних практических тенденций и неопределённости относительно возможного влияния ЦРП на выживаемость пациентов с мПКР важно проанализировать показатели ОВ пациентов, перенёсших ЦРП, по сравнению с ЦНЭ у больных мПКР, что явилось целью исследования.
Материалы и методы
В ретроспективное исследование включены 102 пациента с мПКР, в том числе 32 пациента, которым была выполнена ЦРП, и 70 больных с ЦНЭ. Исходы заболевания включали смертность от всех причин, 30-дневную и 90-дневную смертность. Исходы были стратифицированы по типу циторедуктивной операции (ЦРП против ЦНЭ). Всем пациентам проводили системную терапию на базе Городской онкологической больницы № 62 г. Москвы и в Городском онкологическом диспансере г. Санкт-Петербурга с 2010 по 2022 год. Первичным результатом исследования являлась ОВ пациентов, перенёсших ЦРП или ЦНЭ. Вторичные результаты включали продолжительность пребывания в стационаре и повторную госпитализацию пациентов.
Статистический анализ. Данные пациентов были консолидированы в виде электронных таблиц и проанализированы с помощью программы Statistica v12.1 (StatSoft Inc., Tulsa, OK, USA). Нормальность распределения проверяли с помощью теста Колмогорова-Смирнова-Lilliefors. Количественные показатели, имеющие нормальное распределение, описывали с помощью средних арифметических величин (M) и стандартных отклонений (SD), границ 95%-ного доверительного интервала (95% ДИ). В случае отсутствия нормального распределения количественные данные описывали с помощью медианы (Me) и нижнего и верхнего квартилей [Q1 – Q3]. Категориальные данные описывали с указанием абсолютных значений (n) и процентных долей (%). Доверительные интервалы (95% ДИ) для долей (%) рассчитывали по методу Klopper-Pearson. Сравнение процентных долей при анализе многопольных таблиц сопряжённости выполняли с помощью критерия Pearson`s χ². Продолжительность жизни рассчитывали от даты диагноза до даты последнего наблюдения или смерти. Показатели выживаемости пациентов оценивали с помощью статистического метода анализа времени жизни (Survival Analysis) с расчётом описательных характеристик времени жизни в форме таблицы жизни и построения кривых Kaplan-Meier. Для исключения факторов, не имеющих самостоятельной прогностической значимости, использовали регрессионный анализ Cox. Принятый уровень значимости р < 0,05.
Результаты
Характеристика больных представлена в таблице 1.
Таблица 1. Характеристика больных
Table 1. Characteristics of patients
Характеристика Characteristic | ЦРП | CPN (n = 32) | ЦНЭ | CN (n = 70) | χ². p |
n (%) | |||
Пол | Gender | |||
мужской | male | 28 (87,5) | 54 (77,1) | df = 1, χ² = 1,49, p = 0,22 |
женский | female | 4 (12,5) | 16 (22,9) | |
Возраст | Age | |||
18 – 44 | 2 (6,25) | 4 (5,7) | df = 3, χ² = 0,069, p = 0,99 |
45 – 59 | 10 (31,75) | 23 (32,8) | |
60 – 74 | 18 (56,25) | 38 (54,3) | |
> 75 | 2 (6,25) | 5 (7,2) | |
Статус по шкале ECOG | ECOG status | |||
0 | 1 (3,1) | 11 (15,8) | df = 3, χ² = 3,40, p = 0,33 |
1 | 19 (59,4) | 37 (52,8) | |
2 | 8 (25) | 14 (20) | |
3 | 4 (12,5) | 8 (11,4) | |
Гистологический вариант | Histological type | |||
светлоклеточный рак | clear-cell carcinoma | 27 (84,4) | 68 (97,1) | df = 1, χ² = 5,6, p = 0,017 |
несветлоклеточный рак | non-clear carcinoma | 5 (15,6) | 2 (2,9) | |
Категория Т | Категория Т | |||
Т1 | 27 (84,4) | 11 (15,8) | df = 3, χ² = 42,64, p = < 0,00001 |
Т2 | 2 (6,25) | 17 (24,2) | |
Т3 | 3 (4,3) | 39 (55,8) | |
Т4 | 0 | 3 (4,3) | |
Степень дифференцировки | Differentiation grade | |||
G1 | 8 (25,0) | 9 (12,8) | df = 2, χ² = 4,57, p = 0,10 |
G2 | 17 (53,1) | 32 (45,7) | |
G3 | 7 (21,9) | 29 (41,5) | |
Тип метастазов | Metastasis type | |||
метахронные | metachronous | 25 (78,1) | 40 (60) | df = 1, χ² = 3,56, p = 0,059 |
синхронные | synchronous | 7 (21,9) | 28 (40) | |
Количество метастазов | Number of metastases | |||
солитарные | solitary | 2 (6,2) | 3 (4,3) | df = 2, χ² = 4,18, p = 0,12 |
единичные | single | 11 (34,4) | 12 (17,1) | |
множественные | multiple | 19 (59,4) | 55 (78,6) | |
Прогноз по IMDC | IMDC prognosis | |||
благоприятный | favorable | 5 (15,6) | 9 (12,8) | df = 2, χ² = 1,19, p = 0,54 |
промежуточный | intermediate | 16 (50,0) | 43 (61,5) | |
неблагоприятный | poor | 11 (34,4) | 18 (25,7) | |
Локализация метастазов | Metastatic site | |||
лёгкие | lungs | 17 (53,1) | 56 (80,0) | – |
кости | bones | 11 (34,4) | 26 (37,1) | df = 1, χ² = 7,79, p = 0,005 |
печень | liver | 2 (6,2) | 16 (22,8) | df = 1, χ² = 0 ,07, p = 0,78 |
лимфатические узлы | lymph nodes | 10 (31,7) | 27 (38,6) | df = 1, χ² = 0 ,50, p = 0,47 |
головной мозг | brain | 3 (9,4) | 8 (11,4) | df = 1, χ² = 0,04, p = 0,83 |
Таргетная терапия | Target therapy | |||
тирозинкиназные ингибиторы (ТКИ) | tyrosine kinase inhibitors (TKI) | 31 (96,9) | 57 (81,4) | df = 1, χ² = 0,29, p = 0,63 |
ингибиторы контрольных точек (ИКТ) | checkpoint inhibitors (CPI) | 1 (3,1) | 13 (18,6) | |
Метастазэктомия | Лучевая терапия | 6 (18,7) | 16 (22,8) | df = 1, χ² = 4,42, p = 0,035 |
Radiation therapy | Metastasectomy | 2 (6,2) | 13 (18,6) | df = 1, χ² = 2,65, p = 0,10 |
Показатели трёх- и пятилетней ОВ у больных мПКР в группах ЦРП и ЦНЭ составили 62,9% [ 46,9% – 84,5%, 95% ДИ] и 40,5% [ 24,8% – 66,0%, 95% ДИ], 68,1% [ 56,3% – 82,4%, 95% ДИ] и 56,3% [ 43,1% – 73,6%, 95% ДИ] соответственно, при этом медиана ОВ составила 45 [ 30,4 – 94,6, 95% ДИ] и 73,9 [ 45,2 – NA, 95% ДИ] месяцев соответственно (рис. 1).

Рисунок 1. Общая выживаемость больных в группах ЦРП и ЦНЭ (n = 102)
Figure 1. Overall survival (OS) of patients in the CPN and CN groups (n = 102)
В таблице 2 описаны хирургические исходы каждого типа операций. У пациентов с ЦРП значительно короче продолжительность послеоперационного пребывания, реже частота повторных госпитализаций и ниже показатели смертности.
Таблица 2. Хирургические исходы
Table 2. Surgical outcomes
Факторы Factors | ЦРП | CPN (n = 32) | ЦНЭ | CN (n = 70) | χ². p |
Койко-день, M ± SD | Hospital stay, M ± SD | 3,8 ± 6,2 | 5,2 ± 5,7 | p = 0,03 |
Повторная госпитализация, n (%) | Readmission, n (%) | 2 (6,2) | 2 (2,8) | df = 1, χ² = 0,67, p = 0,41 |
Смертность общая, n (%) | Mortality, n (%) | 24 (75) | 43 (61,4) | df = 1, χ² = 3,27, p = 0,07 |
Смертность 30-дневная, n (%) | 30-days mortality, n (%) | 1 (3,1) | 1 (1,4) | df = 1, χ² = 0,32, p = 0,56 |
Смертность 90-дневная, n (%) | 90-days mortality, n (%) | 3 (9,3) | 4 (5,7) | df = 1, χ² = 0,53, p = 0,46 |
Показатели трёх- и пятилетней ОВ у больных мПКР в группах ЦРП и ЦНЭ категории Т1 составили 59,1% [ 41,3% – 84,4%, 95% ДИ] и 37,6% [ 21,2% – 66,6%, 95% ДИ]; 40,9% [ 18,7% – 89,4%, 95% ДИ] и 20,5% [ 4,2% –100,0%, 95% ДИ] соответственно (р = 0,15). Медиана ОВ у пациентов с Т1 при ЦРП и ЦНЭ составила 42,3 [ 27,2 – NA, 95% ДИ] и 21,3 [ 10,1 – NA, 95% ДИ] месяцев соответственно.
В исследовании выполнен расчёт показателей ОВ больных в группах ЦРП и ЦНЭ при категории Т2 – Т3 (рис. 3) и олигометастазах ПКР (рис. 4). Медиана ОВ у пациентов с Т2 – Т3 при ЦРП и ЦНЭ составила 97,9 [ 50,6 – NA, 95% ДИ] и 74,1 [ 49,5 – NA, 95% ДИ] месяцев соответственно. Медиана ОВ у пациентов с олигометастазами ПКР при ЦРП и ЦНЭ составила 65,7 [ 42,3 – NA, 95% ДИ] и 101,7 [ 74,1 – NA, 95% ДИ] месяцев соответственно.
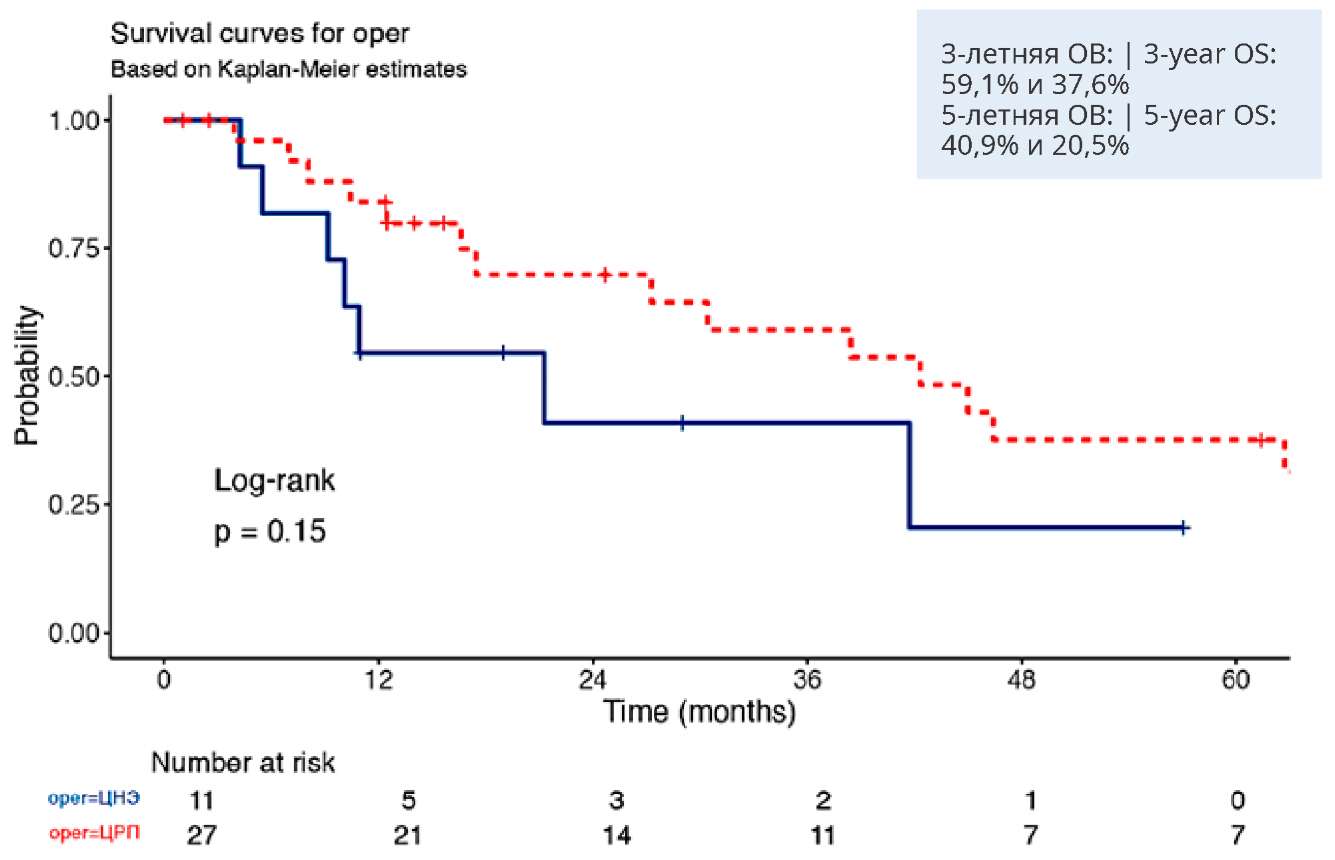
Рисунок 2. Общая выживаемость больных в группах ЦРП и ЦНЭ при категории Т1 (n = 38)
Figure 2. Overall survival (OS) of patients in the CPN and CN groups at T1 category (n = 38)

Рисунок 3. Общая выживаемость больных в группах ЦРП и ЦНЭ при категории Т2 – Т3 (n = 61)
Figure 3. Overall survival (OS) of patients in the CPN and CN groups at T2 – Т3 category (n = 61)
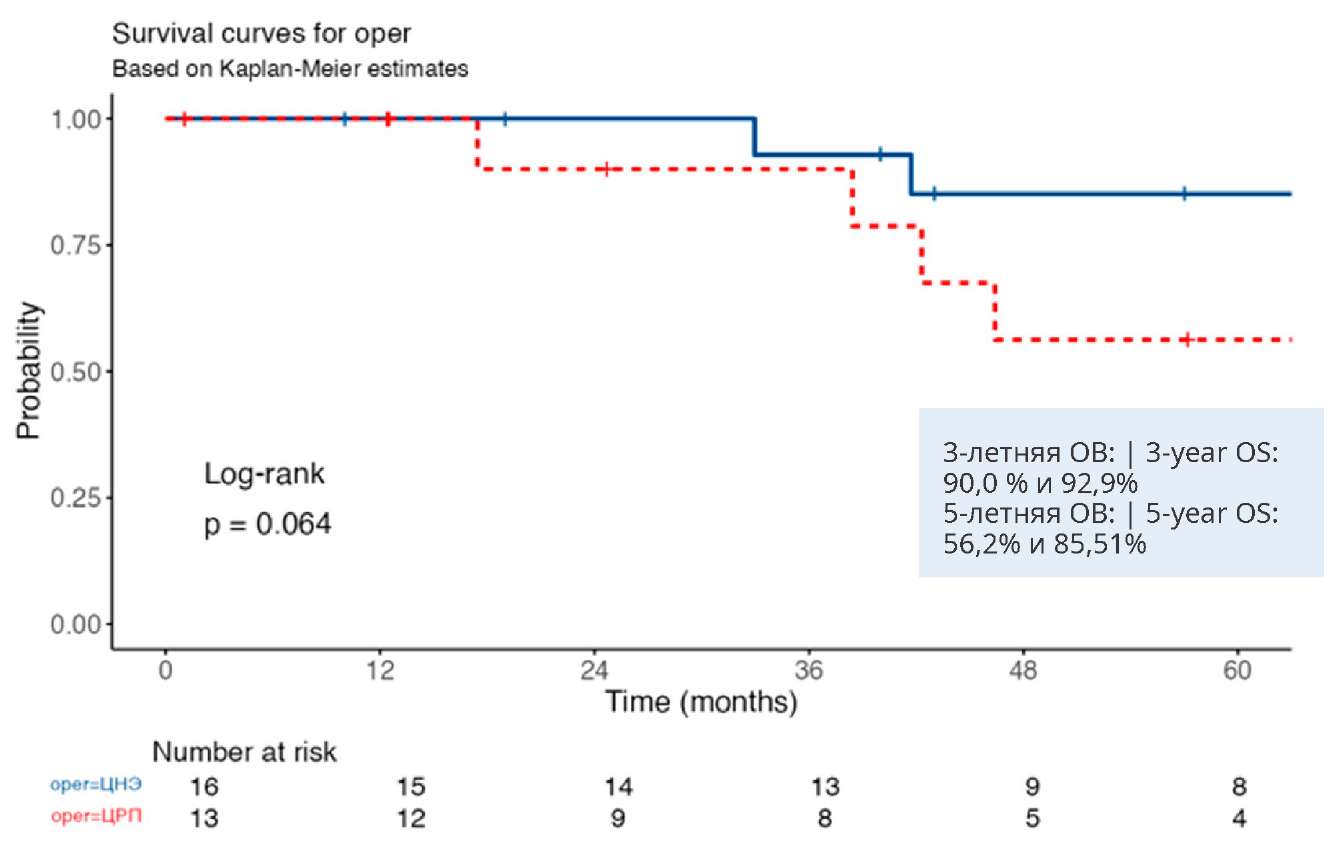
Рисунок 4. Общая выживаемость больных в группах ЦРП и ЦНЭ при олигометастазах ПКР (n = 39)
Figure 4. Overall survival of patients in the CPN and CN groups for oligometastatic RCC (n = 39)
При однофакторном анализе больных группы ЦРП неблагоприятное влияние на прогноз ОВ оказывает статус ECOG (ECOG 3: p = 0,023). В многофакторном анализе подтверждено независимое негативное влияние на показатели ОВ пола, метастазов в кости и лёгкие, а также статуса ECOG (табл. 3).
Таблица 3. Одно- и многофакторный анализ (регрессия Cox) показателей ОВ у больных мПКР при выполнении ЦРП
Table 3. Single- and multivariate analysis (Cox regression) of OS rates in mRCC patients following CNP
Факторы Factors | Градации Gradations | Пациенты, n (%) Patients, n (%) | HR (однофакторный | one-way) | HR (многофакторный | multi-way) |
Пол Gender | Мужчины | Men | 28 (87,5) | – | – |
Женщины | Women | 4 (12,5) | 4,62 (0,92 – 23,12; p = 0,063) | 181,14 (7,98 – 4109,75; p = 0,001) | |
ECOG | ECOG 0 | 1 (3,1) | – | – |
ECOG 1 | 19 (59,4) | 2,35 (0,28 – 19,72; p = 0,430) | 2,23 (0,19 – 25,57; p = 0,520) | |
ECOG 2 | 8 (25,0) | 4,87 (0,44 – 53,61; p = 0,196) | 3,11 (0,21 – 45,53; p = 0,407) | |
ECOG 3 | 4 (12,5) | 18,68 (1,49 – 234,89; p = 0,023) | 30,30 (1,33 – 689,30; p = 0,032) | |
МТС в кости Bone mts | (-) | 21 (65,6) | – | – |
(+) | 11 (34,4) | 1,68 (0,65 – 4,35; p = 0,288) | 26,16 (3,00 – 227,90; p = 0,003) | |
МТС в лёгкие Lung mts | (-) | 15 (46,9) | – | – |
(+) | 17 (53,1) | 2,61 (0,89 – 7,66; p = 0,080) | 8,00 (1,35 – 47,57; p = 0,022) |
Также при однофакторном анализе установлено, что у больных в группе ЦНЭ отрицательное влияние на показатели ОВ оказывают категория Т (Т2: p = 0,012; Т3: p = 0,010), степень дифференцировки опухоли (G3: p = 0,013), ECOG статус (ECOG 3: p = 0,001) и прогноз по IMDC (неблагоприятный: p = 0,001). В многофакторном анализе подтверждено независимое негативное влияние на ОВ возраста, категории Т, гистологического подтипа опухоли, времени появления метастазов, их количества и метастазирования в печень, а также прогноз по IMDC (табл. 4).
Таблица 4. Одно- и многофакторный анализ (регрессия Cox) показателей ОВ у больных мПКР при выполнении ЦНЭ
Table 4. Single- and multivariate analysis (Cox regression) of OS rates in mRCC patients following CN
Факторы Factors | Градации Gradations | Пациенты, n (%) Patients, n (%) | HR (однофакторный | one-way) | HR (многофакторный | multi-way) |
Возраст Age | 18 – 44 | 6 (5,9) | – | – |
45 – 59 | 33 (32,4) | 0,92 (0,26 – 3,24; p = 0,900) | 19,32 (2,24 – 166,55; p = 0,007) | |
60 – 74 | 56 (54,9) | 0,90 (0,27 – 3,02; p = 0,865) | 19,79 (2,58 – 151,80; p = 0,004) | |
> 75 | 7 (6,9) | 2,13 (0,47 – 9,59; p = 0,326) | 41,91 (4,11 – 427,28; p = 0,002) | |
T | Т1 | 38 (37,3) | – | – |
Т2 | 19 (18,6) | 0,29 (0,11 – 0,77; p = 0,012) | 0,69 (0,20 – 2,43; p = 0,569) | |
Т3 | 42 (41,2) | 0,44 (0,23 – 0,82; p = 0,010) | 0,27 (0,10 – 0,74; p = 0,011) | |
Т4 | 3 (2,9) | 0,00 (0,00 – Inf; p = 0,996) | 0,00 (0,00 – Inf; p = 0,999) | |
Гистологический тип Hystology type | Светлоклеточный Clear cell | 95 (93,1) | – | – |
Несветлоклеточный Non-clear cell | 7 (6,9) | 1,53 (0,60 – 3,90; p = 0,371) | 4,48 (1,10 – 18,23; p = 0,036) | |
Cтепень дифференци-ровки опухоли Grade | G1 | 17 (16,7) | – | – |
G2 | 49 (48,0) | 1,18 (0,52 – 2,69; p = 0,693) | 1,94 (0,69 – 5,42; p = 0,208) | |
G3 | 36 (35,3) | 2,97 (1,26 – 6,98; p = 0,013) | 1,67 (0,49 – 5,64; p = 0,410) | |
ECOG | ECOG 0 | 12 (11,8) | – | – |
ECOG 1 | 56 (54,9) | 1,23 (0,28 – 5,38; p = 0,779) | 0,43 (0,06 – 3,22; p = 0,415) | |
ECOG 2 | 22 (21,6) | 4,34 (0,98 – 19,16; p = 0,053) | 2,08 (0,23 – 18,57; p = 0,511) | |
ECOG 3 | 12 (11,8) | 14,51 (3,14 – 67,06; p = 0,001) | 7,60 (0,60 – 96,71; p = 0,118) | |
Время появления метастазов Time of metastasis | Синхронные Synchronous | 35 (34,3) | – | – |
Метахронные Metachronous | 67 (65,7) | 0,67 (0,37 – 1,23; p = 0,195) | 3,60 (1,22 – 10,65; p = 0,020) | |
Количество метастазов Number of metastases | Солитарные Solitary | 5 (4,9) | – | – |
Единичные Single | 24 (23,5) | 3,32 (0,43 – 25,61; p = 0,250) | 14,43 (0,89 – 232,96; p = 0,060) | |
Множественные Multiple | 73 (71,6) | 5,47 (0,74 – 40,44; p = 0,096) | 28,46 (1,73 – 467,57; p = 0,019) | |
Метастазы в печень Liver mts | (-) | 93 (91,2) | – | – |
(+) | 9 (8,8) | 0,53 (0,13 – 2,22; p = 0,388) | 0,07 (0,01 – 0,66; p = 0,020) | |
Прогноз по IMDC IMDC prognosis | Благоприятный Favorable | 14 (13,7) | – | – |
Промежуточный Intermediate | 59 (57,8) | 1,35 (0,55 – 3,29; p = 0,516) | 2,73 (0,89 – 8,37; p = 0,079) | |
Неблагоприятный Poor | 29 (28,4) | 4,57 (1,85 – 11,32; p = 0,001) | 37,67 (7,40 – 191,87; p < 0,001) |
Обсуждение
Данное исследование представляет анализ ЦРП и ЦНЭ, выполненных с 2014 по 2022 год. На современном этапе ЦРП при мПКР применяется редко, поэтому очень важно оценить эффективность данного циторедуктивного метода лечения. В нашей работе установлено, что ЦРП у пациентов мПКР составила 5,4% от всех выполненных циторедуктивных операций. Этот показатель несколько выше, чем в работе N. Hauser et al. (2024), где он составил 4,7% [15]. Интересно, что общая доля ЦРП по сравнению со всеми циторедуктивными операциями существенно не изменилась с 2010 по 2017 годы (4,8% и 4,7% соответственно), что подтверждается результатами нашего исследования [15]. Это противоречит данным исследования A.T. Lenis et al. (2018), в котором авторы обнаружили увеличение частоты ЦРП с 1,8 до 4,3% в период с 2006 по 2013 год [11]. В том же исследовании было установлено, что пациентам с мПКР, поступающим в научно-исследовательские центры, чаще выполняли ЦРП за тот же период (ОР = 1,44; p = 0,004). Кроме того, в данном анализе было отмечено значительное увеличение использования малоинвазивных методов для проведения ЦРП, с 16,0% операций в 2010 году до 42,2% в 2017 году. Решение о проведении ЦРП при метастатическом процессе определялось категорией Т. Пациенты, у которых диагностирована сТ1 без N+, чаще подвергались ЦРП (93,7%), что подтверждается данными N. Hauser et al. (2024) [15]. J. Chen et al. (2020) обнаружили, что риск смерти у пациентов мПКР при выполнении ЦРП с N1 был в 5,48 раза выше, чем у пациентов с N0, что говорит о том, что более высокая стадия и статус N1 имеют худшие исходы [14]. В нашей работе только у 2 (6,2%) пациентов в группе ЦРП была выявлена категория N1. Анализ подгрупп продемонстрировал преимущество ЦРП над ЦНЭ в отношении показателей выживаемости у пациентов с изолированным отдалённым метастазированием [16]. В нашем исследовании у больных с олигометастазами ПКР показатели 5-летней ОВ в группах ЦРП и ЦНЭ составили 56,2% и 85,51% соответственно. В предыдущих работах было высказано предположение, что при местнораспространённых больших опухолях риск снижения функции почек и смертности выше, поэтому необходимо прилагать возможные усилия для сохранения функции почек [17]. В нашей работе только 5 больным из 32 с Т2 – Т3 были выполнены ЦРП, а в группе ЦНЭ — 56 пациентам.
Таким образом, отбор пациентов имеет решающее значение, поскольку ЦРП может быть полезной в некоторых случаях мПКР с первичной опухолью cT1 и олигометастатическим заболеванием. Этот анализ подтверждает решение о том, что ЦРП может быть осуществима с приемлемыми периоперационными результатами при опухолях cT1. E. Mazzone et al. (2018) не обнаружили существенной разницы в частоте осложнений (ОР: 1,00; p = 0,9) и внутрибольничной смертности (ОР: 1,2; p = 0,8) между ЦНЭ и ЦРП [18]. Однако с учётом того, что ЦРП применялась в основном в тех случаях, когда объём первичной опухоли был небольшим, эти различия в показателях ОВ и периоперационных результатах могут быть обусловлены стадией заболевания, а не хирургической стратегией. Эти различия также могут быть обусловлены ошибкой отбора в пользу пациентов с ЦРП, имеющих небольшие первичные опухоли почек. В исследовании, посвящённом влиянию нефронсохраняющих операций на показатели выживаемости пациентов с мПКР, было выявлено, что только 1% пациентов с размером первичной опухоли ≥ 7 см подвергся ЦРП [19]. А в нашем исследовании 10,7% пациентов со стадией Т2 – Т3 было подвергнуто ЦРП. J. Tian et al. (2023) обнаружили, что средний размер опухоли был больше у пациентов, которым проводилась ЦНЭ, по сравнению с ЦРП (7,50 см против 4,95 см; p < 0,001, соответственно) [8]. Мы не проводили исследование в отношении связи размеров первичной опухоли и выполнения ЦРП и ЦНЭ. Современные работы свидетельствуют о том, что ЦРП не уступает и может улучшать показатели выживаемости по сравнению с ЦНЭ, несмотря на различия в размерах первичной опухоли при сопоставимом анализе.
Усовершенствованные технологии, которые недавно начали внедряться в технику проведения ЦРП, такие как использование интраоперационного ультразвукового исследования (ИУИ), могут привести к увеличению показателей ОВ, поскольку вероятность достижения негативных краев при резекции опухоли выше. I. Mihai et al. (2024) обнаружили, что при использовании ИУИ при ЦРП уменьшается частота негативных краев, а также значительно снижается кровопотеря, сокращается медиана продолжительности операции и время ишемии (p = 0,001) [20]. Эти результаты позволяют предположить, что новые достижения могут оказать влияние на показатели ОВ пациентов, подвергшихся ЦРП с использованием ИУИ, по сравнению с пациентами, которым выполнена ЦНЭ. В нашей группе при ЦРП ИУИ выполнялась у 14 (43,7%) пациентов. В группе ЦРП была выше доля cвПКР (60,9% против 57,5%; p < 0,001), в нашей работе, напротив, — 84,4% и 97,1% соответственно. С учётом преимущества ЦРП в отношении показателей выживаемости, отмеченного в литературе, патологический тип cвПКР может быть положительным предиктором показателей ОВ у пациентов с мПКР. Было показано, что коморбидность снижает показатели выживаемости пациентов с мПКР, независимо от возраста [20]. В настоящем исследовании статус ECOG статистически значимо влиял на показатели ОВ в группе ЦРП (р = 0,032).
В исследовании Н.Р. Kale et al. (2019) было показано, что средняя продолжительность пребывания в стационаре для всех циторедуктивных операций составила 5,0 ± 5,9 дня, при этом она была несколько короче для пациентов, перенёсших ЦРП — 4,6 ± 6,4 дня (р = 0,06) [6]. Это также подтверждается нашими результатами — 3,8 ± 6,2 и 5,2 ± 5,7 дня соответственно (р = 0,03). Разница в продолжительности пребывания в стационаре между ЦРП и ЦНЭ является статистически значимой и может оказать реальное влияние на финансовое бремя больничных систем. Возможность выполнить процедуру, которая значительно сокращает среднюю продолжительность пребывания пациентов в стационаре, имеет решающее значение для избежания ненужных расходов пациента и больницы, а также для обеспечения лучшего качества жизни больных. 30-дневная и 90-дневная смертность существенно не отличались между ЦНЭ и ЦРП.
В исследовании N. Hauser et al. (2024) показатели 5-летней ОВ составили в группе ЦРП и ЦНЭ 40,7% и 29,2% соответственно, что не соответствует результатам нашей работы (62,9% и 68,1%). Полученные данные не свидетельствуют о преимуществе показателей ОВ для пациентов, перенёсших ЦРП по сравнению с ЦНЭ, хотя показатели ОВ в наших обеих группах выше, чем у предыдущих авторов [15]. Полученные данные свидетельствуют о преимуществе хирургических результатов и показателей ОВ у пациентов, перенёсших ЦРП, по сравнению с ЦНЭ.
Заключение
На данный момент нет консенсуса по тактике проведения циторедуктивной резекции почки при мПКР. Анализ предыдущих исследований показал, что показатели выживаемости пациентов с мПКР, которым выполнялась ЦРП, выше, чем при проведении ЦНЭ. Необходимы дальнейшие исследования, чтобы определить, какие пациенты лучше всего подходят для данного паллиативного вида лечения с целью повышения показателей выживаемости.
Список литературы
1. Padala SA, Barsouk A, Thandra KC, Saginala K, Mohammed A, Vakiti A, Rawla P, Barsouk A. Epidemiology of Renal Cell Carcinoma. World J Oncol. 2020;11(3):79-87. DOI: 10.14740/wjon1279
2. Capitanio U, Bensalah K, Bex A, Boorjian SA, Bray F, Coleman J, Gore JL, Sun M, Wood C, Russo P. Epidemiology of Renal Cell Carcinoma. Eur Urol. 2019;75(1):74-84. DOI: 10.1016/j.eururo.2018.08.036
3. Harmon SA, Tuncer S, Sanford T, Choyke PL, Türkbey B. Artificial intelligence at the intersection of pathology and radiology in prostate cancer. Diagn Interv Radiol. 2019;25(3):183-188. DOI: 10.5152/dir.2019.19125
4. Studentova H, Spisarova M, Kopova A, Zemankova A, Melichar B, Student V Jr. The Evolving Landscape of Cytoreductive Nephrectomy in Metastatic Renal Cell Carcinoma. Cancers (Basel). 2023;15(15):3855. DOI: 10.3390/cancers15153855
5. Motzer RJ, Jonasch E, Agarwal N, Alva A, Baine M, Beckermann K, Carlo MI, Choueiri TK, Costello BA, Derweesh IH, Desai A, Ged Y, George S, Gore JL, Haas N, Hancock SL, Kapur P, Kyriakopoulos C, Lam ET, Lara PN, Lau C, Lewis B, Madoff DC, Manley B, Michaelson MD, Mortazavi A, Nandagopal L, Plimack ER, Ponsky L, Ramalingam S, Shuch B, Smith ZL, Sosman J, Dwyer MA, Gurski LA, Motter A. Kidney Cancer, Version 3.2022, NCCN Clinical Practice Guidelines in Oncology. J Natl Compr Canc Netw. 2022;20(1):71-90. DOI: 10.6004/jnccn.2022.0001
6. Kale HP, Mays DP, Nadpara PA, Slattum PW, Paul AK, Carroll NV. Economic burden of renal cell carcinoma among older adults in the targeted therapy era. Urol Oncol. 2019;37(6):356.e19-356.e28. DOI: 10.1016/j.urolonc.2019.01.016
7. Flanigan RC, Campbell SC, Clark JI, Picken MM. Metastatic renal cell carcinoma. Curr Treat Options Oncol. 2003;4(5):385-390. DOI: 10.1007/s11864-003-0039-2
8. Tian J, Zeng X, Zhu J, Guan W, Hu Z, Yang C. Cytoreductive partial and radical nephrectomies provide equivalent oncologic outcomes in T1- 2M1 renal cell carcinoma. Transl Cancer Res. 2023;12(2):301-309. DOI: 10.21037/tcr-22-1389
9. Bhat S. Role of surgery in advanced/metastatic renal cell carcinoma. Indian J Urol. 2010;26(2):167-176. DOI: 10.4103/0970-1591.65381
10. Shahait M, Mukherji D, El-Hout Y. Partial nephrectomy for metastatic renal cell carcinoma: Where do we stand? Indian J Urol. 2015;31(2):102- 105. DOI: 10.4103/0970-1591.154300
11. Lenis AT, Salmasi AH, Donin NM, Faiena I, Johnson DC, Drakaki A, Gollapudi K, Blumberg J, Belldegrun AS, Pantuck AJ, Chamie K. Trends in usage of cytoreductive partial nephrectomy and effect on overall survival in patients with metastatic renal cell carcinoma. Urol Oncol. 2018;36(2):78.e21-78.e28. DOI: 10.1016/j.urolonc.2017.09.030
12. Karam JA, Babaian KN, Tannir NM, Matin SF, Wood CG. Role of partial nephrectomy as cytoreduction in the management of metastatic renal cell carcinoma. Minerva Urol Nefrol. 2015;67(2):149-156. PMID: 25645343.
13. Babaian KN, Merrill MM, Matin S, Tamboli P, Tannir NM, Jonasch E, Wood CG, Karam JA. Partial nephrectomy in the setting of metastatic renal cell carcinoma. J Urol. 2014;192(1):36-42. DOI: 10.1016/j.juro.2014.01.086
14. Chen J, He Q, Liu W, Li Y, Zhuang W. The Effect of Cytoreductive Partial Nephrectomy in Elderly Patients with Metastatic Renal Cell Carcinoma. Clin Interv Aging. 2020;15:431-439. DOI: 10.2147/CIA.S243902
15. Hauser N, Giakas J, Robinson H, Davaro F, Hamilton Z. Utilization of Partial Cytoreductive Nephrectomy in Patients with Metastatic Renal Cell Carcinoma. J Clin Med. 2024;13(19):5767. DOI: 10.3390/jcm13195767
16. Kutikov A, Uzzo RG. The R.E.N.A.L. nephrometry score: a comprehensive standardized system for quantitating renal tumor size, location and depth. J Urol. 2009;182(3):844-853. DOI: 10.1016/j.juro.2009.05.035
17. Dey S, Hamilton Z, Noyes SL, Tobert CM, Keeley J, Derweesh IH, Lane BR. Chronic Kidney Disease Is More Common in Locally Advanced Renal Cell Carcinoma. Urology. 2017;105:101-107. DOI: 10.1016/j.urology.2017.03.033
18. Mazzone E, Nazzani S, Preisser F, Tian Z, Marchioni M, Bandini M, Capitanio U, Kapoor A, Tilki D, Montorsi F, Shariat SF, Saad F, Briganti A, I Karakiewicz P. Partial nephrectomy seems to confer a survival benefit relative to radical nephrectomy in metastatic renal cell carcinoma. Cancer Epidemiol. 2018;56:118-125. DOI: 10.1016/j.canep.2018.08.006
19. Hellenthal NJ, Mansour AM, Hayn MH, Schwaab T. Is there a role for partial nephrectomy in patients with metastatic renal cell carcinoma? Urol Oncol. 2013;31(1):36-41. DOI: 10.1016/j.urolonc.2010.08.026
20. Mihai I, Dura H, Teodoru CA, Todor SB, Ichim C, Grigore N, Mohor CI, Mihetiu A, Oprinca G, Bacalbasa N, Tanasescu D, Bratu DG, Boicean A, Oros B, Hasegan A. Intraoperative Ultrasound: Bridging the Gap between Laparoscopy and Surgical Precision during 3D Laparoscopic Partial Nephrectomies. Diagnostics (Basel). 2024;14(9):942. DOI: 10.3390/diagnostics14090942
Об авторах
Д. В. СеменовРоссия
Дмитрий Владимирович Семенов
Санкт-Петербург
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
Р. В. Орлова
Россия
Рашида Вахидовна Орлова — д-р мед. наук, профессор
Санкт-Петербург
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
В. И. Широкорад
Россия
Валерий Иванович Широкорад — д-р мед. наук
Санкт-Петербург
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
С. В. Кострицкий
Россия
Станислав Викторович Кострицкий — канд. мед. наук
Санкт-Петербург
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
Рецензия
Для цитирования:
Семенов Д.В., Орлова Р.В., Широкорад В.И., Кострицкий С.В. Сравнение циторедуктивной резекции почки и циторедуктивной нефрэктомии у пациентов с метастатическим почечноклеточным раком. Вестник урологии. 2026;14(1):60-70. https://doi.org/10.21886/2308-6424-2026-14-1-60-70
For citation:
Semyonov D.V., Orlova R.V., Shirokorad V.I., Kostritsky S.V. Cytoreductive partial nephrectomy versus cytoreductive nephrectomy in metastatic renal cell carcinoma. Urology Herald. 2026;14(1):60-70. (In Russ.) https://doi.org/10.21886/2308-6424-2026-14-1-60-70
JATS XML