Перейти к:
Оценка влияния L-карнитина на качество эякулята в экспериментальной модели варикоцеле
https://doi.org/10.21886/2308-6424-2026-14-1-45-52
Аннотация
Введение. Одной из причин нарушения сперматогенеза с хорошо изученным механизмом повреждения тестикулярной ткани является варикоцеле. В борьбе с окислительным стрессом наиболее изучен L-карнитин, оптимизирующий метаболизм сперматозоидов, положительно влияющий на их созревание и подвижность. Тем не менее в доступной литературе имеются противоречивые данные по оценке влияния карнитинов на эякулят в реальной клинической практике.
Цель исследования. Изучить влияние L-карнитина на показатели спермограммы при варикоцеле в хроническом эксперименте.
Материалы и методы. В эксперименте задействованы 15 кроликов-самцов, рандомизированных в 3 группы: группа 1 — интактные животные (n = 5); группа 2 (группа контроля) — животные с моделью варикоцеле без лекарственного воздействия, вывод через месяц после формирования патологии (n = 5); группа 3 (основная группа) — животные с моделью варикоцеле и лекарственным воздействием в течение месяца с момента формирования патологии (n = 5). Варикоцеле создавали путём сужения просвета левой почечной вены на 1/2 – 2/3 исходного диаметра и дополнительно введения гонадотропина 300 ед/кг веса и 0,2 мл 1% раствора прогестерона в сутки в течение 10 суток, начиная за сутки до сужения почечной вены. В экспериментальных группах препарат вводили внутрижелудочно в дозе по L-карнитину 26,15 мг/сут с пересчётом на видовые особенности обмена веществ кролика. Семенную жидкость исследовали при помощи световой микроскопии с оценкой количества и качества сперматозоидов.
Результаты. Спустя 14 суток от создания модели у всех животных визуализировали семенные вены (до 1,8 мм, без различий между группами) и регистрировали рефлюкс. Средний диаметр семенных вен был равен 2,1 мм на 30-е сутки. Отмечено прогрессирующее уменьшение объёма левого семенника в течение 30 суток в среднем на 0,6 см3 (с 0,77 см3 до 0,71 см3) (p > 0,05 между всеми группами). В группе 1 исходные характеристики общих показателей спермограммы были достоверно выше, чем в группах 2 и 3 (p < 0,05 – 0,01). Общее количество сперматозоидов — 310,2 млн (группа 1), 199,3 млн (группа 2) и 247,6 млн (группа 3). Показатели спермограммы в группе 2 были значимо ниже, чем в группе 3 со следующим соотношением: общее количество сперматозоидов — 199,3 / 247,6 млн (живые формы — 68,3 / 80,6%, PR + NP — 61,5 / 73,4%, PR — 48,7 / 65,4%, скорость сперматозоидов — 4 / 8 мк/с) (p < 0,01).
Заключение. В эксперименте на модели варикоцеле при сохраняющемся действии альтерирующего фактора применение антиоксидантного комплекса на основе L-карнитина улучшает качественные и количественные параметры эякулята.
Для цитирования:
Маслюков А.В., Мозговой С.И., Цуканов Ю.Т., Теленков В.Н., Цуканов А.Ю., Халаман В.В. Оценка влияния L-карнитина на качество эякулята в экспериментальной модели варикоцеле. Вестник урологии. 2026;14(1):45-52. https://doi.org/10.21886/2308-6424-2026-14-1-45-52
For citation:
Maslyukov A.V., Mozgovoy S.I., Tsukanov Yu.T., Telenkov V.N., Tsukanov A.Yu., Khalaman V.V. Assessment of L-Carnitine's effect on semen quality in an experimental varicocele animal model. Urology Herald. 2026;14(1):45-52. (In Russ.) https://doi.org/10.21886/2308-6424-2026-14-1-45-52
Введение
Бесплодие является глобальной проблемой, затрагивающей около 15% супружеских пар, что составляет примерно 48,5 миллиона пар во всем мире. Согласно статистике, мужской фактор является причиной бесплодия в 50% случаев, и это определяет высокую актуальность для изучения его развития и способов лечения [1][2]. В целом причины нарушения сперматогенеза разнообразны, но непосредственный механизм повреждения тестикулярной ткани достаточно универсален и сводится к явлению оксидативного стресса [3][4].
Одной из причин патоспермии с хорошо изученным механизмом альтерации является варикоцеле [5 – 8]. Предопределяют оксидативный стресс при варикоцеле такие факторы, как гипоксия, локальная гипертермия, микроделеции митохондриальных генов, недостаточность белков теплового шока, экспрессии каспаз, Bak, р53 и ряда других факторов, нарушающих соотношение пролиферация / апоптоз сперматогенных клеток [9].
Считается, что антиоксиданты улучшают качество спермы за счёт уменьшения окислительного повреждения [10][11]. Высокую эффективность антиоксидантов демонстрируют результаты ряда научных исследований [3][4][12]. Так, недавний систематический обзор сообщает о повышении частоты клинической беременности при приёме антиоксидантов (ОШ 1,89; 95% ДИ от 1,45 до 2,47; р < 0,00001) 20 рандомизированных клинических исследований (1706 мужчин, I2 = 3%) по сравнению с плацебо, но при доказательствах низкой определённости. Несмотря на полученное отношение шансов, авторы говорят о необходимости дальнейших крупных, хорошо спланированных рандомизированных плацебо-контролируемых исследований для выяснения точной роли антиоксидантов в лечении бесплодных мужчин с оценкой о наступлениях беременности и живорождениях [13].
Одним из широко обсуждаемых веществ в контексте антиоксидантной терапии мужского бесплодия является L‑карнитин. Это достаточно давно известная аминокислота, обнаруживаемая в придатках яичка, семенной плазме и сперматозоидах. Карнитины участвуют в метаболизме сперматозоидов, положительно влияя на их подвижность и созревание [14]. В последние годы были опубликованы работы, посвящённые различным аспектам применения L‑карнитина непосредственно при варикоцеле [10][11][15], однако результаты исследований весьма неоднозначны [16], что диктует необходимость дальнейшего изучения проблемы.
Одним из путей изучения влияния различных видов лечения на процесс нарушенного сперматогенеза, помимо клинических исследований, является экспериментальный. В связи с этим представляется обоснованным изучение различных вариантов фармакологической поддержки сперматогенеза в хроническом эксперименте на животных. Варикоцеле является патологией, относительно легко моделируемой в хроническом эксперименте. А поскольку оно включает в себя основной набор альтерирующих ткань яичка при мужском бесплодии факторов, то именно модель варикоцеле представляется возможным использовать для изучения эффективности медикаментозной коррекции нарушения функции гонад [17][18].
Цель исследования: изучить влияние L‑карнитина на показатели спермограммы при экспериментальном варикоцеле.
Материалы и методы
В хроническом эксперименте были задействованы 15 половозрелых кроликов-самцов породы Серый Великан (Oryctolagus cuniculus) в возрасте 4,5 – 5,5 месяца. Средняя масса животного составила 3 кг. К вязке животных не допускали. Эксперимент проведён в соответствии с правилами, принятыми Европейской конвенцией по защите позвоночных животных, используемых для экспериментальных и иных научных целей (Страсбург, 1986). Исследование выполнено на базе кафедры анатомии, гистологии, физиологии и патологической анатомии факультета ветеринарной медицины Омского государственного аграрного университета им. П.А. Столыпина. Исследование одобрено ЛЭК ФГБОУ ВО ОмГМУ Минздрава России (№ 111, от 14.06.2019 года).
Перед проведением исследования каждому животному был присвоен индивидуальный номер от 1 до 15. Все животные были рандомизированы и распределены на три группы:
- Группа 1 — интактные животные. Предоставление нормальной анатомии семенника и показателей спермограммы (n = 5).
- Группа 2 (группа контроля) — животные с моделью варикоцеле без лекарственного воздействия, вывод из эксперимента через 1 месяц после формирования патологии (n = 5).
- Группа 3 (основная группа) — животные с моделью варикоцеле и лекарственным воздействием в течение 1-го месяца с момента формирования патологии (n = 5).
Создание варикоцеле в эксперименте. Варикоцеле создавали путём сужения просвета почечной вены на 1/2 – 2/3 исходного диаметра и дополнительного парентерального введения гонадотропина 300 ед/кг веса и 0,2 мл 1% раствора прогестерона в сутки в течение 10 суток, начиная за сутки до сужения почечной вены. Критерием создания модели варикоцеле считали регистрацию при дуплексном ангиосканировании увеличения диаметра вен семенного канатика в 2 раза от исходного / сам факт их визуализации / регистрация рефлюксной волны крови длительностью более 1 секунды. Рефлюкс провоцировали мануальной компрессией брюшной полости (приём, заменяющий пробу Valsalva, в связи с тем, что волевое натуживание у животного невозможно) [18][19].
Основные этапы операции: под общей анестезией выполняли лапаротомию левым боковым доступом, в забрюшинной клетчатке выделяли левую почечную и впадающую в неё левую яичковую вены. Дистальнее яичковой вены лигировали почечную вену на 1/2 – 2/3 просвета сосуда монофиламентной нерассасывающейся нитью (4-0) (рис. 1, 2).
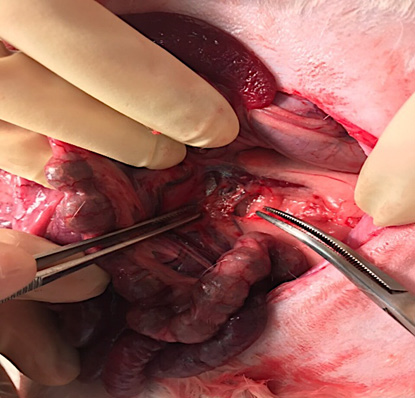
Рисунок 1. Диссекция сосудистой ножки
Figure 1. Dissection of the renal vascular pedicle

Рисунок 2. Селективное сужение левой почечной вены на 1/2 – 2/3 исходного диаметра
Figure 2. Selective narrowing of the left renal vein to 1/2 – 2/3 of its original diameter
Для контроля формирования варикоцеле на 7-е, 14-е и 30-е сутки выполняли ультразвуковое исследование семенников в режиме серой шкалы и допплеровского картирования. Модель формировалась к исходу 7-х суток с момента операции.
В группе 3 введение тестируемых образцов препарата осуществляли в течение 1 месяца (через 7 дней после операции по созданию модели).
В экспериментальных группах препарат в форме порошка вводили внутрижелудочно в дозе по L‑карнитину 26,15 мг/сут с пересчётом на видовые особенности обмена веществ кролика [20].
Сбор и подготовка проб. Сбор эякулята осуществляли при помощи искусственной вагины для кролика. Семенную жидкость исследовали при помощи световой микроскопии с оценкой количества и качества сперматозоидов.
Животные групп 2 и 3 выведены из эксперимента через 1 месяц.
Статистический анализ. Обработка и анализ массива статистических данных выполнялись с помощью пакета прикладных программ “IBM SPSS Statistics v.22.0” (SPSS: An IBM Company, IBM SPSS Corp., Armonk, NY, USA). Нормальность распределения проверяли с помощью теста Shapiro-Wilk. Количественные данные описывались с помощью медианы (Me) и нижнего и верхнего квартилей [ Q1; Q3]. Категориальные данные описывались с указанием абсолютных значений (n) и процентных долей (%). Сравнение двух групп по количественному показателю, распределение которого отличалось от нормального, выполнялось с помощью U-критерия Mann-Whitney c модулем Probabilistic Index при неравенстве дисперсий (M-W test). Сравнение процентных долей при анализе многопольных таблиц сопряженности выполнялось с помощью критерия Pearson`s chi-square (χ²). Принятые уровни достоверности р < 0,05, <0,01.
Результаты
При ультразвуковом ангиосканировании у животных группы 1 лишь у одного была зафиксирована семенная вена диаметром 0,6 мм. У остальных — не визуализированы. Рефлюкса также не было. Объём семенника в среднем составил 0,77 см³.
Спустя 14 суток от создания модели у всех животных групп 2 и 3 визуализированы семенные вены (до 1,8 мм, р > 0,05 между группами) и зарегистрирован рефлюкс (рис. 3A, 3B). Средний диаметр семенных вен (до 2,1 мм) был зарегистрирован на 30-е сутки.

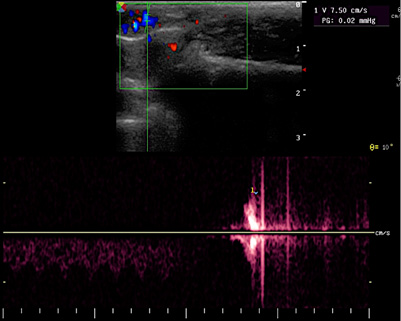
Рисунок 3. Эхограмма (А) и допплерограмма (В) на 30-е сутки. При мануальной компрессии брюшной полости определён рефлюкс по семенным венам кролика со скоростью 7,5 см/с
Figure 3. Echogram (A) and Doppler image (B) on day 30. During manual compression of the abdomen, reflux in the rabbit’s spermatic veins was detected with a flow velocity of 7.5 cm/s
Отмечено прогрессирующее уменьшение объёма левого семенника в течение 30 суток в среднем на 0,6 см³ (с 0,77 см³ до 0,71 см³) (p > 0,05 между группами).
При анализе спермограмм в группе 3 отмечена в разной степени положительная динамика, что отражено в таблице.
Таблица. Анализ основных показателей спермограммы
Table. Analysis of the main semen parameters
Группа | Group | 1 | 2 | 3 |
Общее количество сперматозоидов (млн) | Total number of spermatozoa (mln) | 310,2 | 199,3** | 247,6* |
% живых форм | % of living forms | 94,3 | 68,3** | 80,6* |
Количество патологических форм (на 100 сперм) | Number of pathological forms (per 100 sperm) | 2 | 9** | 6* |
Общая подвижность (PR + NP)% | General mobility (PR + NP)% | 91,4 | 61,5** | 73,4* |
Прогрессивно-подвижные (PR) % | Progressive-mobile (PR) % | 87,2 | 48,7** | 65,4* |
Скорость сперматозоидов (мк/с) | Sperm rate (mk/s) | 13 | 4** | 8* |
Количество лейкоцитов (млн/мл) | White blood cell count (mln/ml) | 0,02 | 0,32** | 0,19* |
Примечание. Данные представлены в виде медиан. Уровень различий в сравнении с нормой: * р < 0,05; ** р < 0,01
Note. Data are presented as medians. Degree of difference versus normal: * p < 0.05; ** p < 0.01
Сравнительный анализ спермограмм групп 2 и 3 продемонстрировал наличие различий от нормы по всем оцениваемым показателям.
В группе 1 исходные характеристики общих показателей спермограммы были достоверно выше, чем в группах 2 и 3 (p < 0,05 — 0,01). Общее количество сперматозоидов — 310,2 млн (группа 1), 199,3 млн (группа 2) и 247,6 млн (группа 3). В группе 1 из общего количества 310,2 млн 94,3% — живые формы, PR + NP — 91,4%, PR — 87,2% и скоростью сперматозоидов — 13 мк/с.
Показатели спермограммы в группе 2 были значимо ниже, чем в группе 3 с соотношением: общее количество сперматозоидов — 199,3 / 247,6 млн (живые формы — 68,3 / 80,6%; PR + NP — 61,5 / 73,4%; PR — 48,7 / 65,4%; скорость сперматозоидов — 4 / 8 мк/с) (p < 0,01).
Таким образом, животные группы 3 имели лучшие показатели сперматогенеза, в отличие от группы 2.
Обсуждение
Согласно данным литературных источников, у мужчин с первичным бесплодием варикоцеле встречается в 35 – 40% случаев, а при вторичном бесплодии данный показатель может достигать 80% [12]. Патогенез бесплодия, вызванного варикоцеле, представляет собой сложный процесс, включающий различные механизмы, оказывающие пагубное воздействие на сперматогенез [21], что подтверждается результатами настоящего исследования. Одним из ведущих механизмов в патогенезе бесплодия, ассоциированного с варикоцеле, является оксидативный стресс [12][22]. Варикоцеле может приводить к повышению активных форм кислорода, изменению уровня гормонов, нарушению плотных контактов между поддерживающими клетками и повреждению гематотестикулярного барьера [21]. Повреждение гематотестикулярного барьера может стимулировать аутоиммунную реакцию в яичках с агглютинацией сперматозоидов, снижением количества, концентрации, подвижности сперматозоидов и, в итоге, развитием бесплодия [21].
Результаты настоящего исследования указывают на существенную роль варикоцеле в развитии патоспермии, что согласуется с данными, полученными в исследованиях других авторов [22][23]. Так, в исследовании Р.И. Панченко с соавторами (2022) у пациентов, страдающих варикоцеле, в 100% случаев регистрировалась астенозооспермия, в 14% — олигозооспермия, в 23% — тератозооспермия [22].
На сегодняшний день результаты многих исследований демонстрируют эффективность варикоцелэктомии при лечении бесплодия у мужчин с варикоцеле. После хирургического вмешательства отмечено улучшение качества эякулята [24]. Между тем существует только три показания для хирургического лечения варикоцеле: наличие болевого синдрома в мошонке при физической нагрузке; нарушения сперматогенеза, приводящие к мужскому бесплодию и / или репродуктивным потерям; прогрессирующая гипотрофия яичка на стороне поражения [25]. Данный факт обусловливает необходимость поиска эффективных методов консервативного лечения и профилактики патоспермии при варикоцеле, что доказывают результаты многоцентрового исследования A. Shomarufov et al. (2025), посвящённого оценке эффективности микрохирургической варикоцелэктомии и антиоксидантной терапии в улучшении показателей спермы и снижении фрагментации ДНК. Результаты данного исследования свидетельствуют о том, что микрохирургическая варикоцелэктомия наряду с антиоксидантной терапией способствует улучшению параметров спермы: повышению концентрации сперматозоидов и их подвижности. По мнению авторов, антиоксидантная терапия является хорошей альтернативой или дополнением при лечении пациентов с варикоцеле, которым не показано оперативное лечение [23], что также подтверждает настоящее исследование.
Довольно большое количество экспериментальных и клинических исследований посвящено оценке роли антиоксидантов при лечении инфертильных пациентов с варикоцеле [12]. Среди иных антиоксидантов большой интерес учёных вызывает L‑карнитин, установлено его снижение у мужчин с варикоцеле и патоспермией. Так, T. Mostafa et al. (2022) изучали уровень L‑карнитина в семенной плазме 86 мужчин: 45 мужчин с бесплодием, вызванным азооспермией и варикоцеле, 21 мужчина с бесплодием, вызванным азооспермией, без варикоцеле, и 20 фертильных мужчин. Авторы установили, что средние уровни L‑карнитина в семенной плазме были значительно ниже у бесплодных мужчин с олигоастенотератозооспермией с варикоцеле (216,3 ± 57,1 нг/мл) по сравнению с бесплодными мужчинами олигоастенотератозооспермией без варикоцеле (252,9 ± 62,9 нг/мл; р = 0,01) или фертильными мужчинами (382,8 ± 63,6 нг/мл; р = 0,001) [26].
L‑карнитин — эндогенный метаболит, представляющий собой четвертичный амин, основной функцией которого в клетках млекопитающих является перенос длинноцепочечных жирных кислот через внутреннюю митохондриальную мембрану для β-окисления и выработки энергии АТФ. L‑карнитин является мощным антиоксидантом, поглощающим свободные радикалы, кроме того, он поддерживает уровень свободного кофермента А в митохондриях [4]. По данным ряда исследований, приём L‑карнитина способствует улучшению параметров спермы: концентрации, подвижности сперматозоидов, общего количества эякулированных сперматозоидов [3]. Однако при проведении систематического обзора G. Tsampoukas et al. (2020) сделал выводы, что доказательств, подтверждающих роль L‑карнитина в качестве основного или вспомогательного средства при лечении варикоцеле, недостаточно, а имеющиеся на данный момент доказательства противоречивы [16].
Результаты настоящего исследования выявили наличие достоверных различий показателей спермограммы у лабораторных животных с варикоцеле со значительным их улучшением в группе животных, получающих L‑карнитин. Исследования in vitro показывают, что L‑карнитин оказывает прямое влияние на клетки Sertoli, улучшая развитие половых клеток и положительно влияя на мужскую фертильность [27].
Заключение
В эксперименте на модели варикоцеле, при сохраняющемся действии альтерирующего фактора, применение антиоксидантного комплекса на основе L‑карнитина повышает качественные и количественные параметры эякулята.
Список литературы
1. Лебедев Г.С., Голубев Н.А., Шадеркин И.А., Шадеркина В.А., Аполихин О.И., Сивков А.В. Комарова В.А. Мужское бесплодие в Российской Федерации: статистические данные за 2000–2018 годы. Экспериментальная и клиническая урология. 2019;(4):4-12.
2. Божедомов В.А. Шомаруфов А.Б., Божедомова Г.Е., Охоботов Д.А., Камалов Д.М., Камалов А.А. Варикоцеле и репродуктивная функция: эпидемиология и риск развития бесплодия (данные обследования 3908 мужчин). Урология. 2021;3:122-128. Bozhedomov VA, Shomarufov AB, Bozhedomova GE, Oxobotov DA, Kamalov DM, Kamalov AA. Varicocele and reproductive function: epidemiology and risk of infertility (survey data from 3908 men). Urologiia. 2021;3:122-128. (In Russian). DOI: 10.18565/urology.2021.3.122-128
3. Жукова О.В., Ших Е.В. Клинико-фармакологические подходы к применению антиоксидантной терапии при мужском бесплодии. Фармакология & Фармакотерапия. 2024;4:18-26.
4. Филиппова О.В., Леонова М.В. Синергизм компонентов в антиоксидантных комплексах для профилактики и лечения мужского бесплодия. Экспериментальная и клиническая урология. 2025;18(3):108-120.
5. Su JS, Farber NJ, Vij SC. Pathophysiology and treatment options of varicocele: An overview. Andrologia. 2021;53(1):e13576. DOI: 10.1111/and.13576
6. Байчоров Э.Х., Панченко Р.И. Варикоцеле как фактор нарушения сперматогенеза и снижения мужской фертильности. Астраханский медицинский журнал. 2023;18(1):6-16.
7. Shah R, Agarwal A, Kavoussi P, Rambhatla A, Saleh R, Cannarella R, Harraz AM, Boitrelle F, Kuroda S, Hamoda TAA, Zini A, Ko E, Calik G, Toprak T, Kandil H, Gül M, Bakırcıoğlu ME, Parekh N, Russo GI, Tadros N, Kadioglu A, Arafa M, Chung E, Rajmil O, Dimitriadis F, Malhotra V, Salvio G, Henkel R, Le TV, Sogutdelen E, Vij S, Alarbid A, Gudeloglu A, Tsujimura A, Calogero AE, El Meliegy A, Crafa A, Kalkanli A, Baser A, Hazir B, Giulioni C, Cho CL, Ho CCK, Salzano C, Zylbersztejn DS, Tien DMB, Pescatori E, Borges E, Serefoglu EC, Saïs-Hamza E, Huyghe E, Ceyhan E, Caroppo E, Castiglioni F, Bahar F, Gokalp F, Lombardo F, Gadda F, Duarsa GWK, Pinggera GM, Busetto GM, Balercia G, Cito G, Blecher G, Franco G, Liguori G, Elbardisi H, Keskin H, Lin H, Taniguchi H, Park HJ, Ziouziou I, de la Rosette J, Hotaling J, Ramsay J, Molina JMC, Lo KL, Bocu K, Khalafalla K, Bowa K, Okada K, Nagao K, Chiba K, Hakim L, Makarounis K, Hehemann M, Rodriguez Peña M, Falcone M, Bendayan M, Martinez M, Timpano M, Altan M, Fode M, Al-Marhoon MS, Sadighi Gilani MA, Soebadi MA, Gherabi N, Sofikitis N, Kahraman O, Birowo P, Kothari P, Sindhwani P, Javed Q, Ambar RF, Kosgi R, Ghayda RA, Adriansjah R, Condorelli RA, La Vignera S, Micic S, Kim SHK, Fukuhara S, Ahn ST, Mostafa T, Ong TA, Takeshima T, Amano T, Barrett T, Arslan U, Karthikeyan VS, Atmoko W, Yumura Y, Yuan Y, Kato Y, Jezek D, Cheng BK, Hatzichristodoulou G, Dy J, Castañé ER, El-Sakka AI, Nguyen Q, Sarikaya S, Boeri L, Tan R, Moussa MA, El-Assmy A, Alali H, Alhathal N, Osman Y, Perovic D, Sajadi H, Akhavizadegan H, Vučinić M, Kattan S, Kattan MS, Mogharabian N, Phuoc NHV, Ngoo KS, Alkandari MH, Alsuhaibani S, Sokolakis I, Babaei M, King MS, Diemer T, Gava MM, Henrique R, Silva RSE, Paul GM, Mierzwa TC, Glina S, Siddiqi K, Wu H, Wurzacher J, Farkouh A, Son H, Minhas S, Lee J, Magsanoc N, Capogrosso P, Albano GJ, Lewis SEM, Jayasena CN, Alvarez JG, Teo C, Smith RP, Chua JBM, Jensen CFS, Parekattil S, Finelli R, Durairajanayagam D, Karna KK, Ahmed A, Evenson D, Umemoto Y, Puigvert A, Çeker G, Colpi GM; Global Andrology Forum. Consensus and Diversity in the Management of Varicocele for Male Infertility: Results of a Global Practice Survey and Comparison with Guidelines and Recommendations. World J Mens Health. 2023;41(1):164-197. DOI: 10.5534/wjmh.220048
8. Agarwal A, Finelli R, Durairajanayagam D, Leisegang K, Henkel R, Salvio G, Aghamajidi A, Sengupta P, Crisóstomo L, Tsioulou PA, Roychoudhury S, Finocchi F, Darbandi M, Mottola F, Darbandi S, Iovine C, Santonastaso M, Zaker H, Kesari KK, Nomanzadeh A, Gugnani N, Rambhatla A, Duran MB, Ceyhan E, Kandil H, Arafa M, Saleh R, Shah R, Ko E, Boitrelle F. Comprehensive Analysis of Global Research on Human Varicocele: A Scientometric Approach. World J Mens Health. 2022;40(4):636- 652. DOI: 10.5534/wjmh.210202
9. Finelli R, Leisegang K, Kandil H, Agarwal A. Oxidative Stress: A Comprehensive Review of Biochemical, Molecular, and Genetic Aspects in the Pathogenesis and Management of Varicocele. World J Mens Health. 2022;40(1):87-103. DOI: 10.5534/wjmh.210153
10. Крупин В.Н., Нашивочникова Н.А., Уездный М.Н. Антиоксидантная терапия мужского бесплодия у пациентов с варикоцеле. Урологические ведомости. 2021;11(4):294-304.
11. Гамидов С.И., Попков В.М., Шатылко Т.В., Попова А.Ю., Королев А.Ю., Овчинников Р.И, Гасанов Н.Г. Место медикаментозной терапии в лечении мужчин с варикоцеле. Урология. 2018;(5):114-121.
12. Шатылко Т.В., Гамидов С.И., Попова А.Ю., Бицоев Т.Б. Роль антиоксидантов в лечении бесплодных мужчин с варикоцеле. Медицинский Совет. 2021;(13):23-33.
13. de Ligny W, Smits RM, Mackenzie-Proctor R, Jordan V, Fleischer K, de Bruin JP, Showell MG. Antioxidants for male subfertility. Cochrane Database Syst Rev. 2022;5(5):CD007411. DOI: 10.1002/14651858.CD007411.pub5
14. Жиборев Б.Н., Уваров А.Г., Звягина В.И., Фомина М.А. L-карнитин спермоплазмы в периконцепционной диагностике у пациентов с варикоцеле. Всероссийская научно-практическая конференция студентов и молодых специалистов с международным участием «Биохимические научные чтения памяти академика РАН Е.А. Строева»; Февраль 4-6, 2016; Рязань.
15. Гамидов С.И., Шатылко Т.В., Ли К.И., Гасанов Н.Г. Роль антиоксидантных молекул в терапии мужского бесплодия и подготовке мужчины к зачатию ребенка. Медицинский Совет. 2020;(3):122-129.
16. Tsampoukas G, Khan MF, Katsouri A, Akhter W, Moussa M, Deliveliotis K, Papatsoris A, Buchholz N. L-carnitine as primary or adjuvant treatment in infertile patients with varicocele. A systematic review. Arch Ital Urol Androl. 2020;92(3). DOI: 10.4081/aiua.2020.3.263
17. Цуканов А.Ю. Диагностика варикоцеле и выбор способа его оперативного лечения в свете новых данных об этиологии и патогенезе: Дис… док. мед. наук. Москва; 2006. Ссылка активна на 15.12.2025.
18. Патент РФ на изобретение № 2299477 C2/20.05.07. Бюл. №14. Цуканов А.Ю. Способ моделирования варикоцеле. Ссылка активна на 15.12.2025.
19. Цуканов Ю.Т., Маслюков А.В., Теленков В.Н., Лубягина Е.В., Цуканов А.Ю. Способ создания модели варикоцеле в хроническом эксперименте. Экспериментальная и клиническая урология. 2024;17(3):15-22.
20. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. Под ред. Хабриева Р.У. М.: Медицина, Изд-во Шико; 2005.
21. Wang LH, Zheng L, Jiang H, Jiang T. Research advances in inflammation and oxidative stress in varicocele-induced male infertility: a narrative review. Asian J Androl. 2025;27(2):177-184. DOI: 10.4103/aja202488
22. Панченко Р.И., Гармаш О.Н., Горбунков В.Я., Байчоров Э.Х. Новые подходы в лечении больных с варикоцеле при различных формах патоспермии в зависимости от возраста. Амбулаторная хирургия. 2022;19(1):108-112.
23. Shomarufov A, Bozhedomov V, Fozilov A, Abbosov S, Abdurakhimova L. Sperm DNA Fragmentation in Infertile Men With Varicocele: Clinical Epidemiology and Comparative Assessment of Microsurgical Varicocelectomy and Antioxidant Therapy. Front Biosci (Schol Ed). 2025;17(3):33393. DOI: 10.31083/FBS33393
24. Sountoulides P, Pyrgidis N, Kaltsas A, Gravas S, Kikidakis D, Zachos I, Zachariou A, Dimitriadis F, Sofikitis N. Comparative Impact of Microsurgical Varicocelectomy Versus Observation on Infertility in Infertile Men With Subclinical Varicocele. Cureus. 2025;17(1):e77477. DOI: 10.7759/cureus.77477
25. Овчинников Р.И., Ижбаев С.Х. Варикоцеле: нечасто обсуждаемые аспекты знакомой проблемы. Opinion Leader. 2021;6(47):50-54.
26. Mostafa T, Abougabal K, Mintziori G, Nabil N, Adel M, AboSief AF. Seminal L-Carnitine In Infertile Oligoasthenoteratozoospermic Men with Varicocele. J Reprod Infertil. 2022;23(1):26-32. DOI: 10.18502/jri.v23i1.8449
27. Mateus FG, Moreira S, Martins AD, Oliveira PF, Alves MG, Pereira ML. L-Carnitine and Male Fertility: Is Supplementation Beneficial? J Clin Med. 2023;12(18):5796. DOI: 10.3390/jcm12185796
Об авторах
А. В. МаслюковРоссия
Андрей Валерьевич Маслюков
Омск
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
С. И. Мозговой
Россия
Сергей Игоревич Мозговой — д-р мед. наук, доцент
Омск
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
Ю. Т. Цуканов
Россия
Антон Юрьевич Цуканов — д-р мед. наук, профессор
Омск
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
В. Н. Теленков
Россия
Владимир Николаевич Теленков — д-р. ветеринар. наук, доцент
Омск
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
А. Ю. Цуканов
Россия
Антон Юрьевич Цуканов — д-р мед. наук, профессор
Омск
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
В. В. Халаман
Россия
Виктория Викторовна Халаман
Омск
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
Рецензия
Для цитирования:
Маслюков А.В., Мозговой С.И., Цуканов Ю.Т., Теленков В.Н., Цуканов А.Ю., Халаман В.В. Оценка влияния L-карнитина на качество эякулята в экспериментальной модели варикоцеле. Вестник урологии. 2026;14(1):45-52. https://doi.org/10.21886/2308-6424-2026-14-1-45-52
For citation:
Maslyukov A.V., Mozgovoy S.I., Tsukanov Yu.T., Telenkov V.N., Tsukanov A.Yu., Khalaman V.V. Assessment of L-Carnitine's effect on semen quality in an experimental varicocele animal model. Urology Herald. 2026;14(1):45-52. (In Russ.) https://doi.org/10.21886/2308-6424-2026-14-1-45-52
JATS XML