Перейти к:
Эректильная функция у пациентов после пластики уретры
https://doi.org/10.21886/2308-6424-2025-13-1-19-26
Аннотация
Введение. На сегодняшний день развитие реконструктивной урологии демонстрирует высокие показатели эффективности лечения стриктур уретры, обеспечивая удовлетворительные параметры мочеиспускания. При этом существует потребность в поддержании высокого качества жизни, связанного с сексуальной функцией мужчин.
Цель исследования. Оценить эректильную функцию мужчин со стриктурной болезнью уретры в зависимости от наличия факторов риска эректильной дисфункции (ЭД), характеристик стриктур и применяемых методик хирургии.
Материалы и методы. В исследование включены 153 сексуально активных пациента со стриктурами уретры, подвергнутых хирургическому лечению. Оценку эректильной функции проводили с помощью использования опросника МИЭФ-5, при этом учитывали наличие у пациентов факторов риска развития ЭД (возраст, курение, ишемическая болезнь сердца, артериальная гипертензия, сахарный диабет), параметры стриктур (первичная / рецидивная, протяжённость) и технику хирургии (с пересечением и без пересечения спонгиозного тела). Контрольные точки оценки: исходно (до хирургии), через 3, 6, и 12 месяцев после уретропластики.
Результаты. Медиана возраста пациентов составила 53,0 года, показателей эректильной функции до операции — 19,0 балла. Вне зависимости от изучаемых параметров во всех группах исследования к 3-му месяцу наблюдения отмечено ухудшение показателей эректильной функции, которое регрессировало к году наблюдения. Длительность восстановления и тяжесть нарушения эректильной функции была связана с возрастом, курением, наличием ишемической болезни сердца и артериальной гипертензии, протяжённостью стриктуры и рецидивным характером стриктур. Значимых различий в показателях эректильной функции после оперативного вмешательства, в зависимости от степени пересечения спонгиозного тела, не выявлено. По результатам многофакторного анализа предикторами развития ЭД после операции являются возраст (СОШ 1,082; 95% ДИ 1,038 – 1,127; p < 0,001), артериальная гипертензия (СОШ 4,608; 95% ДИ 1,089 –19,511; p = 0,038) и исходный статус эректильной функции (СОШ 0,046; 95% ДИ 0,013 – 0,160; p < 0,001).
Заключение. Нарушения эректильной функции после хирургического лечения стриктур уретры имеют преимущественно транзиторный характер с регрессией к 12-му месяцу наблюдения. Негативное влияние на восстановление эректильной функции оказывают пожилой возраст, курение, сердечно-сосудистые заболевания, протяжённость и рецидивный характер стриктур.
Для цитирования:
Котов С.В., Ирицян М.М., Клименко А.А., Манцов А.А. Эректильная функция у пациентов после пластики уретры. Вестник урологии. 2025;13(1):19-26. https://doi.org/10.21886/2308-6424-2025-13-1-19-26
For citation:
Kotov S.V., Iritsyan M.M., Klimenko A.A., Mantsov A.A. Erectile function in patients after urethral plastic surgery. Urology Herald. 2025;13(1):19-26. (In Russ.) https://doi.org/10.21886/2308-6424-2025-13-1-19-26
Введение
Эректильная дисфункция (ЭД) является одной из наиболее значимых проблем мужского здоровья. Её распространённость в мире составляет 52% у мужчин в возрасте 40 – 70 лет [1]. Результаты анонимного анкетирования, проведённого в Российской Федерации, показали, что 49,7% включённых в исследование мужчин в возрасте от 20 до 75 лет отмечают у себя симптомы ЭД [2].
Рассматривая эректильную функцию у пациентов со стриктурами уретры, стоит отметить, что степень имеющихся отклонений в качестве сексуальной жизни может носить как органический, так и психологический характер и может быть связана не только со стриктурной болезнью, но и с имеющимися сопутствующими хроническими заболеваниями пациента, индивидуальным медицинским анамнезом и образом жизни [3]. Вполне логично предположить, что общепризнанные факторы риска ЭД, как немодифицируемые, так и модифицируемые, включая возраст, сердечно-сосудистые заболевания, сахарный диабет, ожирение, дислипидемию, гиперхолестеринемию, метаболический синдром, образ жизни (гиподинамия, курение), имеют своё влияние и на мужчин со стриктурами уретры. При этом с увеличением возраста пациента прогрессирует как частота встречаемости ЭД, так и сопутствующая патология [4][5].
Цель исследования: оценить эректильную функцию мужчин со стриктурной болезнью уретры в зависимости от наличия факторов риска ЭД, характеристик стриктур и применяемых методик хирургии.
Материалы и методы
Дизайн исследования. Одноцентровое клиническое простое лонгитюдное сравнительное исследование в параллельных группах с проспективной оценкой эректильной функции после реконструктивно-восстановительных операций на мочеиспускательном канале выполнено в ГКБ № 1 им. Н.И. Пирогова в период с 2019 по 2023 годы.
Этическое заявление: исследование спланировано и разработано в соответствии с положениями Хельсинкской декларации (пересмотренной в Fortaleza, Brasil, октябрь, 2013 год) и принципами Надлежащей клинической практики (GCP Guidelines), одобрено Локальным независимым этическим комитетом ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России (Протокол № 213 от 13 декабря 2021 года). Все пациенты подписывали информированное согласие на участие в исследовании и обработку персональных данных.
Характеристика выборки. Мужчины в возрасте от 18 до 80 лет со стриктурами уретры, которым выполнена пластика уретры (n = 153). Из исследования были исключены сексуально неактивные мужчины с длительно текущей ЭД тяжёлой степени, не проявляющие заинтересованности в половой жизни.
При оценке состояния эректильной функции учитывали наличие у пациентов факторов риска развития ЭД (возраст, курение, ишемическая болезнь сердца, артериальная гипертензия, сахарный диабет), параметры стриктур (первичная / рецидивная, протяжённость) и технику хирургии (с пересечением и без пересечения спонгиозного тела). Для этих целей пациенты были разделены на группы в зависимости от:
1) возрастной группы по ВОЗ: 18 – 44 года (n = 54), 45 – 59 лет (n = 43), 60 – 74 года (n = 47), 75 и более лет (n = 9);
2) курения табачной продукции: да (n = 47), нет (n = 106);
3) наличия в анамнезе ишемической болезни сердца: есть (n = 31), нет (n = 122);
4) наличия в анамнезе артериальной гипертензии: есть (n = 61), нет (n = 92);
5) наличия в анамнезе сахарного диабета 2 типа: есть (n = 17), нет (n = 136);
6) наличия в анамнезе предшествующего лечения стриктур уретры: первичные (n = 131), рецидивные (n = 22);
7) протяжённости дефекта мочеиспускательного канала: < 3 см (n = 95), ≥ 3,0 см (n = 58);
8) типа операции: с пересечением (n = 96), без пересечения (n = 57) спонгиозного тела.
Инициальное и наблюдательное обследование. На догоспитальном этапе всем пациентам выполняли стандартное предоперационное лабораторно-инструментальное обследование, необходимое и достаточное для оценки общего состояния здоровья, характеристик стриктур и выбора техники хирургии.
Оценку эректильной функции осуществляли посредством использования опросника «Международный индекс эректильной функции – 5 (МИЭФ-5)». Интерпретацию данных МИЭФ-5 производили по общепринятым пороговым значениям суммы баллов: 22 – 25 баллов — ЭД отсутствует; 17 – 21 — ЭД лёгкой степени; 12 – 16 — ЭД умеренно-лёгкой степени; 8 – 11 — ЭД умеренной степени; 5 – 7 — ЭД тяжёлой степени. Для оценки динамики показателей ЭФ сравнивали результаты исходного опроса (до хирургии) с результатами, полученными в контрольных точках наблюдения: 3, 6, и 12 месяцев после уретропластики.
Статистический анализ. Обработка и анализ массива статистических данных выполняли на персональном компьютере с помощью электронных таблиц “Microsoft Office Excel 2010” (Microsoft Corp., Redmond, WA, USA) и пакета прикладных программ “IBM SPSS Statistics v.22.0” (SPSS: An IBM Company, IBM SPSS Corp., Armonk, NY, USA), StatTech v.4.6.1 (ООО «Статтех», Россия). Информацию, полученную в процессе исследования, вносили в электронную базу данных посредством программы “Microsoft Office Excel”.
Нормальность распределения проверяли с помощью теста Колмогорова-Смирнова-Lilliefors. В случае отсутствия нормального распределения количественные данные описывали с помощью медианы (Me), нижнего и верхнего квартилей (Q1 – Q3). Категориальные данные описывали с указанием абсолютных значений и процентных долей (%). Сравнение двух групп по количественному показателю, распределение которого отличалось от нормального, выполняли с помощью U-критерия Mann-Whitney. При сравнении количественных показателей, распределение которых отличалось от нормального, в двух связанных группах использовали критерий Wilcoxon. Построение прогностической модели вероятности определённого исхода выполняли при помощи метода логистической регрессии. Для оценки связи между определённым исходом и фактором риска использовали метод соотношения шансов с расчётом нескорректированного (НОШ) и скорректированного соотношения шансов (CОШ) с границами 95% доверительного интервала (95% ДИ). Для оценки доли вариации зависимой переменной использовали коэффициент детерминации R² Nagelkerke.
Результаты
Медиана возраста пациентов составила 53 [ 38,0 – 64,0] года, показатель эректильной функции, по данным МИЭФ-5, — 19,0 [ 13,0 – 22,0] балла.
Возраст. Через 3 месяца после хирургического лечения во всех возрастных группах выявлено ухудшение эректильной функции, при этом у пациентов в возрасте 60 – 74 лет данные изменения были статистически значимы. К 12-му месяцу мы наблюдали постепенное восстановление параметров эрекции, сравнимое с исходными показателями, и только в возрастной группе 18 – 44 года отмечено значительное улучшение эректильной функции (табл. 1).
Табакокурение. Распространённость вредной привычки составила 30,7%. В группе пациентов с длительным стажем курения как исходные показатели эректильной функции, так и наблюдаемые через 3 и 12 месяцев были значительно хуже, чем в группе пациентов без табакокурения в анамнезе. При этом в обеих группах мы также наблюдали ухудшение эректильной функции на 3-м месяце мониторинга и восстановление её к 12-му месяцу (табл. 2).
Сопутствующие заболевания. Показатели МИЭФ-5 были значимо ниже у пациентов с ишемической болезнью сердца на 12-м месяце мониторинга, при артериальной гипертензии — на 3-м и 12-м месяцах. Наличие сахарного диабета не оказывало влияния на качество эрекции мужчин ни в одной из контрольных точек (табл. 3).
Параметры стриктур. Исходные показатели баллов МИЭФ-5 не зависели от протяжённости дефекта уретры и наличия в анамнезе предшествующего лечения стриктур, однако пациенты с рецидивными и протяжёнными стриктурами уретры имели более выраженное ухудшение эректильной функции к 3-му месяцу наблюдения. Через год после уретропластики данные различия сохранялись между пациентами с первичными и рецидивными стриктурами, в то время как различий в зависимости от протяжённости стриктур мы не наблюдали (табл. 4).
Техники хирургии. Уретропластики с пересечением спонгиозного тела выполнены в 62,7% случаев (анастомотическая пластика уретры «конец-в-конец» — 78 (51,0%) больных, анастомотическая пластика уретры по типу «бульбопростатический анастомоз» — 7 (4,6%), аугментационная пластика уретры с использованием слизистой ротовой полости по типу «аугментационный анастомоз» — 11 (7,2%)), без пересечения — в 37,3% (анастомотическая уретропластика без пересечения спонгиозного тела — 42 (27,5%), аугментационная уретропластика с использованием кожного флэпа — 7 (4,6%), аугментационная уретропластика без пересечения спонгиозного тела с использованием слизистой ротовой полости — 8 (5,2%) больных).
Значимых статистических различий между группами в зависимости от методики хирургии не выявлено ни в одной из контрольных точек оценки. Распределение пациентов по степени выраженности ЭД в зависимости от методики хирургии и периода оценки показателей представлено на рисунке, демонстрирующем уменьшение частоты тяжёлой и умеренной степени ЭД к 12-му месяцу наблюдения в сравнении с результатами, полученными на 3-м месяце.
Многофакторный анализ. Прогностическая модель для определения вероятности развития ЭД включала возраст пациентов, сопутствующую патологию, характеристики стриктур уретры, различные методики хирургического вмешательства. Предикторами развития ЭД на 3-м месяце наблюдения стали возраст, артериальная гипертензия и качество эректильной функции в дооперационном периоде (табл. 6).
Таблица 1. Показатели эректильной функции в зависимости от возраста пациентов
|
Возраст, лет |
МИЭФ-5, баллы (Me [Q₁ – Q3]) |
||||||
|
Исходно |
Этапы наблюдения |
||||||
|
3 месяца |
p |
6 месяцев |
p |
12 месяцев |
p |
||
|
18 – 44 |
21,5 [ 12,5 – 25,0] |
21,0 [ 14,5 – 22,0] |
0,973 |
21,0 [ 17,0 – 23,6] |
0,177 |
23,0 [ 22,0 – 24,8] |
< 0,001 |
|
45 – 59 |
19,0 [ 11,0 – 21,5] |
12,0 [ 6,0 – 16,5] |
0,041 |
15,0 [ 12,0 – 19,0] |
0,334 |
21,00 [ 17,5 – 22,5] |
0,036 |
|
60 – 74 |
20,0 [ 14,0 – 21,0] |
10,0 [ 5,0 – 12,5] |
< 0,001 |
11,0 [ 7,0 – 15,0] |
< 0,001 |
18,00 [ 15,5 – 21,0] |
0,189 |
|
≥ 75 |
16,0 [ 16,0 – 17,0] |
5,0 [ 5,0 – 15,0] |
0,123 |
10,0 [ 6,0 – 17,0] |
0,208 |
17,00 [ 12,0 – 18,0] |
0,833 |
|
Примечание. МИЭФ-5 — международный индекс эректильной функции 5 |
|||||||
Таблица 2. Показатели эректильной функции в зависимости от табакокурения
|
Табакокурение |
МИЭФ-5, баллы (Me [Q₁ – Q3]) |
||
|
исходно |
3 месяца |
12 месяцев |
|
|
Да |
16,0 [ 11,5 – 21,0] |
10,0 [ 5,0 – 16,0] |
17,0 [ 14,0 – 21,0] |
|
Нет |
21,0 [ 14,0 – 23,0] |
14,50 [ 8,5 – 21,0] |
22,00 [ 19,6 – 23,0] |
|
P |
0,015 |
0,005 |
< 0,001 |
|
Примечание. МИЭФ-5 — международный индекс эректильной функции 5 |
|||
Таблица 3. Показатели эректильной функции в зависимости от сопутствующих заболеваний
|
Заболевания |
МИЭФ-5, баллы (Me [Q1 – Q3]) |
|||
|
исходно |
3 месяца |
12 месяцев |
||
|
ИБС |
да |
19,0 [ 13,0 – 21,0] |
12,0 [ 5,0 – 17,5] |
19,0 [ 16,0 – 22,0] |
|
нет |
19,0 [ 13,26 – 23,0] |
14,00 [ 5,0 – 21,0] |
21,00 [ 17,0 – 23,0] |
|
|
p |
0,458 |
0,163 |
0,029 |
|
|
АГ |
да |
18,0 [ 14,0 – 21,0] |
10,0 [ 5,0 – 16,0] |
18,0 [ 15,0 – 21,0] |
|
нет |
20, [ 10,0 – 24,0] |
16,0 [ 10,0 – 21,0] |
22,0 [ 19,76 – 24,0] |
|
|
p |
0,260 |
0,001 |
< 0,001 |
|
|
СД 2 типа |
да |
16,0 [ 12,0 – 22,0] |
16,0 [ 5,0 – 21,0] |
21,00 [ 20,00 – 22,0] |
|
нет |
19,0 [ 14,0 – 22,0] |
13,0 [ 5,0 – 20,0] |
21,0 [ 16,8 – 23,0] |
|
|
p |
0,386 |
0,812 |
0,856 |
|
|
Примечание. МИЭФ-5 — международный индекс эректильной функции 5; ИБС — ишемическая болезнь сердца; АГ — артериальная гипертензия; СД — сахарный диабет |
||||
Таблица 4. Показатели эректильной функции в зависимости от параметров стриктур
|
Параметры |
МИЭФ-5, баллы (Me [Q1 – Q3]) |
|||
|
исходно |
3 месяца |
12 месяцев |
||
|
Протяжённость СУ |
< 3 см |
18,0 [ 12,0 – 22,0] |
16,0 [ 6,5 – 21,0] |
21,0 [ 18,0 – 23,0] |
|
≥ 3 см |
20,5 [ 14,0 – 22,0] |
12,0 [ 5,0 – 15,8] |
21,0 [ 17,0 – 23,0] |
|
|
p |
0,653 |
0,038 |
0,407 |
|
|
Лечение СУ в анамнезе |
нет |
19,0 [ 12,0 – 22,0] |
14,0 [ 7,0 – 21,0] |
22,0 [ 18,0 – 23,0] |
|
да |
19,0 [ 15,6 – 22,8] |
5,0 [ 5,0 – 15,5] |
18,5 [ 15,3 – 21,0] |
|
|
p |
0,668 |
0,011 |
0,019 |
|
|
Примечание. МИЭФ-5 — международный индекс эректильной функции 5; СУ — стриктура уретры |
||||
Таблица 5. Показатели эректильной функции в зависимости от степени пересечения спонгиозного тела
|
Спонгиозное тело |
МИЭФ-5, баллы (Me [Q1 – Q3]) |
|||
|
исходно |
3 месяца |
6 месяцев |
12 месяцев |
|
|
С пересечением |
18,0 [ 10,0 – 22,0] |
15,0 [ 5,0 – 21,0] |
16,0 [ 11,0 – 21,0] |
21,0 [ 17,0 – 23,0] |
|
Без пересечения |
21,0 [ 15,8 – 22,3] |
11,5 [ 5,0 – 16,0] |
14,0 [ 10,0 – 19,3] |
21,0 [ 16,8 – 23,0] |
|
P |
0,076 |
0,155 |
0,233 |
0,894 |
|
Примечание. МИЭФ-5 — международный индекс эректильной функции 5 |
||||
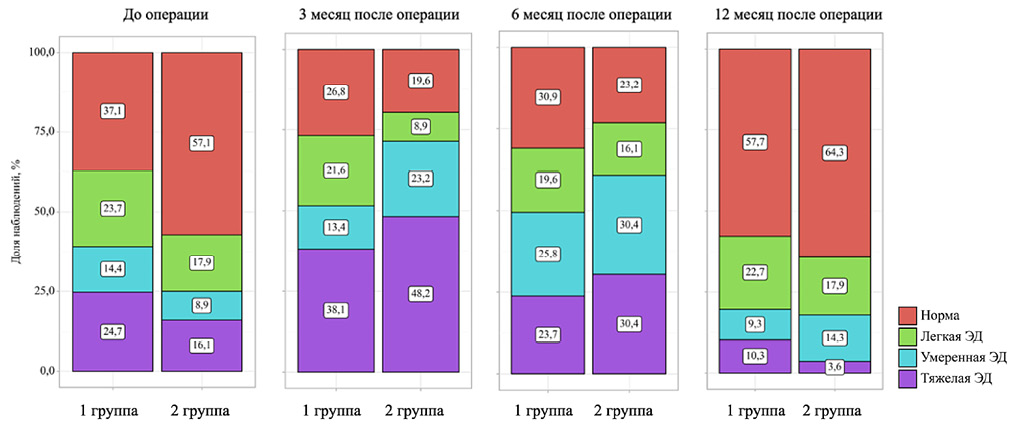
Рисунок. Динамика степени эректильной дисфункции при пересекающих (группа 1) и непересекающих (группа 2) пластиках уретры
Таблица 6. Предикторы вероятности развития эректильной дисфункции после операции: многофакторный анализ
|
Предикторы * |
Многофакторный анализ |
|||
|
НОШ; 95% ДИ |
P |
СОШ; 95% ДИ |
P |
|
|
Возраст |
1,045; 1,022 – 1,068 |
< 0,001 |
1,082; 1,038 – 1,127 |
< 0,001 |
|
Артериальная гипертензия |
2,468; 1,223 – 4,983 |
0,012 |
4,608; 1,089 – 19,511 |
0,038 |
|
ЭД в дооперационном периоде |
0,200; 0,096 – 0,420 |
< 0,001 |
0,046; 0,013 – 0,160 |
< 0,001 |
|
Примечание. * — в таблице приведены только факторы, продемонстрировавшие прогностическую значимость; НОШ — нескорректированное отношение шансов; СОШ — скорректированное отношение шансов; ДИ — доверительный интервал; ЭД — эректильная дисфункция |
||||
Обсуждение
Значительное время основное внимание в реконструктивной хирургии уретры было приковано преимущественно к улучшению функциональных показателей мочеиспускания и обеспечению безрецидивного течения стриктурной болезни. Современная концепция ведения пациентов со стриктурами уретры требует от оперирующего хирурга не только достижения результатов в восстановлении проходимости уретры, но и минимизации влияния хирургического вмешательства на сексуальную сферу пациента, предотвращая развитие сексуальных дисфункций [6]. В понятие сексуальная дисфункция после реконструктивной хирургии мочеиспускательного канала входят такие состояния, как ЭД, эякуляторные и оргазмические нарушения, искривления и укорочения полового члена, формирование хорды и расстройства чувствительности в области половых органов.
Данные о частоте развития ЭД после анастомотической и заместительной пластики уретры одними из первых опубликовали A.R. Mundy et al. в 1993 году [7]. В группе пациентов (n = 86), которым была выполнена анастомотическая пластика уретры, временная ЭД в послеоперационном периоде отмечена в 53% случаев, постоянная ЭД — в 5%. В группе пациентов (n = 114), подвергнутых заместительной пластике уретры, временная ЭД зафиксирована у 38% пациентов, постоянная ЭД — у 0,9%. В исследовании J.T. Anger et al. (2007) проанализированы изменения эректильной функции у 25 пациентов со стриктурой бульбозного отдела уретры в пред- и послеоперационном периодах. Согласно валидизированному опроснику МИЭФ-15 (домен: EF) отмечено снижение баллов с 26,9 до 24,8 (p = 0,13), при этом у 4% пациентов отмечено развитие ЭД de novo [8].
Результаты подобных исследований показали высокую частоту сексуальных нарушений после пластики уретры, что послужило почвой для последующего изучения генеза ЭД и разработки техник, минимизирующих хирургическую травму, нарушение кровотока в спонгиозном теле и, как следствие, сохраняющих изначальную пенильную гемодинамику. Одной из таких методик является реконструкция мочеиспускательного канала без пересечения спонгиозного тела [9-11].
Эффективность данной техники наглядно представлена в работе D.W. Chapman et al. (2019) [12], в которой установлено, что при 64,2 месяца наблюдения развитие ЭД de novo у пациентов, перенёсших анастомотическую пластику «конец-в-конец», составило 14,3%, в то время как при анастомотической пластике уретры без пересечения спонгиозного тела ЭД de novo отмечена только в 4,3% случаев (p = 0,008).
Результаты нашего исследования не выявили статистических различий в количественных характеристиках эректильной функции (баллы МИЭФ-5) в зависимости от применения пересекающих и непересекающих спонгиозное тело техник. Однако развитие в 4,4% случаев ЭД de novo отмечено при хирургии, предполагающей пересечение губчатого тела (пластика уретры «конец-в-конец» — 2 случая, аугментационный анастомоз — 1 случай). Кроме того, данные пациенты имели в анамнезе один и более факторов риска развития ЭД.
Также наше исследование подтвердило, что нарушение эректильной функции носит транзиторный характер и к 12-му месяцу наблюдения отмечается постепенное её восстановление. Ранее было установлено, что время, необходимое для полного восстановления эректильной функции после операции у пациентов в возрасте до 40 лет, составляет 6 месяцев [13]. В проспективном исследовании B.A. Erickson et al. (2007) развитие ЭД наблюдалось у 40% пациентов после пластики стриктур передней уретры, с полным регрессом симптоматики в течение 6 месяцев [14]. Вероятно, ЭД в первые месяцы послеоперационного периода связана с хирургической травмой, течением раневого процесса, дренированием нижних мочевыводящих путей. Кроме того, как показало наше исследование, отрицательное влияние на динамику восстановления эректильной функции после уретропластики оказывают: пожилой возраст пациентов, курение табачной продукции, наличие сердечно-сосудистых заболеваний и некоторые параметры стриктурной болезни (протяжённые и рецидивные стриктуры).
Связь ЭД с возрастом пациентов показана и в других работах. Так, A. Urkmez et al. (2018) представили данные о состоянии эректильной функции при стриктурной болезни у пациентов в возрастных группах < 65 и > 65 лет. Установлено, что исходный и послеоперационный средний балл МИЭФ-15 (domen: EF) у пациентов < 65 лет (21,68 и 21,6 балла) выше, чем у пациентов старшей возрастной группы (17,91 и 13,58 балла) [15].
P. Bhowmik et al. (2022) также доказали, что изменения эректильной функции пациентов в возрасте < 40 лет имеют преходящий характер с полным восстановлением исходного уровня к 6-му месяцу в отличие от пациентов в возрасте > 40 лет [16]. Эти данные полностью подтверждаются нашим исследованием, где мы наблюдали нормализацию эректильной функции у пациентов 18 – 44 лет уже через полгода, тогда как в более старших возрастных группах эрекция восстанавливалась только через год после пластики уретры. Помимо того, в работе P. Bhowmik et al. (2022) установлено, что предикторами ухудшения эректильной функции являются протяжённость стриктуры и отдел поражённой уретры. Наше исследование также показало, что протяжённость стриктуры влияет на сроки восстановления эректильной функции наряду с предшествующим лечением стриктур.
Заключение
Нарушения эректильной функции после хирургического лечения стриктур уретры имеют преимущественно транзиторный характер. Развитие ЭД и динамика восстановления эректильной функции после уретропластики обусловлены не только хирургической травмой и длительным периодом восстановления пациентов, но и исходным общим соматическим состоянием пациента. Значительному ухудшению эректильной функции подвержены пациенты старших возрастных групп с сердечно-сосудистыми заболеваниями, наличием вредных привычек (табакокурение), протяжёнными стриктурами, а также ранее выполненными хирургическими вмешательствами на уретре.
Список литературы
1. Braun M, Wassmer G, Klotz T, Reifenrath B, Mathers M, Engelmann U. Epidemiology of erectile dysfunction: results of the 'Cologne Male Survey'. Int J Impot Res. 2000;12(6):305-11. DOI: 10.1038/sj.ijir.3900622
2. Пушкарь Д.Ю., Камалов А.А., Аль-Шукри С.Х., Еркович А.А., Коган М.И., Павлов В.Н., Журавлев В.Н., Берников А.Н. Эпидемиологическое исследование распространенности эректильной дисфункции в Российской Федерации. Русский медицинский журнал. 2012;(3):112-115. eLIBRARY ID: 17826950; EDN: PACUHF
3. Rosen RC. Psychogenic erectile dysfunction. Classification and management. Urol Clin North Am. 2001;28(2):269-78. DOI: 10.1016/s0094-0143(05)70137-3
4. Laumann EO, West S, Glasser D, Carson C, Rosen R, Kang JH. Prevalence and correlates of erectile dysfunction by race and ethnicity among men aged 40 or older in the United States: from the male attitudes regarding sexual health survey. J Sex Med. 2007;4(1):57-65. DOI: 10.1111/j.1743-6109.2006.00340.x
5. Mulhall JP, Luo X, Zou KH, Stecher V, Galaznik A. Relationship between age and erectile dysfunction diagnosis or treatment using real-world observational data in the USA. Int J Clin Pract. 2016;70(12):1012-1018. DOI: 10.1111/ijcp.12908
6. Коган М.И., Глухов В.П., Ильяш А.В., Бугаенко В.А., Митусов В.В., Сизякин Д.В. Многоэтапные операции при стриктурах передней уретры: оценка сексуальной функции. Экспериментальная и клиническая урология. 2022;15(4):96-101. DOI: 10.29188/2222-8543-2022-15-4-96-101
7. Mundy AR. Results and complications of urethroplasty and its future. Br J Urol. 1993;71(3):322-5. DOI: 10.1111/j.1464-410x.1993.tb15951.x
8. Anger JT, Sherman ND, Webster GD. The effect of bulbar urethroplasty on erectile function. J Urol. 2007;178(3 Pt 1):1009-11; discussion 1011. DOI: 10.1016/j.juro.2007.05.053
9. Jordan GH, Eltahawy EA, Virasoro R. The technique of vessel sparing excision and primary anastomosis for proximal bulbous urethral reconstruction. J Urol. 2007;177(5):1799-802. DOI: 10.1016/j.juro.2007.01.036
10. Andrich DE, Mundy AR. Non-transecting anastomotic bulbar urethroplasty: a preliminary report. BJU Int. 2012;109(7):1090-4. DOI: 10.1111/j.1464-410X.2011.10508.x
11. Котов С.В. Анастомотическая уретропластика без пересечения спонгиозного тела – новый метод уретропластики для лечения коротких стриктур бульбозного отдела уретры. Экспериментальная и клиническая урология. 2015;(3):68-71. eLIBRARY ID: 25622728; EDN: VOSGLJ
12. Chapman DW, Cotter K, Johnsen NV, Patel S, Kinnaird A, Erickson BA, Voelzke B, Buckley J, Rourke K. Nontransecting Techniques Reduce Sexual Dysfunction after Anastomotic Bulbar Urethroplasty: Results of a Multi-Institutional Comparative Analysis. J Urol. 2019;201(2):364-370. DOI: 10.1016/j.juro.2018.09.051
13. Xie H, Xu YM, Xu XL, Sa YL, Wu DL, Zhang XC. Evaluation of erectile function after urethral reconstruction: a prospective study. Asian J Androl. 2009;11(2):209-14. DOI: 10.1038/aja.2008.1
14. Erickson BA, Wysock JS, McVary KT, Gonzalez CM. Erectile function, sexual drive, and ejaculatory function after reconstructive surgery for anterior urethral stricture disease. BJU Int. 2007;99(3):607-11. DOI: 10.1111/j.1464-410X.2006.06669.x
15. Urkmez A, Yuksel OH, Ozsoy E, Topaktas R, Sahin A, Koca O, Ozturk MI. The effect of urethroplasty surgery on erectile and orgasmic functions: a prospective study. Int Braz J Urol. 2019;45(1):118-126. DOI: 10.1590/S1677-5538.IBJU.2018.0276
16. Bhowmik P, Sharma G, Sharma PK, Patawari PK, Dey S, Mandal S. Prospective study of de novosexual dysfunction after anterior urethroplasty: Causative factors, incidence, and recovery of function - A singlecenter experience. Urol Ann. 2022;14(1):60-66. DOI: 10.4103/ua.ua_24_21.
Об авторах
С. В. КотовРоссия
Сергей Владиславович Котов — д-р мед. наук, профессор
Москва
М. М. Ирицян
Россия
Михаил Матевосович Ирицян — канд. мед .наук
Москва
А. А. Клименко
Россия
Алексей Алексеевич Клименко
Москва
А. А. Манцов
Россия
Артём Андреевич Манцов
Москва
Рецензия
Для цитирования:
Котов С.В., Ирицян М.М., Клименко А.А., Манцов А.А. Эректильная функция у пациентов после пластики уретры. Вестник урологии. 2025;13(1):19-26. https://doi.org/10.21886/2308-6424-2025-13-1-19-26
For citation:
Kotov S.V., Iritsyan M.M., Klimenko A.A., Mantsov A.A. Erectile function in patients after urethral plastic surgery. Urology Herald. 2025;13(1):19-26. (In Russ.) https://doi.org/10.21886/2308-6424-2025-13-1-19-26













































